Prophylaxe 16.12.2019
Neue Klassifikation parodontaler und periimplantärer Erkrankungen
share
Seit einem Jahr liegt sie nun vor: die neue Klassifikation parodontaler und periimplantärer Erkrankungen. Tabelle 1 nach Caton et al.1 gibt einen Überblick. Klassifikationen ändern sich mit der Evolution des Wissens, wie Tabelle 2 darstellt. Auch die bisher international anerkannte Klassifikation der Parodontitis2 stellte bereits einen großen Fortschritt gegenüber den Vorläufern dar, indem sie erstmals auch gingivale Erkrankungen erfasste und die etwas arbiträre Einteilung der „Adult Periodontitis“ aufgrund eines erreichten Alters von 36 Jahren verließ. Aber auch bei der Unterscheidung in „chronische“ und „aggressive“ Parodontitis wurde immer bemängelt, dass die Überschneidungen zu groß seien und biologisch keine wesentlich unterschiedliche Pathobiologie vorliege.
Der große Wissenszuwachs durch Grundlagenforschung, Epidemiologie und prospektive Studien in den letzten 20 Jahren brachte die Notwendigkeit mit sich, alle vorliegende Evidenz erneut eingehend zu sichten. Dies führte schließlich zur Entwicklung dieses neuen Rahmenwerks einer Klassifikation mit Stadien und Graden, wie sie z. B. bei Tumorklassifizierungen bereits seit Langem üblich sind. Schweregrad und die Komplexität können für jeden Einzelnen besser eingeteilt werden und allgemeinmedizinische (Risiko-)Faktoren (wie Rauchen oder Zuckerkrankheit) erfahren eine gebührende Berücksichtigung. In dem vorliegenden Beitrag soll vor allem auf die gänzlich neuen Aspekte hingewiesen werden.

Was ist ganz neu?
- Erstmals gibt es eine neue Definition von parodontaler Gesundheit, im normalen sowie im reduzierten Parodont.
- Zudem wird bei der Identifikation in drei Formen von Parodontitis unterteilt: Parodontitis, nekrotisierende Parodontalerkrankungen und Parodontitis als Manifestation einer systemischen Erkrankung (vgl. Tab. 1). „Aggressive“ und „chronische“ Parodontitis werden durch eine Staging- und Grading-Matrix (Stadien und Grade) ersetzt.
- Mukogingivale Rezessionen werden neu klassifiziert.
- Erstmals werden periimplantäre Gesundheit, periimplantäre Mukositis und Periimplantitis definiert.
1. Definition gingivale/parodontale Gesundheit
Parodontale Gesundheit ist durch das Fehlen einer klinisch messbaren Entzündung definiert. Als primäre Messgröße gilt Blutung auf Sondieren (BOP); die Sondierungstiefe (ST) gilt als Abgrenzung zur Parodontitis. Das primäre Instrument zur parodontalen Diagnostik ist die graduierte Parodontalsonde.
Gingivale Gesundheit: keine Schwellung, keine Rötung, ST ≤ 3 mm, Blutung auf Sondieren (BOP) < 10 %
Gingivale Gesundheit kann sowohl im intakten Parodont ohne klinischen Attachmentverlust (AV)/Knochenverlust als auch in einem reduzierten Parodont vorliegen. Das bedeutet, es liegt ein AV entweder aufgrund von Rezessionen/nach chirurgischer Kronenverlängerung oder erfolgreich abgeschlossener Parodontitistherapie vor.
Die Behandlung einer Gingivitis führt zur Wiederherstellung völliger klinischer gingivaler Gesundheit. Auch nach erfolgreich behandelter Parodontitis können gesunde Verhältnisse vorliegen, jedoch bleibt ein erhöhtes Risiko, sodass diese Patienten eine unterstützende Parodontaltherapie (UPT) in einem individuellen Intervall benötigen.
2. Drei Formen von Parodontitis
Parodontitis liegt vor, wenn es zu AV durch Entzündung gekommen ist. Klinischer AV (Clinical Attachment Loss – CAL) setzt sich zusammen aus ST plus allfälligen Rezessionen (Rez). Unter Bezugnahme auf die Schmelz-Zement-Grenze (SZG) wird das Gebiss mit einer standardisierten Parodontalsonde sowie einem Druck von 0,2 N auf das Vorliegen von CAL überprüft. (Hinweis: Die Genauigkeit des Sondierens hängt von Erfahrung, Druck, Sonde, Anatomie, Zahnstellung, Vorhandensein von Zahnstein oder Restaurationsrändern und Erkennbarkeit der SZG ab.)
Definition des „Parodontitisfalls“:
- approximaler AV ≥2mm an ≥2 nicht benachbarter Zähnen
- nicht durch endodontische Probleme, Wurzelfraktur, Karies oder traumatische Rezession bedingt
Formen der Erkrankung
Die Differenzialdiagnose, welche Form der Krankheit vorliegt, basiert auf der Anamnese, den spezifischen Anzeichen und Symptomen nekrotisierender Parodontitis und dem Vorhandensein oder Fehlen einer systemischen Erkrankung, die das Immunsystem des Wirts verändert. Nekrotisierende Parodontitis ist durch Schmerzen, Ulzera/Pseudomembranen, Papillenverlust und manchmal auch durch freiliegenden Knochen charakterisiert. Je nach Ausmaß des AV werden drei Formen unterschieden: (nekrotisierende Gingivitis, Parodontitis oder Stomatitis). Sie stehen immer im Zusammenhang mit Einschränkungen der Immunabwehr des Wirts. „Parodontitis als Manifestation systemischer Erkrankungen“ ist mit seltenen, meist monogenetischen Syndromen (z. B. Trisomie 21, Papillon-Lefèvre-Syndrom) verbunden, und die Einstufung erfolgt auf der primären systemischen Erkrankung gemäß aktuellem ICD-Code. Diese internationale statistische Klassifikation der Krankheiten und verwandter Gesundheitsprobleme (International Statistical Classification of Diseases and Related Health Problems) ist das wichtigste weltweit anerkannte Klassifikationssystem für medizinische Diagnosen. Es wird von der Weltgesundheitsorganisation (WHO) herausgegeben und oft kurz auch als Internationale Klassifikation der Krankheiten bezeichnet. Die aktuelle Ausgabe ist ICD-10.
Vier Stadien und drei Grade statt „aggressiver“ und „chronischer“ Parodontitis
Diese charakterisieren nun die jeweilige vorliegende Erkrankung, was Vorteile in Hinsicht auf eine individualisierte Diagnose und Therapie bringt.
Stadium = Schweregrad zum Zeitpunkt der Diagnose + Komplexität der Behandlung
Grad = Information über biologische Merkmale + Progressionsrate + Risikobeurteilung
Was ist Staging?
Die vier Stadien beschreiben den Schweregrad und Komplexität der Erkrankung. Durch das Staging werden Schwere und Ausmaß des parodontalen Abbaus bei Diagnosestellung, gemessen durch Ausmaß des klinischen AV oder des radiologischen Knochenverlustes des am schwersten betroffenen Zahnzwischenraumes klassifiziert. Dies schließt den Zahnverlust ein, der auf Parodontitis zurückzuführen ist (≤ 4, ≥ 5 Zähne).
Eine weitere Dimension ist die Komplexität der Behandlung. Faktoren wie Sondierungstiefen, Art des Knochenverlustes (vertikal und/oder horizontal), Furkationsbeteiligung, erhöhte Zahnmobilität, Anzahl der fehlenden Zähne, Bisskollaps und Verlust der Kaufunktion werden in die neue Klassifizierung mit einbezogen.
Das Ausmaß der Erkrankung, definiert durch die Anzahl und die Verteilung von Zähnen mit parodontalem Abbau, wird ebenfalls in die Klassifikation integriert.
< 30 Prozent der Zähne betroffen = lokalisierte Parodontitis
≥ 30 Prozent der Zähne betroffen = generalisierte Parodontitis (Abb. 1)
Was ist Grading?
Hierbei wird das Risiko (indirekt) bzw. die Evidenz (direkt) für rasche Progression eingeschätzt sowie die wahrscheinliche Reaktion auf die Therapie. Dies kann die Intensität der Therapie und der nötigen Sekundärprävention in der Erhaltungsphase vorgeben. Der direkte Nachweis für Progression beruht auf evtl. vorhandenen älteren Röntgenaufnahmen. Indirekte Evidenz basiert auf der Einschätzung des Knochenverlusts am schlimmsten betroffenen Zahn im Gebiss als Funktion des Alters (radiologischer Knochenverlust, BL) in Prozent der Wurzellänge, geteilt durch das Alter (Abb. 1, Zahn 11/21). Der Parodontitisgrad wird weiter durch das Vorhandensein von Risikofaktoren (Rauchen, Diabetes mellitus) modifiziert. Grundsätzlich wird hierbei von einer moderaten Progressionsrate ausgegangen (Grad B) und kontrolliert, ob Faktoren vorliegen, welche die Anwendung von Grad C (instabile Situation) rechtfertigen würden. Grad A wird angewendet, sobald die Krankheit gestoppt und Stabilität erreicht ist.
Grad A: BL 0,25–1, Nichtraucher, kein Diabetes/Normoglykämie
Grad B: BL 1, <10 Zigaretten/Tag, HbA1c <7,0%
Grad C: BL>1, ≥10 Zigaretten/Tag, HbA1c ≥7,0%
 Abb. 1: 30-jährige Patientin, starke Raucherin (15 Zigaretten/Tag); höchster approximaler AV bei 11/21 (ca. 60%; BL/Alter >1). © Bruckmann
Abb. 1: 30-jährige Patientin, starke Raucherin (15 Zigaretten/Tag); höchster approximaler AV bei 11/21 (ca. 60%; BL/Alter >1). © Bruckmann
Vorgehen im Einzelfall
Die umfassende Mundgesundheitsbeurteilung neuer Patienten umfasst auch eine Parodontalbeurteilung. Falls keine parodontale Erkrankung aus der Vorgeschichte erhoben wird oder die klinische Untersuchung nicht auf ein Vorhandensein hinweist (keine schwarzen Dreiecke oder auffälligen Rezessionen), ist ein parodontales Screening (PSI) erforderlich. (Hinweis: Die Aussage basiert auf dem Patientenratgeber: „Parodontitis. Verstehen, vermeiden und behandeln.“ www.dgparo.de/patientenportal/patientenratgeber) Diese bestätigte entweder das Fehlen einer Parodontalerkrankung oder führt zur Diagnose einer lokalisierten/generalisierten Gingivitis (PSI max. Grad 2) bzw. dem Verdacht auf Parodontitis (PSI 3 oder 4), der weitere klinische und radiologische Untersuchungen auslöst. Ziel ist es, am Ende folgende Aussagen zur vorliegenden Erkrankung treffen zu können: Art der Parodontitis, Ausdehnung, Stadium, Grad, Stabilität der klinischen Situation und Risikofaktor(en). Im Einzelfall könnte dies z. B. heißen: Parodontitis, generalisiert, Stadium III, Grad C, derzeit stabil, Risikofaktor Rauchen (15 Zigaretten/Tag; Abb. 1).
3. Mukogingivale Deformitäten und Zustände
Gegenüber der alten Klassifikation („Miller Klassifikation“)3 werden nun auch der parodontale Phänotyp (dünn/dick), der approximale Attachmentverlust, der Zustand der Wurzeloberfläche sowie die Sichtbarkeit der Schmelz-Zement-Grenze berücksichtigt. Tabelle 3 zeigt ein Schema für die Klassifikation mukogingivaler Zustände (gingivaler Phänotyp) und gingivaler Rezessionen. Dies ermöglicht eine bessere Voraussagbarkeit chirurgischer Interventionsmöglichkeiten bzw. vorbereitender konservativer Therapienotwendigkeiten (Abb. 2 und 3).
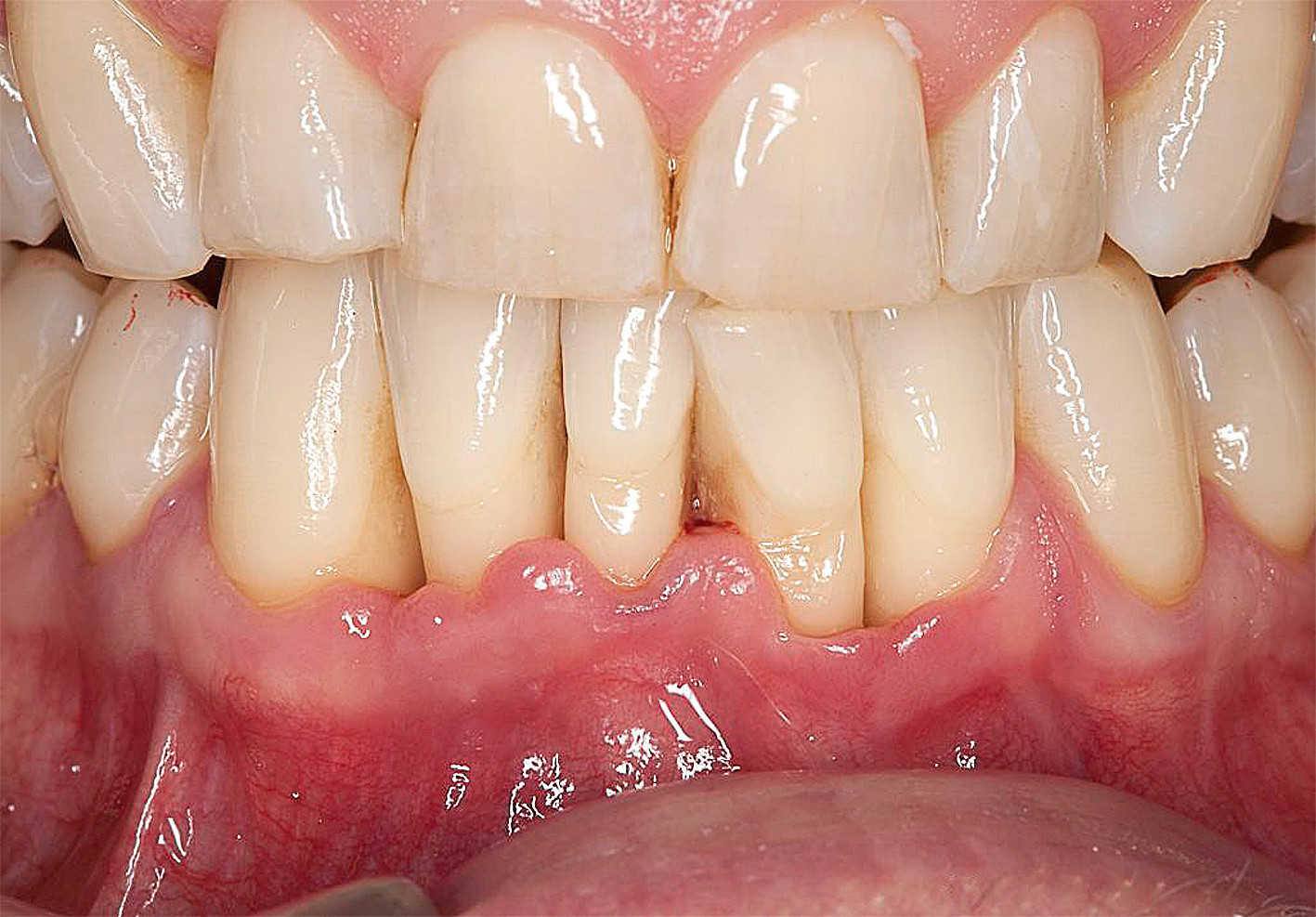 Abb. 2: Beispiel für RT3 (approximaler AV ist höher als bukkaler AV) an Zahn 31–43 mesial. GD: dicker Phänotyp, wenig KG, SZG: A, Stufe: – © Bruckmann
Abb. 2: Beispiel für RT3 (approximaler AV ist höher als bukkaler AV) an Zahn 31–43 mesial. GD: dicker Phänotyp, wenig KG, SZG: A, Stufe: – © Bruckmann
4. Periimplantäre Erkrankungen und Zustände (vgl. Tab. 1)
Die klinische Methode zur Erkennung einer Entzündung sollte eine visuelle Untersuchung, Sondierung mit einer parodontalen Sonde und manuelle Palpation umfassen. Es wurde dabei keine kritische Sondierungstiefe definiert, die mit der periimplantären Gesundheit einhergeht. Von größerer Bedeutung sind hier die Abwesenheit von Bluten und/oder Suppuration bei schonungsvollem Sondieren, keine Erhöhung der Sondierungstiefe im Vergleich zu früheren Untersuchungen, kein radiologischer Knochenverlust.
Periimplantäre Mukositis
Klinisches Hauptmerkmal ist das Bluten beim schonungsvollen Sondieren, evtl. Rötung, Schwellung und/oder Suppuration. Zudem gibt es keinen über die initiale Remodellierung hinausgehenden Knochenabbau.
Periimplantitis
Hier wurde ein krankhafter Zustand definiert, der sich durch Entzündung (BoP/Pusaustritt/größer werdende ST) der periimplantären Mukosa und progressiven Knochenabbau zeigt sowie mit schlechter Plaquekontrolle und schwerer Parodontitis in der Anamnese in Zusammenhang steht.
Diagnose (falls keine Vorbefunde vorhanden): Kombination von BoP/Pusaustritt + Sondierungstiefen ≥ 6 mm + Knochenniveau ≥ 3 mm apikal des am meisten koronal befindlichen intraossären Implantatanteils.
 Abb. 3: Beispiel für eine Stufenbildung an Zahn 26. SZG: B, Stufe: + © Bruckmann
Abb. 3: Beispiel für eine Stufenbildung an Zahn 26. SZG: B, Stufe: + © Bruckmann
Zusammenfassung und Ausblick
Ziel der Konsensuskonferenz war eine weltweit einheitliche, auf gesicherten Forschungsergebnissen basierende Klassifikation. Diese soll die bestmögliche Diagnostik und Versorgung von Patienten ermöglichen. Die Umsetzung in die Praxis wird sicher noch einige Zeit benötigen und eventuell noch Nachbesserungen erfahren. Schulungsunterlagen zur Implementation in der Praxis sind in Vorbereitung. Die Hoffnung aller Beteiligten geht dahin, dass die neue Klassifikation parodontaler und periimplantärer Erkrankungen weltweite Akzeptanz finden und sich im klinischen Alltag als praktisch und hilfreich erweisen wird, um so schlussendlich die Betreuung der Patientinnen und Patienten zu verbessern. Es geht darum, parodontale/periimplantäre Erkrankungen zu verhindern oder frühzeitig zu erkennen und der richtigen Therapie zuzuführen.
Die vollständige Literaturliste gibt es hier.
Der Beitrag ist im Prophylaxe Journal erschienen.
Foto: zlikovec – stock.adobe.com