Oralchirurgie 28.02.2011
Nachblutungen - Chirurgische Problemfälle vermeiden
share
In den letzten Jahren hat die Anzahl an Patienten, die unter Dauertherapie mit oralen Antikoagulantien stehen, nicht zuletzt aufgrund der Altersentwicklung in der Bevölkerung deutlich zugenommen. Die zahnärztlich-chirurgische Behandlung von Patienten, die entweder durch eine medikamentös verursachte oder angeborene Gerinnungsstörung ein erhöhtes Blutungsrisiko aufweisen, stellen für den niedergelassenen Zahnarzt eine besondere Herausforderung dar.
Um Komplikationen bei der Durchführung von zahnärztlich-chirurgischen Maßnahmen zu vermeiden, ist es von besonderer Wichtigkeit, Patienten mit Blutungsrisiken zu erkennen und das erhöhte Blutungsrisiko dieser Patientengruppe bezüglich des geplanten Eingriffes richtig einzuschätzen. Das Ziel dieses Artikels ist eine Übersicht über die häufigsten Ursachen für angeborene und erworbene Gerinnungsstörungen und ein Überblick über das therapeutische Vorgehen, um das Blutungsrisiko zu minimieren.
1. Die physiologische Gerinnung
Die physiologische Blutstillung (Hämostase) beruht auf dem einwandfreien Zusammenwirken von Blutgefäßen, Thrombozyten und Gerinnungsfaktoren. Nach Verletzung der Gefäßwand erfolgt zunächst die primäre Hämostase durch eine Vasokonstriktion und Bildung des („weißen“) Plättchenthrombus durch Adhäsion und Aggregation der Thrombozyten. Die sekundäre Hämostase (plasmatische Gerinnung) entspricht der eigentlichen Aktivierung der Blutgerinnungskaskade (Gerinnungsfaktoren), deren Aktivierung über das sog. intrinsische oder extrinsische System erfolgen kann. Der primäre Thrombozytenthrombus wird durch Fibrin stabilisiert und unter Einschluss weiterer korpuskulärer Blutbestandteile entsteht ein der Gefäßwand anhaftender sog. „roter“ Thrombus. Im Anschluss daran muss das gebildete Fibringerinnsel durch eine funktionstüchtige Fibrinolyse wieder aufgelöst werden, damit die Heilung stattfinden bzw. das Blutgefäß rekanalisiert werden kann.
2. Überprüfung der Gerinnung
Eine einfache Überprüfung der Gerinnung kann durch die Messung der Blutungszeit (Normalwert bis 7 Minuten) erfolgen. Sie ist verlängert bei thrombozytären und vaskulär bedingten Gerinnungsstörungen. Da sie jedoch in Abhängigkeit verschiedener Patientenfaktoren (Alter, Hormonstatus, Körpertemperatur) starken individuellen Schwankungen unterliegt, besitzt sie eine nur unzureichende Aussagekraft bezüglich der zu erwartenden Blutung.
Bei Verdacht auf das Vorliegen einer plasmatischen Gerinnungsstörung eignen sich zunächst Globaltests zur Eingrenzung des vermuteten Hämostasedefektes. Die Prothrombinzeit/Thromboplastinzeit nach Quick dient der Überprüfung des extrinsischen Systems und der Vitamin K-abhängig in der Leber gebildeten Gerinnungsfaktoren. Da Cumarine (Marcumar®) die Vitamin K-abhängige Synthese der Gerinnungsfaktoren in der Leber hemmen, kann ihre Wirkung mithilfe des Quick-Wertes kontrolliert werden. Da jedoch die Bestimmung des Quick-Wertes labor- und methodenabhängig unterschiedlich ist und somit der Quick-Wert aus verschiedenen Labors nicht miteinander verglichen werden kann, wurde 1983 die INR (International Normalized Ratio) von der WHO eingeführt, um eine methoden- und geräteunabhängige Standardisierung der Prothrombinzeit zu ermöglichen. Dabei wird der INR-Wert mithilfe einer Formel in Bezug zu einem WHO-Referenzthromboplastin errechnet. Der INR-Wert eines Gesunden liegt bei ca. 1. Je stärker die Gerinnung gehemmt ist, desto höher ist der INR-Wert, im Gegensatz zum Quick-Wert (siehe Tabelle 1). Die aktivierte partielle Thromboplastinzeit (aPTT) dient zur Überprüfung des intrinsischen Systems (Faktor VIII, IX, XI und XII). Da unfraktioniertes Heparin (Liquemin®) die Wirkung von natürlichem Antithrombin verstärkt, kann dessen Wirkung mithilfe der aPTT kontrolliert werden.

Tabelle 1
Seitenanfang
3. Gerinnungsstörungen
Prinzipiell kann eine pathologische Blutungsneigung (hämorrhagische Diathese) durch eine Funktionsstörung der Blutgefäße (Vaskulopathien, in ca. 5% der Fälle), der Thrombozyten (Thrombozytäre Störungen, 65-80%) und der Gerinnungsfaktoren (Koagulopathien, 20-30%) bedingt sein. Durch das besondere Milieu in der Mundhöhle (Speichel, mechanische und mikrobielle Belastung) wirken sich Gerinnungsstörungen besonderes dort frühzeitig und nachhaltig aus. Für den chirurgisch tätigen Zahnarzt sind vor allem die angeborenen und erworbenen Defektkoagulopathien sowie die thrombozytären Störungen von besonderer Relevanz, während hingegen Vasopathien kaum eine klinische Bedeutung besitzen.
3.1 v. Willebrand-Syndrom (VWS)
Die häufigste angeborene Defektkoagulopathie mit einer Prävalenz von 0,8-1,3% ist das v. Willebrand-Syndrom (VWS), das auf den finnischen Internisten Erik Adolf von Willebrand zurückgeht, der diese Gerinnungsstörung erstmals im Jahre 1926 am Beispiel einer Blutersippe von den Ålandinseln beschrieb. Im deutschen Sprachgebrauch findet sich auch häufig noch die Verwendung „v. Willebrand-Jürgens-Syndrom“, eine Bezeichnung, die sich auf eine gemeinsame Publikation aus dem Jahre 1933 mit dem Leipziger Hämatologen Jürgens bezieht. Der v. Willebrand-Faktor (VWF) (FVIIIC, artihämophiles Globin) ist ein adhäsives Glykoprotein, das einerseits die Adhäsion der Thrombozyten an das verletzte Subendothel und die Thrombozytenaggregation vermittelt. Andererseits ist der VWF ein Trägerprotein für den Faktor VIII, mit gleichzeitiger protektiver Wirkung. Das VWS ist ein sehr heterogenes Krankheitsbild, das in unterschiedlicher schwerer Form angeboren oder erworben sein kann (siehe Tabelle 2).

Tabelle 2
Entsprechend heterogen sind auch die klinischen Symptome und Laborbefunde. Das Leitsymptom beim klassischen VWS ist die verlängerte Schleimhautblutung, die sich typischerweise nach einer Zahnextraktion manifestiert. Der Nachweis im Labor erfolgt durch Bestimmung von VWF-Aktivität, VWF-Antigen, FVIII-Aktivität.
3.2 Hämophilie
Die zweithäufigste angeborene Defektkoagulopathie ist die X-chromosomal rezessiv vererbte Hämophilie, die mit einer Prävalenz von 1:100.000 Männer auftritt. Bei der weitaus häufigeren Hämophilie A (85%) ist der Faktor VIII betroffen, im Gegensatz zur deutlich selteneren Hämophilie B (15%), bei welcher der Faktor IX inaktiv oder fehlend ist. Der Faktor VIII setzt sich aus zwei funktionellen Einheiten zusammen, dem eigentlichen X-chromosomal kodierten antihämophilen Globin (Faktor VIIIC) und dem oben bereits beschriebenen, auf Chromosom 12 kodierten VWF. Die Restfaktorenaktivität bestimmt den Schweregrad der Hämophilie (siehe Tabelle 3). Typisch ist in 2/3 der Fälle eine positive Familienanamnese, klinisch finden sich Nachblutungen bei normaler primärer Blutstillung, im Labor ist die aPTT verlängert, während Quick (INR) und Blutungszeit normal sind.

Tabelle 3
Seitenanfang
3.3 Vitamin K-Antagonisten
Die wichtigste erworbene Defektkoagulopathie entsteht durch eine Verminderung der Vitamin K (Vit. K) abhängigen Gerinnungsfaktoren (Faktoren II, VII, IX, X, Protein C und S). Vit. K, ein fettlösliches Vitamin, das in Anwesenheit von Gallesäuren entweder im Dünndarm resorbiert (Vit. K1) oder von Darmbakterien gebildet wird (Vit. K2), ist ein Kofaktor bei der g-Carboxylierung der o.g. Gerinnungsfaktoren in der Leber. Neben einer Synthesestörung in der Leber (ca. 50-60% alkoholtoxische Leberschädigung) oder Vit. K-Mangel infolge Malabsorption, gestörter Darmflora oder Verschlussikterus (gestörte Fettresorption infolge Gallemangel) ist die orale Langzeittherapie mit Vit. K-Antagonisten (Antikoagulantien [Cumarine, Marcumar®]) die häufigste Ursache für eine Verminderung der Vit. K abhängigen Gerinnungsfaktoren. Indikation und empfohlener INR-Bereich für die Anwendung von Cumarinen sind in Tabelle 4 dargestellt.

Tabelle 4
Für die meisten Indikationen wird ein INR im Bereich zwischen 2,0 und 3,0 als ausreichend angesehen. Die am häufigsten verwendeten Cumarinderivate (Marcumar®, Coumadin®) besitzen eine lange Halbwertszeit und erreichen ihren therapeutischen Bereich erst nach 24–48h (siehe Tabelle 5), weshalb überbrückend ein (niedermolekulares) Heparin eingesetzt werden muss (sog. bridging). Nach dem Absetzen bzw. Antagonisieren mit Vit. K (Konakion®) ist ihre Wirkung nicht sofort aufgehoben, da erst neue funktionsfähige Gerinnungsfaktoren in der Leber synthetisiert werden müssen. Die Kontrolle der Therapie mit Cumarinderivaten erfolgt durch den INR-Wert.
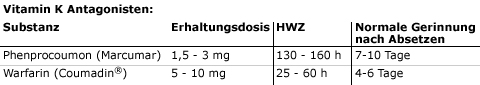
Tabelle 5
3.4 Thrombozytenaggregationshemmer
Um eine funktionsfähige Gerinnung zu gewährleisten, müssen ausreichend funktionstüchtige Thrombozyten vorhanden sein. Eine zu geringe Thrombozytenanzahl (Thrombozytopenie) kann durch eine Bildungsstörung im Knochenmark, gesteigerten peripheren Umsatz oder kombinierte Bildungs- und Abbaustörungen hervorgerufen werden (siehe Tabelle 6).

Tabelle 6
Von besonderer Relevanz sind erworbene Funktionsstörungen der Thrombozyten (Thrombozytopathien), die durch die Einnahme von Thrombozytenaggregationshemmern verursacht werden. Neben der Acetylsalicylsäure (ASS) („low dose“ Aspirin®, ASS 100®) kommen vor allem die Thienopyridinderivate Clopidogrel (Plavix®, Iscover®) und Ticlopidin (Tiklyd®) als Sekundärprophylaxe nach Myokardinfarkt bzw. ischämischen oder thrombotischen zerebrovaskulärem Insult zur Anwendung. Die Wirkung von ASS beruht auf einer irreversiblen Hemmung des Enzyms Cyclooxygenase. Die Folge ist eine irreversible Blockade der Plättchenadhäsion und -aggregation sowie der Sekretion von Plättcheninhaltsstoffen. Die Thienopyridinderivate besitzen im Gegensatz zu ASS eine lange Halbwertszeit und erreichen ihre max. Wirkung erst vier bis sechs Tage nach oraler Gabe. Der Wirkmechanismus beruht auf einer irreversiblen Hemmung der ADP-Rezeptoren an der Thrombozyten-Membranoberfläche. Damit wird die Thrombozytenaggregation, die Sekretion von Plättcheninhaltsstoffen und die Bindung an Fibrinogen irreversibel verhindert. Die irreversible Wirkung von ASS bzw. Thienopyridinen besteht während der gesamten Lebenszeit der Thrombozyten (ca. sieben bis zehn Tage) und kann nur durch eine Neusynthese von funktionstüchtigen Thrombozyten aufgehoben werden.
Die Messung der Blutungszeit besitzt keine zuverlässige Aussagekraft bezüglich der Wirkung von Thrombozytenaggregationshemmern (s.o.). Durch Spezialuntersuchungen (Thrombozytenadhäsion, Thrombozytenaggregation, Freisetzung von Plättchenfaktor 3 (release reaction)) kann die Funktion der Plättchen untersucht werden.
Seitenanfang
4. Therapeutisches Vorgehen
Voraussetzung für die erfolgreiche Behandlung von blutungsgefährdeten Patienten in der Praxis ist die sorgfältige Indikationsstellung und Planung des Eingriffes nach Erhebung einer gründlichen Anamnese und Einschätzung des zu erwartenden Blutungsrisikos. Es ist oftmals ratsam, Rücksprache mit dem behandelnden (Haus-)Arzt zu halten und ggf. zunächst eine bestehende Grunderkrankung zu behandeln. Ein eigenmächtiges Ab- oder Umsetzen der Antikoagulantientherapie sollte in jedem Fall vermieden werden. Eine gewebeschonende Operationsmethode (Trennung der Krone, Teilung der Wurzel), ein möglichst dichter Wundverschluss (adaptierende Wundnaht mit tiefgreifenden Nähten) sowie der Einsatz lokaler Blutstillungsmaßnahmen (Verbandsplatte, Hämostyptika) tragen entscheidend zur Verringerung des postoperativen Nachblutungsrisikos bei. Eine routinemäßige plastische Deckung der Operationswunden ist nicht erforderlich, da dadurch hauptsächlich neue Nachblutungsquellen entstehen und Nachblutungsraten von bis zu 23% festgestellt wurden. Zur Sicherung der lokalen Blutstillung nach einem zahnärztlich-chirurgischen Eingriff hat sich die Applikation lokaler, resorbierbarer Hämostyptika, welche die Bildung des Blutkoagels unterstützen und stabilisieren, als wirksam erwiesen. Im Handel sind zahlreiche Produkte erhältlich. Gelatineschwämme (Gelastypt®), oxidiert regenerierte Zellulose (Tabotamp®) und Kollagenvliese (Lyostypt®) wirken, indem sie durch ihre Oberflächeneigenschaften die intrinsische Gerinnungskaskade aktivieren. Durch lokale Applikation von Thrombin (z.B. in TachoSil®) wird die Fibrinbildung stimuliert. Humanes Fibrinogen, Thrombin und FXIII (fibrinstabilisierender Faktor) entsprechen der Endstrecke der Gerinnungskaskade und sind als Teilkomponenten im Fibrinkleber (Tissucol®, Beriplast®) enthalten. Die postoperative Applikation des Fibrinolysehemmers Tranexamsäure in Form von Aufbisstupfern oder Mundspülungen unterstützt die Hemmung der lokalen Fibrinolyse.
4.1 v. Willebrand-Syndrom (VWS), Hämophilie
Um bei Hämophilie A oder VWS die Faktoraktivität zu erhöhen, wird das Vasopressinanalogon Desmopressin (DDAVP= 1-Deamino-8-D-Arginin-Vasopressin) (Minirin®) verabreicht, das gespeicherten F VIIIC und VWF aus dem Endothel freisetzt. Der Faktorenanstieg in Folge sollte vorher getestet werden. Da sich nach wiederholter Gabe von Desmopressin die Speicher unterschiedlich stark erschöpfen, ist die Verabreichung des Vasopressinanalogons bei einigen Patienten auf wenige Anwendungen begrenzt. Liegen bei der Hämophilie ausgeprägte Faktorenmangelzustände vor, so müssen die Faktoren substituiert werden. Kleinere chirurgische Eingriffe können ab 20-30% Restaktivität, größere ab 50% durchgeführt werden. Formen von VWS, die nicht auf DDAVP ansprechen müssen, ebenfalls mit Faktoren substituiert werden.
Wichtig ist in jedem Falle die strenge Indikationsstellung, da die Gerinnungsfaktoren entweder aus gepooltem Plasma gewonnen werden und somit die Gefahr von Hemm(Anti-)körperbildung bzw. der Übertragung von viralen Erkrankungen (Hepatitis C oder HIV) besteht, oder rekombinant hergestellt werden, was sehr teuer ist.
4.2 Vitamin K-Antagonisten
Vor der Durchführung zahnärztlich-chirurgischer Eingriffe bei oral antikoagulierten Patienten muss das Risiko einer Nachblutung bei Fortführung der Antikoagulation dem Risiko thromboembolischer Komplikationen beim Absetzen entgegengestellt werden. Nach Empfehlungen der Deutschen Gesellschaft für Zahn-, Mund- und Kieferheilkunde (DGZMK) können die Extraktionen eines oder mehrerer Zähne sowie unkomplizierte Osteotomien, unter Berücksichtigung lokaler blutstillender Maßnahmen, bis zu einem INR-Wert von 2,0-3,5 durchgeführt werden, wobei die präoperative INR-Bestimmung am Tag der OP angeraten wird.
Für die Durchführung umfangreicher chirurgischer Sanierungen oder zahnärztlich-chirurgischer Eingriffe mit ungenügender lokaler Blutstillungsmöglichkeit wird ein INR-Wert von 1,6–1,9 empfohlen. Je nachdem wie hoch der INR-Wert des zu behandelnden Patienten eingestellt ist (Marcumarausweis!) braucht (k)eine Umstellung der oralen Antikoagulation auf (niedermolekulares) Heparin erfolgen. Bei Hochrisikopatienten, die ein intensives Monitoring bzw. i.v. Heparinisierung benötigen oder bei Patienten, die nicht in der Lage sind im Falle einer Nachblutung den Arzt aufzusuchen, ist eine stationäre Behandlung indiziert.
Seitenanfang
4.3 Thrombozytenaggregationshemmer
Das Nachblutungsrisiko nach zahnärztlich-chirurgischen Eingriffen ist unter der Einnahme von ASS 100 als gering einzustufen und somit ein Absetzen von ASS 100 unter Berücksichtigung des Nutzen-Risiko-Verhältnisses nicht zu rechtfertigen. Bestehen jedoch zusätzlich qualitative oder quantitative Thrombozytenanomalien, angeborene oder erworbene Koagulopathien, chronische Nieren- oder Leberfunktionseinschränkungen oder Alkoholismus, so ist das Blutungsrisiko zusätzlich erhöht und ein Absetzen von ASS (nach Rücksprache mit dem behandelnden Arzt) sinnvoll. Ist kein Absetzen möglich, sollte der Patient stationär behandelt werden. Obwohl bis jetzt keine Untersuchungsergebnisse über eine erhöhte Nachblutungsgefahr nach dentoalveolären Eingriffen unter der Therapie von Clopidogrel (Plavix®, Iscover®) und Ticlopidin (Tiklyd®) vorliegen, wird ein Absetzen sieben bis zehn Tage vor dem zahnärztlich-chirurgischen Eingriff empfohlen.
5. Postoperative Nachsorge
Bei gerinnungsgehemmten Patienten empfiehlt es sich, innerhalb der ersten Woche eine engmaschige postoperative Wundkontrolle durchzuführen. Generell sollte der Operateur für den Patienten erreichbar sein. Im Rahmen der postoperativen medikamentösen Behandlung ist zu beachten, dass viele schmerzstillende Medikamente Acetylsalizylsäure beinhalten und somit ihrerseits das Nachblutungsrisiko erhöhen können. Auch andere nicht-steroidale Antiphlogistika (NSAID, non steroidal antiinflammatory drugs) und Antibiotika, aber auch Phytotherapeutika wie z.B. Ginko, können die Blutgerinnung negativ beeinflussen. Die Nahtentfernung sollte nach weitgehendem Abschluss der Wundheilung ca. acht bis zehn Tage postoperativ erfolgen.
6. Zusammenfassung
Um Blutungskomplikationen bei der ambulanten zahnärztlich-chirurgischen Behandlung von Patienten mit Gerinnungsstörungen zu vermeiden, ist eine strenge Indikationsstellung, eine sorgfältige Therapieplanung unter Einbeziehung der behandelnden (Haus-)Ärzte, eine sorgfältige lokale Blutstillung sowie eine engmaschige postoperative Nachbetreuung erforderlich. Eine perioperative Verwendung von Analgetika, welche die Thrombozytenaggregation hemmen, sollte vermieden werden.