Oralchirurgie 24.05.2012
Periimplantäre Entzündungen
share
Risikofaktoren, Diagnostik, Prävention und Therapiemöglichkeiten
Mit der zunehmenden Zahl an dentalen Implantationen steigt auch die Prävalenz der periimplantären Entzündungen. Die Häufigkeit einer Mukositis wird in der Literatur mit Werten bis zu 80 Prozent und die einer Periimplantitis zwischen 11,3 und 47,1 Prozent angegeben.1,2 Dabei existiert noch keine offizielle Leitlinie bzw. gültiges Protokoll zum Vorgehen gegen diese Entzündungsformen.3,4 Die Höhe dieser Werte verdeutlicht die Relevanz der Diagnostik, Prävention und Therapieansätze bezüglich dieser Erkrankungen.
Der Sammelbegriff der periimplantären Entzündungen lässt sich in zwei Krankheitsformen gliedern, die Mukositis und die Periimplantitis. Die Mukositis ist definiert als reversible Entzündung des periimplantären Weichgewebes eines in Funktion stehenden, osseointegrierten Implantates. Es liegt bei dieser Form der Entzündung noch kein pathologischer Knochenabbau vor. Sie geht nicht obligat in eine Periimplantitis über. Bei der Periimplantitis handelt es sich dagegen um einen Entzündungsprozess der periimplantären Gewebe mit Knochenverlust bei osseointegrierten Implantaten in Funktion. Wichtig ist dabei die Kennzeichnung, dass die Implantate zum Zeitpunkt der Freilegung und der funktionellen Belastung alle klinischen Anzeichen eines Erfolges aufwiesen.
Grundsätzlich lassen sich Komplikationen, die zum Implantatverlust führen können, in primäre (während der Einheilphase) und sekundäre (nach der Osseointegration) Komplikationen einteilen. Diese können biologischer (infektiös-bakterieller) oder mechanischer (funktioneller) Natur sein. Die periimplantären Entzündungen zählen damit zu den sekundären Komplikationen der Implantologie.
Periimplantäre Strukturen
Vergleicht man die periimplantären Weichgewebe mit den parodontalen Strukturen natürlicher Zähne, besteht nur bedingt Ähnlichkeit. Die periimplantäre Mukosa enthält mehr kollagene Fasern in einer anderen Strukturierung im Vergleich zur Gingiva. Das implantatnahe Bindegewebe ist gefäßärmer als entsprechende parodontale Strukturen und weist dementsprechend eine schlechtere Abwehr gegenüber exogenen Irritationen auf.5,6 Bei einer entzündlichen Zerstörung dieser Kontaktstelle kann eine bakterielle Kontamination direkt in Richtung des Knochens vordringen und zu einer raschen Zerstörung führen.7
Risikofaktoren
Risikofaktoren, die die Entstehung einer Periimplantitis beeinflussen können, sind zusammengefasst:
– Mangelnde Mundhygiene und Compliance
– Parodontitis-Hintergrund
– Rauchen
– Lokale präimplantologische Pathologien
– Suprakonstruktion
– Systemische Erkrankungen
– Bereits stattgefundener implantologischer Misserfolg
– Breite bzw. Vorhandensein der befestigten Mukosa
Die Mundhygiene gilt als wichtigster Präventionsfaktor zur Vermeidung periimplantärer Erkrankungen. Sie ist sehr eng verknüpft mit der An- bzw. Abwesenheit dieser Erkrankungsform.8,9 Ohne regelmäßige Kontrollen ist eine periimplantäre Entzündung eine häufige klinische Erscheinungsform.10–12 Die Compliance des Patienten, d.h. die Kooperation vor, während und nach der Behandlung (besonders in Bezug auf einer effektiven häuslichen Mundhygiene und die Wahrnehmung von Recallterminen und PZR) muss vor der Implantation evaluiert und festgehalten werden. Wie in der Parodontologie spielt eine bakterielle Besiedelung die größte Rolle in Bezug auf eine periimplantäre Entzündung.13–16 In zahlreichen Studien wurde gezeigt, dass die entzündliche periimplantäre Flora der einer aggressiv verlaufenden Parodontitis gleicht.14,15,17 Es ist bewiesen, dass parodontal-pathogene Keime bei Parodontitispatienten übertragen werden können. Dabei kann die vorhandene Restbezahnung als Reservoir für die mikrobielle Besiedelung der Implantate dienen. Diese Residualflora besitzt dabei den größten Einfluss auf die Mikroflora der gesetzten Implantate. Nach der Extraktion aller Zähne ist ein deutlicher Verlust an pathogenen Bakterien nachzuweisen.15,18
Eine chronische Parodontitis stellt aber keineswegs eine absolute Kontraindikation für eine erfolgreiche Implantation dar. Es ist aber essenziell, die aktive Parodontitis vorher in den Griff zu bekommen, d.h. wirkungsvoll zu behandeln, einschließlich einer Aufklärung des Patienten.14,19 Diese Aufklärung beinhaltet, dass der Patient wissen muss, dass nicht die gleichen Erfolgsaussichten herrschen wie bei einem gesunden Patienten (verringerte Erfolgsaussicht). Dazu zählen gleichermaßen die Bewusstmachung der Notwendigkeit einer perfekten häuslichen Mundhygiene, engmaschiger Recalls und regelmäßiger professioneller Zahnreinigungen (PZR).20–22 Patienten mit einer durchgemachten Parodontitis haben eine bis zu 4,7-mal erhöhte Rate, an einer Periimplantitis zu erkranken. Dabei besteht eine synergistische Wirkung mit Tabakkonsum. Das Rauchen gilt in der Parodontologie als Hauptrisikofaktor für parodontale Erkrankungen und Wundheilungsstörungen. Raucher haben eine bis zu 4,6-mal erhöhte Rate, an einer Periimplantitis zu erkranken.10–12,23 Starkes Rauchen kann zu einer Kontraindikation werden.
Bei aggressiven Parodontitiden ist dagegen bei einer geplanten implantologischen Versorgung Vorsicht geboten und eine sehr strenge Indikationsstellung bzw. Kontraindikation angezeigt.19 Die Möglichkeit einer retrograden Periimplantitis wurde ebenfalls nachgewiesen. Dabei kann die Entzündung von Nachbarzähnen mit periapikalen Infektionen oder aber von vorhandenem bzw. verbliebenem Narben- und Granulationsgewebe ausgehen. Es sollte, besonders bei einer verkürzten Dauer zwischen Extraktion eines entzündeten Zahnes und dessen Ersatz mit einem Implantat, auf eine exakte und vollständige Kürettage der Alveole Wert gelegt werden. Ebenso kann die Inzidenz durch eine Zunahme des zeitlichen Abstandes zwischen der endodontischen Behandlung eines beherdeten Zahnes und der Implantatinsertion in unmittelbarer Nachbarschaft reduziert werden.24 Größten Wert ist auf die Hygienefähigkeit der Suprakonstruktion zu legen, ebenso auf den spalt- und spannungsfreien Sitz und die richtige Okklusion. Bezüglich der Abutmentverbindungen zeigen sich Innenverbindungen vorteilhafter als Außenverbindungen. Bei Innenverbindungen ist die Konusverbindung durch Presspassung und nach innen verlagertem vertikalen Mikrospalt (Microgap) am besten.25 Verbliebene Zementreste im Sulkus können ebenfalls entzündliche Reaktionen hervorrufen („Zementitis“). Das Legen eines Fadens vor Zementierung kann dies minimieren. Auf eine exakte Säuberung nach definitiver Zementierung ist zu achten. Eine Möglichkeit so eine zementinduzierte Entzündung zu umgehen, wäre der Einsatz provisorischer, wasserlöslicher Zemente oder die Verwendung verschraubter Prothetik.
Zudem erhöhen bestimmte systemische Faktoren die Empfänglichkeit für die Entwicklung einer periimplantären Erkrankung z.B. Diabetes, hormonelle Störungen, Immunsuppressionen oder bestimmte Medikamente. Ein bereits stattgefundener implantologischer Misserfolg kann als Prädiktor für einen weiteren Misserfolg werden, sofern keine eliminierbare Ursache gefunden werden kann.26 Eine genügende Breite der befestigten Mukosa um ein Implantat herum (>2mm) sollte angestrebt werden.27–30 Fehlt diese, so ist die Anfälligkeit der periimplantären Region gegenüber plaqueinduzierter Gewebszerstörung erhöht. Die Schaffung befestigter Gingiva sollte spätestens bei der Freilegung des Implantats erfolgen.
Prävention
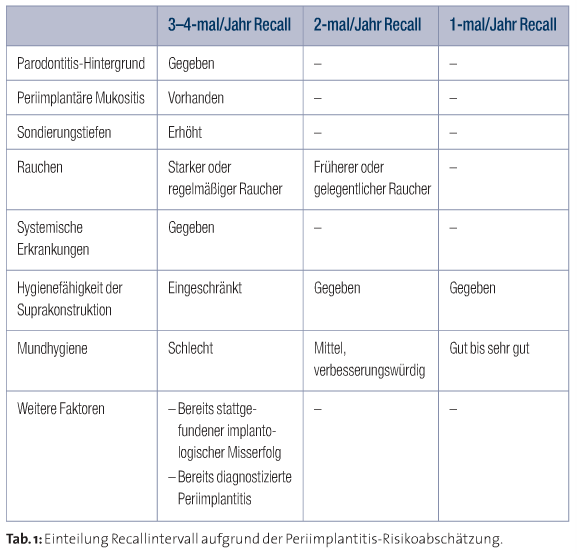
Der wichtigste Faktor in Bezug auf periimplantäre Entzündungen ist die Prävention. Die Prävention beginnt bereits bei der Implantatplanung: Rauchentwöhnung, Socket Preservation, Parodontitistherapie, Compliance des Patienten in Bezug auf die häusliche Mundhygiene und die spätere Wahrnehmung der Recalltermine, regelmäßige professionelle Zahnreinigungen, Gingivaverdickungen usw. Die Applikation von 1%igem CHX-Gel vor dem Einsetzen des Abutments auf das Implantat scheint eine effektive Methode zu sein, in der frühen Phase eine bakterielle Kolonisation des Implantates zu reduzieren und einer periimplantären Entzündung entgegenzuwirken.33 Nur durch die Einbindung des Patienten in einen regelmäßigen Recall ist die frühzeitige Erkennung einer periimplantären Entzündung und ggf. Intervention gewährleistet. Studien belegen das häufige Vorkommen periimplantärer Entzündungen nach Jahren Tragezeit ohne systematische Erhaltungstherapie.4,10 Über die Frage, wie oft ein solcher Recall stattfinden sollte, stehen in der Literatur keine eindeutigen Aussagen.31 Analog der Parodontitis-Risikoabschätzung32 verwenden wir anhand der oben genannten Risikofaktoren eine eigene Periimplantitis-Risikoabschätzung. Hiernach richtet sich das Recallintervall (Tab. 1). Nach unserem Wissen existiert derzeit noch keine Richtlinie bezüglich einer solchen Intervallfestlegung.
„Stunde-Null“-Parameter
Um Vergleiche zwischen den im Recall gemessenen Werten (Knochenabbau, Sondierungstiefen) und den Ausgangswerten anstellen zu können, sind verschiedene Parameter nach Implantatinsertion bzw. prothetischer Versorgung festzuhalten.
Sinnvolle Zeitintervalle für die Anfertigung von Röntgenbildern sind:
– präimplantologische Röntgendiagnostik,
– postimplantologische Röntgenkontrolle,
– Röntgen-Kontrolle nach Eingliederung der Prothetik („Stunde-Null“-Referenz),
– Röntgenkontrolle ein Jahr nach Eingliederung der Prothetik, danach im Rahmen der diagnostischen Röntgennotwendigkeit bei Jahreskontrollen,
– bei pathologischen Befunden im Rahmen des Recalls.
Wobei die wichtigste Aufnahme nach der prothetischen Versorgung stattfindet („Stunde-Null“-Referenz). Sie dient erstens zur Überprüfung der Prothetik (richtiger Sitz, Zementreste) und zweitens als Referenzaufnahme zum Vergleich mit allen späteren angefertigten Röntgenbildern. Zusätzlich sollten periimplantäre Sondierungstiefen als Referenzwerte festgehalten werden.
Diagnostik und Recall
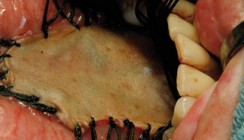
Patienten mit Implantaten sollten bei jedem Recall einen standardisierten diagnostischen Ablauf (Tab. 2) durchlaufen. Dieser Ablauf wird bei jedem Termin durchgeführt und dokumentiert. Dadurch wird eine genaue Dokumentation ermöglicht und Verlaufsbeobachtungen erleichtert. Unbestritten ist der regelmäßige, implantologische Recall ein wesentlicher Bestandteil der gesamten Therapie. Durch den meist stummen Verlauf einer beginnenden periimplantären Erkrankung ist diese oft nicht vom Patienten selbst zu erkennen (Abb. 1). Nicht diagnostiziert und damit unbehandelt führt die Periimplantitis über kurz oder lang definitiv zum Verlust der Osseointegration und damit zum Verlust des Implantates (Abb. 2 und 3). Da die Mundhygiene die Schlüsselstellung in der Prävention oraler und periimplantärer Erkrankungen einnimmt, gehören professionelle Zahnreinigungen in regelmäßigem Abstand zum Pflichtprogramm der Patienten. Hierbei werden die Patienten, neben einer gründlichen Tiefenreinigung und der Erhebung der Indizes, auch bezüglich der häuslichen oralen Hygiene ständig reinstruiert und remotiviert. Eine Aufklärung des Patienten vor Implantation über die Wichtigkeit dieser Maßnahmen ist unabdingbar. Die Inspektion der periimplantären Weichgewebe kann direkt Aufschluss über mögliche Entzündungen geben. Rötungen oder Schwellungen deuten auf bereits entzündetes Gewebe hin, ebenso Spontanblutungen oder gar Fistelbildungen aufgrund chronischer Entzündungsvorgänge (Abb. 4). Liegen pathologische Veränderungen vor, erfolgt eine Röntgenaufnahme zur Beurteilung der knöchernen Strukturen. Typisch für den entzündlichen periimplantären Knochenabbau ist der schüsselförmige Knochenverlust, der sich klinisch in einem Krater manifestiert, in welchem das Implantat steht.

Anschließend wird jedes Implantat auf Beweglichkeit überprüft. Ist eine Beweglichkeit vorhanden, muss die Ursache abgeklärt werden. Eine Röntgenkontrolle ist in diesem Fall sehr hilfreich. Liegt ein vollständiger Verlust der Osseointegration oder eine Fraktur des Implantates vor, bleibt nur die Explantation als therapeutische Maßnahme. Besteht dagegen ein Problem der Suprastruktur, sollte dieses behoben werden. Der nächste Schritt beinhaltet die periimplantäre Taschensondierung, die an sechs Stellen pro Implantat erfolgen sollte. Trotz Kontroversen bezüglich einer möglichen Schädigung durch das Sondieren, ist diese Maßnahme für ein korrektes diagnostisches Vorgehen unentbehrlich. Ein vorsichtiges Sondieren (mit Kunststoffsonde unter leichtem Druck [0,15N]) führt nachgewiesenermaßen zu keiner iatrogenen Schädigung des Implantates oder der periimplantären Gewebe.34,35 Beim Sondieren ist zunächst auf Entzündungszeichen zu achten, speziell auf Blutungen an den Sondierungsstellen (Abb. 5 und 6). Das Fehlen einer Blutung kann als zuverlässiger Indikator für das Fehlen einer Entzündung angesehen werden.36,37 Ein weiteres, für das Implantat dramatischeres Entzündungszeichen wäre ein eventueller Pusaustritt. Pus ist immer ein Zeichen für eine Infektion und deutet bereits auf eine knöcherne Beteiligung der Entzündung hin. Die Interpretation von Sondierungstiefen an Implantaten ist recht spezifisch und variiert je nach Zugangsmöglichkeiten der Sonde. Je nach Implantathersteller können auch verschiedene Sondierungstiefen als „normal“ angesehen werden. Hier variieren die Abstände zwischen Implantatschulter und angrenzendem Knochen. Sondierungstiefen über sechs Millimeter deuten jedoch auf eine Periimplantitis hin. Die gemessenen Taschentiefen sind allerdings vorsichtig zu interpretieren.38
Therapiemöglichkeiten
Zunächst muss festgehalten werden, dass es keine Therapie gibt, die ein sicheres und voraussagbares Ergebnis liefert. Es existieren viele Erfolg versprechende Ansätze, die hier kurz dargestellt werden. Ziele der Therapie sind die Beseitigung der Entzündungszeichen, das Aufhalten eines Fortschreitens der Entzündung sowie der Vorbeugung eines Rezidivs. Sinnvoll erscheint eine Therapie, basierend auf der Schwere und dem Ausmaß der Erkrankung, die ein kumulatives Vorgehen vorgibt (vgl. Cumulative Interceptive Supportive Therapy, CIST39,40). Das CIST-Protokoll beinhaltet vier Stufen, die den kumulativen Einsatz von mechanischer Behandlung, lokaler Desinfektion, systemischer Antibiotikagabe und chirurgischer Eröffnung beinhalten. Beim Vorliegen von moderaten Entzündungszeichen wie Blutungen nach Sondierung ohne erhöhte Sondierungstiefen, kann eine geschlossene Kürettage (mit Titan- oder Kunststoffküretten) nachgewiesenermaßen effektiv einer Mukositis entgegenwirken.41 Stahl- oder Ultraschallinstrumente können die Titanoberfläche zerkratzen und fördern so weitere Plaqueakkumulation. Verbesserungen des Ergebnisses lassen sich durch zusätzliche Chlorhexidin-Spülungen (0,12%) oder sanftes Einmassieren von Chlorhexidin-Gel (1%) mit einem Bürstchen erreichen.41,42 Dabei reicht eine lokal angewandte CHX-Applikation vollkommen aus. Behandlungen im Sinne einer „Full-Mouth-Desinfection“ erzeugen kein signifikant besseres Ergebnis als eine lokale Behandlung.43 Bei Sondierungstiefen über sechs Millimeter mit oder ohne Suppuration folgt dann eine zusätzliche Antibiose. Die entstandene periimplantäre Tasche repräsentiert eine Nische, die mit parodontal-pathologischen Keimen besiedelt wird.44 Das Keimspektrum einer manifestierten Periimplantitis ähnelt dem einer aggressiv verlaufenden Parodontitis, also vorwiegend anaerobe gram-negative Bakterien. Zurzeit existiert kein standardisiertes Behandlungsprotokoll bezüglich einer adjuvanten Antibiotikatherapie.45 Vorgeschlagen wird die Kombination von Amoxicillin (375mg x 3) und Metronidazol (250mg x 3) über zehn Tage. Eine mikrobiologische Untersuchung ist vor dem Einsatz von Antibiotika zu erwägen, um so die relativ sichere Möglichkeit zu haben, eine gezielte Antibiose durchführen zu können. Die Antibiose kann aber auch lokal appliziert werden. Wie in der Parodontologie ist eine Antibiose aber nur in Verbindung mit einer mechanisch-instrumentellen Therapie Erfolg versprechend.
Ab einem gewissen Stadium (d.h. bei weit fortgeschrittenem Knochenabbau und Sondierungstiefen über sechs Millimeter) zeigt ein offenes Vorgehen zum Defekt und zur Implantatoberfläche klinische und mikrobiologische Vorteile.46,47 Für eine zusätzliche lokale Dekontamination der besiedelten Implantatoberflächen werden in der Literatur verschiedene Möglichkeiten aufgezeigt. Möglichkeiten zur Dekontamination der Implantatoberfläche sind:
– Pulver-Wasser-Strahlgeräte (auch in Verbindung mit Zitronensäure, CHX-Spüllösungen, Wasserstoffperoxid oder Phosphorsäure),
– CO2-, Dioden- oder Er:YAG-Laser,
– Die antimikrobielle Photodynamische Therapie (aPDT).
Viele Methoden zeigten sich in Studien erfolgreich, noch hat sich aber keine Therapie als Mittel der Wahl durchgesetzt.46 Die Wirksamkeit von verschiedenen Desinfektionsmöglichkeiten wurde erwiesen, die Studien lassen sich aber schlecht vergleichen und es fehlen Langzeitergebnisse.48 Weitere Studien untersuchten Laser auf seinen Nutzen bei der Periimplantitistherapie. Dabei zeigen diese durchaus antibakterielles Potenzial auf der Implantatoberfläche. Der Er:YAG-Laser zeigt ein höheres Potenzial im Vergleich zu anderen Laserarten, jedoch keinen überlegenen Nutzen im Vergleich zum konventionellen Débridement.49,50 Bei der antimikrobiellen Photodynamischen Therapie wird ein spezieller Farbstoff (Toloidinblau) durch Lichtenergie bestimmter Wellenlänge (690nm) angeregt, dadurch werden Sauerstoffmoleküle zu Singulett-Sauerstoff aktiviert. Dieser Singulett-Sauerstoff ist in der Lage bakterielle Zellmembranen zu zerstören. Studien belegen die antibakterielle Wirkung und den damit zusätzlichen Nutzen gegenüber der alleinigen mechanischen Wirkung. Zur endgültigen Beurteilung dieser Therapie im Vergleich zum konventionellen Débridement bedarf es weiterer Studien.
Die Notwendigkeit einer zusätzlichen Reduktion oder Elimination von Plaqueretentionsstellen ist auch vereinzelt dokumentiert. Dies trifft vor allem zu, wenn die Mikrostrukur des Implantats betroffen ist und sichtbar freiliegt. Eine Glättung der rauen Oberfläche mit Bohrer oder Fräsen samt anschließender Politur (Implantatplastik) ist aber nur im nicht sichtbaren Bereich (Seitenzahngebiet, unter Coverdenture-Prothesen) indiziert. Ein vorteiliger Effekt dieser Option wurde allerdings noch nicht dokumentiert.
In manchen Fällen kann eine Mukogingivalchirurgie zur Verbreiterung der keratinisierten periimplantären Mukosa oder zur Reduktion der Tiefe einer periimplantären Tasche angezeigt sein. Diese Maßnahmen sind aber selbstverständlich erst nach Rückgang der Entzündung durchzuführen. Ohne eine genügende Breite an keratinisierter Mukosa kann es zu einem späteren Zeitpunkt zu einem signifikant höheren Knochenverlust kommen.51 Aktuell ist die Diskussion einer möglichen gesteuerten Knochenregeneration um ein Implantat herum als posttherapeutische Maßnahme, im Sinne einer Reosseointegration. Es sollte aber deutlich gesagt sein, dass diese Techniken nicht auf die Heilung einer Periimplantitis abzielen, sondern nur auf den Versuch, den ossären Defekt aufzufüllen. Es zeigen sich zwar bereits einige gute Resultate in Hinblick auf einer Reduktion der Taschentiefen, hier sollten aber weitere Studien abgewartet werden.46,52,53
Ab einem gewissen Verlust an Knochen (> 2/3 der Implantatlänge) oder bei weiterem unkontrollierten Fortschreiten der Entzündung ist die Explantation als einziger Ausweg in Betracht zu ziehen.
Fazit
Die Mukositis als Vorstufe einer Periimplantitis kann durch geeignete Prophylaxemaßnahmen vermieden werden. Somit könnte die schwierige und nicht vorhersagbare Behandlung einer Periimplantitis entfallen. Derzeit existiert noch keine überlegene Therapieform bezüglich einer manifesten Periimplantitis. Welche zusätzliche Therapie zum konventionellen mechanischen Débridement (mit Antiseptika und eventuell Antibiotika) genutzt wird, bleibt dem einzelnen Behandler selbst überlassen. Zur endgültigen Entscheidung müssen weitere Studien abgewartet werden.
Eine ausführliche Literaturliste finden Sie hier.