Prophylaxe 10.11.2014
Biofilm-Management: Folgen unzureichender Therapie und Prophylaxe
share
Das Thema Biofilm-Management gewinnt zunehmend an Bedeutung und stellt den Behandler täglich vor Herausforderungen. Der dentale Biofilm ist in meinen Augen das zentrale Problem beim Management von parodontalen, enossalen und dentalen Strukturen. Aus diesem Grund ist es zwingend erforderlich, neben einer systematischen Therapie dem komplizierten Gefüge des Biofilms auf den Grund zu gehen.
Als ausschlaggebender Faktor für die Entstehung von Parodontitiden gilt, neben einer genetischen Disposition, das Vorliegen parodontopathogener Keime. Dabei scheint nicht nur das Vorliegen solcher Keime entscheidend zu sein, sondern deren organisierte Struktur im Biofilm. Somit ist die hohe Resistenz gegen lokale Therapiemaßnahmen zu erklären.
Was ist ein Biofilm?
Unter Biofilmen versteht man die Zusammensetzung von Bakterien, die durch Co-Aggregationsmechanismen als sogenannte Bakterienfamilien agieren und sich gegenseitig stabilisieren (Simmons 1989; Marsh und Bradshaw 1995; Ligtenberg et al. 2007). Biofilme besiedeln vorzugsweise feuchte Oberflächen (Passerini et al. 1992; Giaouris et al. 2005); nicht nur in der Mundhöhle, auch im täglichen Leben stellen sie uns vor Probleme. Ein Beispiel hierfür ist die Besiedlung von Abwasserrohren. Um das Gefüge Biofilm und die Organisation besser verstehen zu können, kann man sich ein Beispiel aus der Geschichte heranziehen: So bildeten die Feldherren im Römischen Reich zum besseren Schutz vor Angreifern sogenannte Schildkrötenformationen. Bei dieser Formation marschierten die Legionäre geschlossen und schützten sich mit ihren großen Schilden vor Pfeilbeschuss und geworfenen Steinen. Auch Mikroorganismen bilden einen gemeinsamen Schutzwall gegen giftige Substanzen, die zu ihrer Elimination führen könnten. Zudem dient der Zusammenschluss dem Nährstoffaustausch, der Weitergabe von Genen und somit einer erhöhten Anpassungsfähigkeit an Veränderungen des umgebenden Milieus.
Bildung des Biofilms
Die Biofilmentstehung lässt sich in drei Phasen unterteilen:
- Induktionsphase
- Akkumulationsphase
- Existenzphase.
Zu Beginn der Induktionsphase bildet sich eine organische Schicht; dadurch können sich die Mikroorganismen besser an der Oberfläche anheften. Zu Beginn haften meist Actinomyceten mithilfe von Fimbrien und Pili an der Oberfläche der Zähne. Diese organische Schicht wird in der Akkumulationsphase von Keimen besiedelt, wobei zunächst aerobe und später anaerobe Keime vorherrschen. Diese formierte organische Matrix dient als Nährstoffzufuhr. Die Matrix, deren Hauptbestandteil Polysaccharide sind, schützt vor äußeren Einflüssen und gewährleistet durch Bildung spezieller Wasserkanäle die Substratzufuhr und den Abtransport von Giftstoffen (Marsh und Bradshaw 1995). Entscheidend für die Stabilität des Biofilms ist die Bildung von mehreren Kolonien, die unabhängig voneinander koexistieren und agieren können. Die Existenzphase ist erreicht, wenn ein Gleichgewicht zwischen Abbau und Zuwachs des Biofilms entstanden ist. Im Biofilm kommt es zum Austausch genetischer Informationen, dem sogenannten „Quorum sensing“, einem interzellulären Kommunikationssystem (Suntharalingam und Cvitkovitch 2005; Wang und Kuramitsu 2005). Der genaue Mechanismus ist bisher noch nicht vollständig geklärt. Die Bakterien im Biofilm sind in der Lage, Resistenzgene gegen Antibiotika zu bilden. Diese hochkomplex organisierten Biofilmstrukturen zeigen eine 1.000- bis 1.500-fach höhere Resistenz gegenüber Antibiotika.
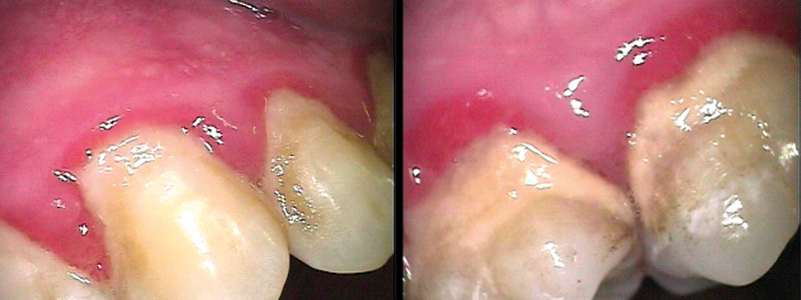
Abb. 1 und 2 (Intraoralkamera-Aufnahmen): Klinisches Bild des supragingivalen Biofilms mit Entzündungszeichen des umliegenden Gewebes.
Die Struktur der oralen Plaque und die Bakterien im oralen Biofilm
Supragingivale Plaque unterscheidet sich zudem gravierend von der subgingivalen Plaque. Im supragingivalen Biofilm leben die Bakterien organisiert und können den Biofilm über die Mundhöhle verlassen, haften direkt an der Zahnoberfläche an und verlieren durch die richtigen Mundhygienemaßnahmen ihre Wirksamkeit. Der subgingivale Biofilm kann leider nicht durch einfache prophylaktische Mundhygienemaßnahmen unschädlich gemacht werden. In tiefen parodontalen Taschen mit einem hohen Attachementverlust findet man vor allem hochpathogene gramnegative anaerobe Keime mit hohem destruktivem Potenzial an Hart- und Weichgewebe wie vom Typ Aggregatibacter actinomycetemcomitans (A.a.c), Porphyromonas gingivalis (P.g) und Bacteroides forsythus (B.f). Bei einer Parodontitis können sich mehr als zwei Billionen Keime in der Mundhöhle befinden. Es kommt zu einem bakteriologischen Ungleichgewicht und infolgedessen zur chronischen lokalen oder generalisierten Infektion.
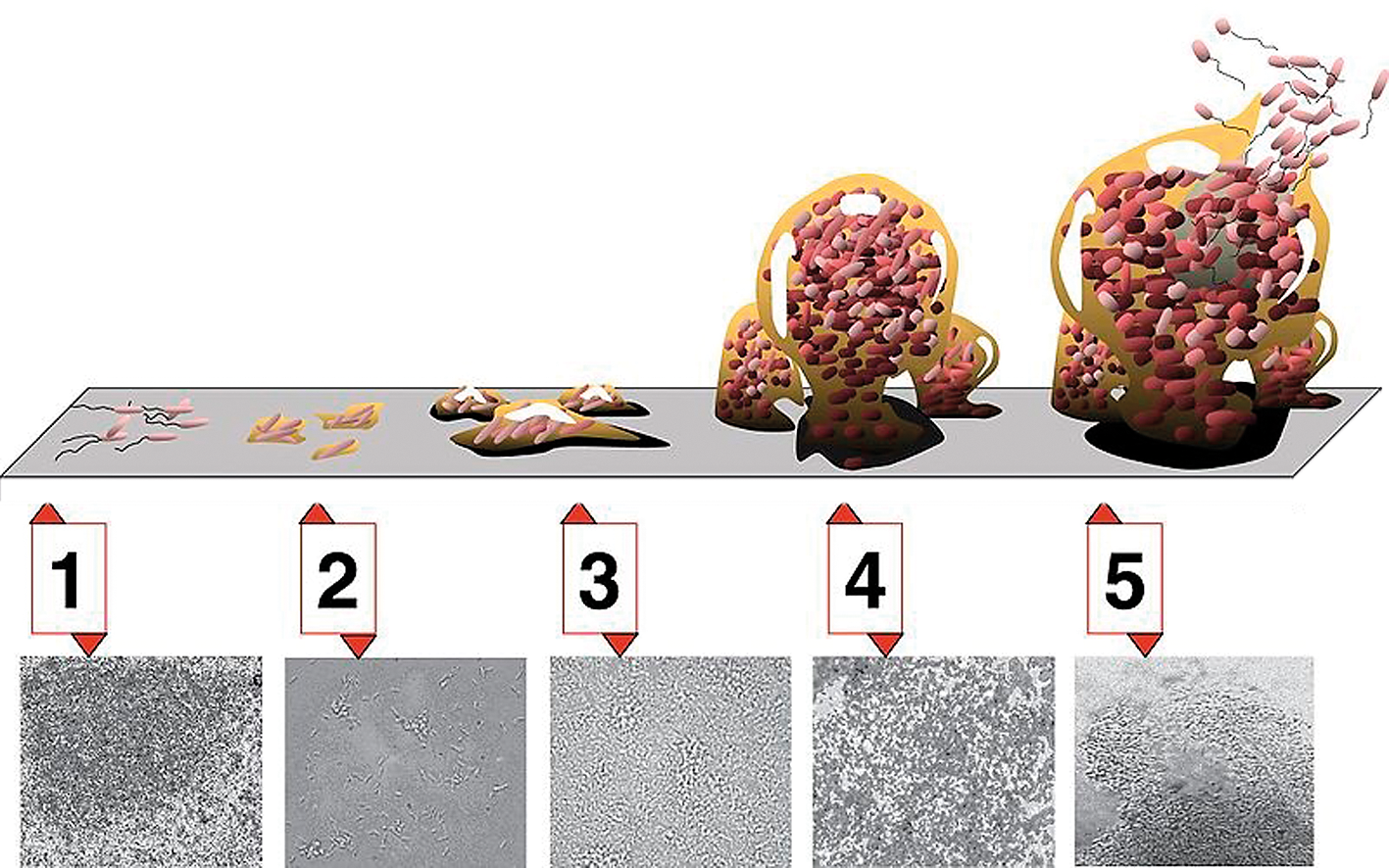
Abb. 3: 5 stages of biofilm development. Stage 1, initial attachment; stage 2, irreversible attachment; stage 3, maturation I; stage 4, maturation II; stage 5, dispersion. Each stage of development in the diagram is paired with a photomicrograph of a developing Pseudomonas aeruginosa biofilm. All photomicrographs are shown to same scale. – (Looking for Chinks in the Armor of Bacterial Biofilms, Monroe D., PLOS Biology, Vol. 5, No. 11, e307 doi: 10.1371/journal.pbio.0050307 by D. Davis.
Welche Herausforderungen ergeben sich für die heutige Parodontitistherapie? State of the Art ist die Full Mouth Desinfection-Methode, bei der vorrangiges Ziel ist, den oralen Biofilm zu zerstören. Dies kann nur mechanisch in Kombination mit Desinfektion erreicht werden. Wie bereits bekannt, ist der Sauerstoffgehalt bei Sondierungstiefen von > 4 mm geringer und bildet somit ideale Bedingungen für die Vermehrung parodontopathogener Keime. In Nischen ist es parodontopathogenen Keimen sogar möglich, zehn bis 14 Tage bis zur nächsten Gewebedesquamation zu überleben. Eine systematische Parodontitistherapie mit strukturiertem Recall, die sogenannte unterstützende Parodontitistherapie (UPT), ist unerlässlich. Man darf nicht annehmen, dass die Erkrankung im Gewebe und die lokale Entzündung, die durch die im Biofilm angesiedelten parodontopathogenen Keime und zumeist innerhalb von vielen Jahren progredient entstanden sind, durch eine einmalige Therapie zu einem bestimmten Zeitpunkt zu beseitigen ist. Die viermal jährlich durchgeführte konzeptionslose professionelle Zahnreinigung erwies sich, laut Beck et al. (2008; PAV), als Misserfolg, da sich nach jeder Therapiemaßnahme der Biofilm in den parodontalen Taschen wieder etablieren konnte. Im Zuge der Möglichkeiten, fehlende Zähne durch Implantate zu ersetzen, werden mehr und mehr parodontal geschädigte Zähne eher extrahiert statt therapiert. Fürst et al. (2010) und viele andere Wissenschaftler bestätigen, dass der parodontale Biofilm in der Mündhöhle überlebt und mit großer Wahrscheinlichkeit die osseointegrierten Implantate spätestens bei der Verbindung mit dem Abutment infizieren kann. Dies zeigt umso mehr, dass eine systematisch aufgebaute Parodontitis- bzw. Periimplantitistherapie in den Fokus der modernen Zahnmedizin gerückt ist.
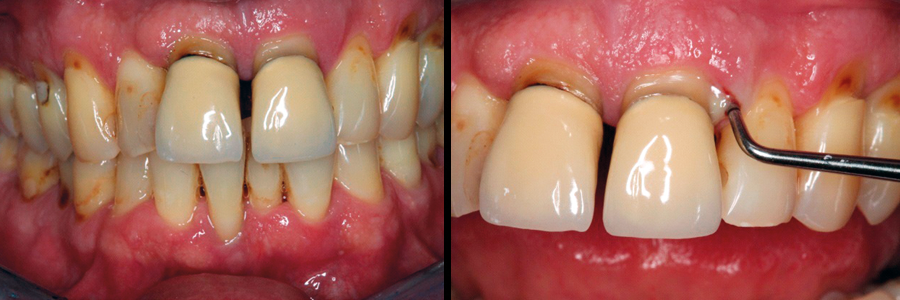
Abb. 4: Klinisches Bild eines parodontal und kariogen geschädigten Gebisses mit deutlich sichtbarem Attachmentverlust. – Abb. 5: Klinisches Bild mit pathologischer Sondierungstiefe und Pusaustritt aus der parodontalen Tasche.
Fazit
Meiner Ansicht nach ist ein Umdenken in Bezug auf den Therapiezeitpunkt bei der Behandlung einer Parodontitis in der täglichen Praxis notwendig. Eine umfassende Untersuchung des Parodonts zu Beginn jeder eingehenden Untersuchung, eine Bestimmung des Kariesrisikos, frühzeitige mikrobiologische Tests und Markerkeimanalysen können zu einer frühen Eliminierung der pathogenen Flora führen. Falls die Parodontitis bzw. Periimplantitis bereits etabliert ist, kann nur ein striktes Behandlungskonzept zum Erfolg führen. Dieses Konzept gliedert sich in eine Hygiene-, Therapie- und Nachsorgephase. Die Nachsorgephase sollte den Patienten idealerweise ein Leben lang begleiten, um ein erneutes Aufkommen der Erkrankung im Keim ersticken zu können.










