Implantologie 20.04.2016
Diagnostik und Planung in der Implantologie
share
In der Debatte um das richtige Maß des Planungsaufwandes in der Implantologie stehen Faktoren wie die Kosten und Strahlenbelastung für den Patienten dem Argument der höheren Positionierungssicherheit bei geführten Implantationen gegenüber. Der Autor erläutert die Vorteile der aus seiner Sicht lohnenden Investition in hochwertige und aktuelle Diagnostiktechnologie.
In einem aktuell erschienenen Editorial beschreibt Fred Bergmann, Präsident der DGOI, die aktuellen Wünsche der Patienten: „Sie fragen nach kürzeren Behandlungszeiten, weniger belastenden, möglichst schmerzfreien Eingriffen und nach Konzepten mit einer reduzierten Implantatzahl.“ Leider haben aber Zahnärzte, die sich im Vorfeld der implantologischen Behandlung hinsichtlich der Indikation (Patientenauswahl), Planung und Diagnostik viel Mühe geben, um den eigentlichen chirurgischen Eingriff möglichst sicher und minimalinvasiv durchführen zu können, mit erstattenden Versicherungen regelmäßig Diskussionen um die „Notwendigkeit“ dieser Maßnahmen. Dass dabei oft im Bereich der späteren prothetischen Versorgung durch gute Positionierung der Implantate viel labortechnischer Aufwand in der prothetischen Phase eingespart werden kann, wird meist nicht beachtet. Bei Patienten, die ihre Behandlung weitgehend selbst zahlen müssen und deshalb den Aufwand ebenfalls kritisch hinterfragen, hatte der Autor diese Probleme bisher nie.
Unterschätzte Risiken
Natürlich war der Planungsaufwand bei Implantationen vor 25 Jahren ein geringerer und die Diagnostik dem damaligen Stand der Technik angepasst. Obwohl jedoch auch mit eher minimalen Diagnosemaßnahmen zu dieser Zeit viele Implantate erfolgreich gesetzt werden konnten, muss bedacht werden, dass die Patientenauswahl damals deutlich kritischer erfolgte, ganz besonders im Hinblick auf Mundhygiene und Allgemeinerkrankungen wie etwa einen gut eingestellten Altersdiabetes. Bei Kettenrauchern ist sicher nach wie vor Zurückhaltung angesagt. Neben den im Implantatanamnesebogen abgefragten Details sollten Zahnärzte auch stets im Auge haben, ob der Patient evtl. psychische Auffälligkeiten mitbringt und ob die Erwartungen des Patienten an die neue Versorgung realistisch umsetzbar sind. Eine Hilfe hierbei ist ggf. auch der Kölner ABC-Risiko-Score für die Implantatbehandlung des BDIZ.
Die Abbildungen 2–5 zeigen, dass nicht alles, was klinisch nach wie vor unproblematisch funktioniert, tatsächlich auch so problemlos ist. Dies betrifft sowohl die offensichtliche vestibuläre Fehlpositionierung von Implantatspitzen im Oberkiefer, besonders im Eckzahnbereich (Abb. 1), als auch massive linguale Perforationen im seitlichen Unterkiefer (Abb. 2). Auch Implantatenden in der Kieferhöhle müssen nicht zwangsläufig zu Problemen führen: Wie knapp am nach mesial verlaufenden Mentalisloup das Implantat hier tatsächlich gesetzt wurde (Abb. 3), war dem Autor als Behandler nicht bewusst und fiel erst bei der dreidimensionalen Planung der Implantate im Unterkiefer links auf. Dass ein Implantat nach Entfernung eines UK-Molaren manchmal mit wenig Diagnostik sofort gesetzt werden kann, sei unbestritten – allerdings wird in solchen freihändigen Fällen das Implantat nachher meist entweder in der mesialen oder in der distalen Alveole orientiert sein (Abb. 4) und damit zwangsläufig eine eher ungünstige extraaxiale Belastung des Pfeilers in Kauf genommen. Diese Beispiele gelten dennoch als klinisch erfolgreiche Implantate, die Abbildungen 1, 3 und 4 zeigen sogar eigene Fälle des Autors, die nach vielen Jahren nach wie vor unproblematisch in situ und in Funktion sind.
Auch wenn Implantate freihändig mit genügend Abstand voneinander gesetzt werden können, erleichtert eine vorherige prothetische Orientierung die Vermeidung des Fehlers, der hier im Oberkiefer links offensichtlich gemacht wurde. Wirklich problematisch ist allerdings die Versorgung rechts mit einem in prothetisch unbrauchbarer Achse eingeheilten Implantat, das mit seiner Spitze den Nachbarzahn verletzt (Abb. 5).
Unliebsame Überraschungen
Gelegentlich gibt es jedoch auch intraoperativ Überraschungen. Ein Eckzahn, bei dem nach erster Diagnostik ausreichend Knochenhöhe zur Verfügung stand, zeigte nach Aufklappung nur eine papierdünne Knochenlamelle von der ehemaligen palatinalen Wand der Alveole, sodass die Implantation letztlich erst nach Knochenaufbau (hier mit einer Titanmembran) und nochmaligem „Bone Spreading“ bei Implantatinsertion (Abb. 6) gelang. Sicher ist es wesentlich vorteilhafter, eine solche Situation (man beachte hier [Abb. 7] die klinische Dicke der Schleimhaut des Oberkiefers bei einem Nichtanlagefall) im Vorfeld des chirurgischen Eingriffs zu kennen und seine Therapie – einschließlich Zeit- und Kostenplanung für den Patienten – rechtzeitig darauf einzustellen.
2-D-Bilder können ganz ähnlich aussehen, obwohl sich die Situation als 3-D-Volumen dann sehr unterschiedlich darstellen kann: Bei Abb. 8 handelt es sich nicht um eine Nervverletzung, sondern um eine linguale Perforation. Bei Abb. 9 und 10 wurde dagegen geplant und beabsichtigt, mit einer separaten intraoperativen 3-D-Kontrollaufnahme geführt, in einem breiten Kiefer am Nerv vorbei implantiert. Dies soll hier ausdrücklich aber nicht als Standard empfohlen werden! Inzwischen sind meist mehrere kurze Implantate die bessere Alternative.
Zudem gibt es die traurigen Fälle, in denen nach der den Nervus alveolaris inf. tangierenden Implantation bei 36 wegen „unklarer Beschwerden“ auch noch die benachbarten Zähne 34 und 35 mit schwer überprüfbarer Indikation entfernt wurden. Angezeigt wäre gewesen, das unmittelbar postoperativ noch nicht osseointegrierte Implantat nach sofort eingeleiteter Diagnostik ein wenig zurückzudrehen und damit den Nerv zu entlasten (Abb. 11).
Im Sinne des Patienten
Ein Beispiel einer OPG-Planung mit zwei Röntgenmesskugeln (Abb. 12) zeigt übrigens, dass sogar innerhalb eines OPGs die Vergrößerungsfaktoren um bis zu 20 Prozent voneinander abweichen können: Wird das OPG auf der Seite der kleiner dargestellten Messkugel auf 5 mm kalibriert, so hat die Kugel auf der Gegenseite (objektiv gleich groß) im Röntgenbild auf einmal einen Durchmesser von 6 mm. Hier bleibt es dem Gefühl des Behandlers überlassen, ob er seine Sicherheitsabstände entsprechend erhöht und eventuell unnötig kurze Implantate verwendet oder bereit ist, ein höheres Risiko einzugehen. Alternativ stehen hierbei inzwischen sehr effektive Planungshilfen und diagnostische Möglichkeiten zur Verfügung.
Auf evidenzbasierte Studien, die in doppelt verblindetem Seitenvergleich die Überlegenheit von 3-D-geplanten und minimalinvasiv geführt gesetzten Implantaten gegenüber der „Freihandimplantation“ belegen, werden Zahnärzte – schon aus ethischen Gründen – wohl verzichten müssen. Im Hinblick auf Genauigkeit, chirurgisches Trauma, postoperative Schwellung und vom Patienten angegebene Beschwerden kann der Autor dieses Artikels aus seiner operativen Erfahrung diese Überlegenheit allerdings eindeutig feststellen. Auch von anderen Autoren gibt es inzwischen viele Fallberichte, die eine deutliche Korrelation der postoperativen Morbidität mit der Invasivität des Eingriffs bestätigen.
Fallbeispiel
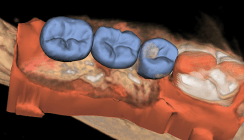
Im hier gezeigten Fall wurde sechs Wochen nach Zahnentfernung im Bereich des ehemaligen knöchernen Septums in idealer prothetischer Position ein Implantat geplant (Abb. 13), wobei der prothetische Vorschlag mit dem radiologischen 3-D-DVT-Datensatz gematched wurde. Die so gefundene Idealposition konnte mit einer vollgeführten Implantation eins zu eins umgesetzt werden, das Implantat wurde sechs Wochen postoperativ mit einer im CAD/CAM-Verfahren hergestellten, einteiligen Abutmentkrone versorgt; rechts unten in Abb. 13. Diese Art der prothetischen Versorgung mit extraoral durchgeführter Verklebung auf einer Titanbasis eliminiert völlig das Risiko einer durch Zementierung verursachten periimplantären Entzündung („Zementitis“). Dabei bleibt der prothetische Aufwand in einem sehr überschaubaren Rahmen, da keine Modelle mit Laborimplantat, Übertragungspfosten, Abdruckhilfskappen, Gingivamasken, individuelle Löffel und Ähnliches benötigt werden. Als einzige implantatbezogene Aufbauteile sind für die optische Erfassung der spätere Titankern (CAD/CAM-Basis) und ein wenig kostenintensiver Scanbody notwendig. Die Herstellung kann, wenn nötig, sogar in einer Sitzung erfolgen. Natürlich wäre das auch ohne entsprechenden Planungsaufwand lösbar gewesen – die Positionierung hätte aber vermutlich zu Kompromissen geführt.
Schablonenposition und Gingiva-Management
Zugegeben schwierig wird die geführte Implantation im zahnlosen Kiefer, wenn sichere Befestigungsmöglichkeiten an Zähnen zur stabilen Lagerung einer Schablone fehlen. Es kann durchaus sinnvoll sein, längerfristig nicht erhaltungswürdige Zähne zur Fixierung einer Bohrschablone noch bis zur Implantatinsertion zu belassen und ggf. erst bei Implantation zu entfernen. Die in der Literatur gelegentlich angegebenen großen Abweichungen zwischen Planung und Ausführung sind nach Erfahrung des Autors nur durch eine ungenügende Lagesicherung der Röntgen- bzw. Bohrschablonen zu erklären. Geht der Behandler hier sorgsam vor, wird er mit deutlich besseren Ergebnissen belohnt – die Planungssysteme an sich funktionieren sehr exakt (Abb. 14). Eine prothetische Versorgung im Unterkiefer, bei der die Implantatpositionen nach erfolgreicher Osseointegration genau im Bereich des Interdentalraums zweier Zähne liegen, wünscht sich ganz sicher niemand.
Nach früheren Erfahrungen mit einem Hülse-in-Hülse-System, das sehr lange Bohrer in zwingend parallel einzuführende Hülsen zur Führung verwandte und deswegen gerade im dorsalen Bereich oft Platz- und Handlingprobleme verursachte, verwendet der Autor nun ein flexibleres Bohrsystem. Alle Bohrer sind in dem in der Schablone fixierten Führungsring ohne zusätzliche Hülse sicher geführt und haben einen definierten Tiefenanschlag. Gebohrt wird regulär auf vollem Durchmesser, nur Schritt für Schritt in die Tiefe. Da der vordere Teil der Bohrung leicht konisch ist, können die Bohrer sogar etwas angewinkelt in die Schablone bzw. den Bohrstollen eingekippt werden, bevor sie durch den parallelwandigen Teil sicher geführt die Bohrung Schritt für Schritt vertiefen – aus Sicht des Autors derzeit für geführte Implantatbohrungen der beste Ansatz. Falls Bone Spreading geplant ist, gibt es auch Bohrer mit geringem Durchmesser, die nur die Implantatachse fixieren. Es ist auch immer möglich, mit einem kleinen krestalen Schnitt die Gingiva um die geplanten Implantatdurchtrittsstellen etwas zu mobilisieren und hernach dicht zu vernähen oder um die Gingivaformer zu positionieren, um keine befestigte Gingiva zu verlieren. Wenn die Gingiva gestanzt wird, können die ausgestanzten Teile auch problemlos als „freies Schleimhauttransplantat“ an die alte Position reponiert werden und heilen dort problemlos wieder ein, wenn doch eine gedeckte Einheilung sinnvoll erscheint. Patienten, bei denen der Autor in einzelnen Quadranten mit reichlich befestigter Gingiva nach Stanzung implantiert und an anderer Stelle die Gingiva zum Schutz vor Gewebeverlust leicht mobilisiert und vernäht hat, empfinden meist die Implantation „ohne Nähte“ als deutlich atraumatischer (Abb. 15).
In MKG Update 2015 schreibt S. Haßfeld zur DVT-Bildgebung und Implantatplanung: „Der Fragestellung der klinischen Relevanz der DVT widmet sich die Arbeitsgruppe Guerrero et al., die bei 365 inserierten Implantaten bei 108 Patienten untersuchten, ob die Diagnostik mit DVT gegenüber der konventionellen Planung mit Panoramaschichtaufnahmen eine bessere Einschätzung der Notwendigkeit augmentativer Maßnahmen und eine Vorhersage von Komplikationen zulässt. Bei der Operationsplanung durch vier erfahrene Operateure zeigte die DVT-basierte Diagnostik wesentlich bessere Ergebnisse.“
(Nicht nur) eine Kostenfrage
Im Vergleich mit Kostenplänen für Einzelzahnversorgungen mit Implantaten, die nur nach OPG „freihand“ gesetzt werden, stellt der Autor aufgrund der recht kostengünstigen Laborleistung keine höheren Gesamtkosten für seine aufwendiger geplanten Implantationen fest. Dies gilt umso mehr, wenn mehrere Implantate geplant sind – der Planungsaufwand ändert sich dadurch nur geringfügig.
Die Kosten für die Herstellung einer geführten Schablone sind in den letzten Jahren deutlich gesunken. In naher Zukunft kann eine entsprechende Schablone sogar direkt in der Praxis im CAD/CAM-Verfahren aus einem Kunststoffblock herausgefräst werden. In der aktuellen Version der CEREC-Software ist – allerdings nur im durchgängig mit Sirona-Geräten durchgeführten Workflow – diese Möglichkeit bereits implementiert. Bei aller Preisdiskussion sollte jedoch die Qualität, Sicherheit und Genauigkeit der Schablonen stets unbedingt im Blick bleiben.
Erfahrungsgemäß ist es – wie beim Matchen von CT/DVT und CAD/CAM-Daten – nur eine Frage von kurzer Zeit, bis entsprechende Lösungen auch mit „offenen Schnittstellen“ von Mitbewerbern implementiert werden.
Gelegentlich wird die Strahlenbelastung durch die DVT-Untersuchung als Gegenargument benutzt. Dabei sind – wegen der sehr unterschiedlichen Geräte – allgemeingültige Angaben schwierig. Ein Scan zur Planung von Implantaten mit 0,3 mm Auflösung und Aufnahme beider Kiefer liegt beim vom Autor verwendeten Gerät bei etwa 35 Mikrosievert und entspricht damit zwei bis drei üblichen Orthopantomogrammen oder etwa sieben Einzelaufnahmen. Umgerechnet ist der Patient damit der natürlichen Strahlenbelastung in einer Woche auf festem Boden oder bei etwa neun Stunden Flug ausgesetzt. Ein einfacher Flug in die Karibik entspricht damit in etwa der notwendigen Dosis für eine sorgfältig geplante Implantation – um die Frage von „Notwendigkeit“ und „Vertretbarkeit“ in eine auch patientenverständliche Relation zu rücken. Es lohnt sich jedenfalls sicher für Behandler und Patient, sich mit den neuen Planungs- und Diagnostikmöglichkeiten vor Implantationen intensiv zu befassen.