Implantologie 21.02.2011
Knochenersatz in der zahnärztlichen Chirurgie
Der Wunsch, Knochendefekte mit einem Ersatzmaterial zu füllen, besteht schon seit mehr als 4.000 Jahren. Ein Schädelfund aus den peruanischen Anden, bei dem ein frontaler Defekt mit einer 1mm starken Goldplatte bedeckt war, lässt darauf schließen, dass schon in dieser prähistorischen Zeit die Schädelkalotte nach Trepanation mit einem Ersatzmaterial versehen wurde.
Über die Jahrtausende wurden nun die verschiedensten Materialien, wie z.B. Kokosnussschalen aber auch schon Hundeknochen, für die Implantation verwendet. In der 2. Hälfte des 19. Jahrhunderts unterteilte Ollier Ersatzmaterialien nach ihrer Herkunft in autogene, allogene und xenogene Knochentransplantate.
Autogener Knochen
Autogener Knochen bedeutet, dass Spender und Empfänger das gleiche Individuum sind. Noch heute wird autogener Knochen als „Goldstandard“ bezeichnet, da es das einzige Transplantatmaterial ist, welches eine osteogene Eigenschaft besitzt, d.h. das Transplantat ist direkt an der Bildung und Entwicklung von Knochen beteiligt. Der große Nachteil liegt jedoch in der Gewinnung von autogenem Knochenmaterial, was immer einen Zweiteingriff mit allen entsprechenden Risiken notwendig macht. Als extraorale Spenderregionen dienen oft der Beckenkamm, das Tibiaplateau oder die Schädelkalotte. Intraoral kann Knochen aus der Unterkiefersymphyse, dem Tuber maxillae oder dem Ramus mandibulae gewonnen werden. Der Vorteil der intraoralen Knochenentnahme liegt in der verringerten Morbidität für den Patienten, wohingegen sich aufgrund des geringen Knochenangebotes eine extraorale Transplantatentnahme manchmal nicht vermeiden lässt.
Allogener Knochen
Im Gegensatz zum autogenen Knochen hat ein allogenes Knochentransplantat nicht dasselbe Individuum, allerdings dieselben Spezies als Ursprung. Das Transplantat kann dabei sowohl von einer lebenden zweiten Person oder einer Leiche entnommen werden. Der Vorteil der durch Gewebebanken kontrollierten Allotransplantate von Leichenspendern liegt in der großen Verfügbarkeit. Hingegen besteht wie bei Organtransplantationen immer ein Restrisiko hinsichtlich der Übertragung von Infektionskrankheiten (wobei das Übertragen von HIV eine Wahrscheinlichkeit von 1:1,6 Millionen hat) und antigener Abwehrreaktionen des Empfängers, da selbst Allotransplantate von Leichen bei Empfängern Immunreaktionen verusachen können. Um die Antigenität erheblich zu reduzieren, wird allogener Knochen gefriergetrocknet, welcher dann in mineralisierter Form (FDBA = Freeze Dried Bone Allograft) oder in demineralisierter Form (DFDBA = Demineralized Freeze Dried Bone Allograft) vorliegt. Beide haben gegenüber autogenen Knochentransplantaten den Nachteil der fehlenden osteogenen Eigenschaft, d.h. wenn mit allogenen Transplantaten augmentiert wird, muss immer mit einer längeren Knochenbildungszeit gerechnet werden. FDBA und DFDBA sollen sowohl durch Osteoinduktion (= die Fähigkeit, die Differenzierung von mesenchymalen Stammzellen zu unterstützen) als auch durch Osteokonduktion (= die Fähigkeit, Knochenwachstum entlang der Oberfläche zu unterstützen, d.h. eine Leitschiene für die knochenbildenden Zellen darzustellen) Knochen bilden. Der Unterschied zwischen FDBA und DFDBA liegt in der Mineralisation bzw. Demineralisation. Eine Demineralisation soll dabei Knochenkollagen und Wachstumsfaktoren, wie zum Beispiel Bone Morphogenetic Proteins (BMPs), freilegen. Verschiedene Studien haben gezeigt, dass mineralisierter gefriergetrockneter Knochen in verschiedensten Einsatzgebieten (Sinusbodenaugmentation, Auffüllen von Extraktionsalveolen oder kleinflächige Kieferkammaugmentationen) effektiver ist als demineralisierter gefriergetrockneter Knochen.
Seitenanfang
Knochenersatzmaterialien
Neben autogenen und allogenen Knochentransplantaten kamen gerade in den letzten Jahren die Knochenersatzmaterialien immer mehr zum Einsatz (aktuell sind 43 verschiedene Knochenersatzmaterialien auf dem deutschen Markt erhältlich). Ein großer Vorteil liegt bei Knochenersatzmaterialien darin, dass sie einen Zweiteingriff beim Spender nicht notwendig machen. Ein weiterer Vorteil vieler Knochenersatzmaterialien ist aufgrund ihrer synthetischen Herstellung das fehlende Infektionsrisiko, sodass eine Übertragung von Viren, Bakterien und auch Prionen sehr geringfügig ist. Allein Knochersatzmaterialien tierischer Herkunft (=xenogene Knochenersatzmaterialien) besitzen ein minimales Restrisiko für eine Übertragung von Prionen, obwohl eigentlich durch den Herstellungsprozess, das Wissen und die Überprüfung der Herkunft des Rohmaterials eine Eiweißübertragung fast ausgeschlossen werden muss. Dennoch besteht bei diesen Knochenersatzmaterialien eine Aufklärungspflicht.
Neben dem Fehlen des Zweiteingriffes und des Infektionsrisikos sollte ein Knochenersatzmaterial noch weitere Anforderungen erfüllen, wie z.B. eine ausreichende Stabilität, ein optimales Resorptionsverhalten, eine gute Verarbeitung und eine überschaubare Kostenentwicklung. Bislang konnte kein Knochenersatzmaterial alle Anforderungen zu 100% erfüllen und somit wurde noch kein Knochenersatzmaterial entwickelt, welches den autologen Knochen als „Goldstandard“ ersetzen kann. Der Hauptgrund dafür liegt, wie auch bei den allogenen Transplantaten, in der fehlenden osteogenen Potenz, wobei allerdings in einigen Studien bei manchen Knochenersatzmaterialien eine osteoinduktive Eigenschaft beschrieben wird. Die Anforderung, welche wohl fast alle heute verwendeten Knochenersatzmaterialien erfüllen, ist eine gute Osteokonduktion, d.h. dass die Ersatzmaterialien eine Art Führungsschiene für alle an der Knochenbildung beteiligten Zellen bilden. In der Tabelle ist eine kleine Auswahl unterschiedlicher Knochenersatzmaterialien nach verschiedenen Kriterien aufgeführt. Zur ersten Gruppe gehören die Hydroxylapatite. Dieses, in den letzten zwei Jahrzehnten meist aus Rinderknochen hergestellte, xenogene Hydroxylapatit hat den großen Vorteil, dass es sich als ein Bestandteil des natürlichen Knochens sehr gut mit benachbartem Hart- und Weichgewebe verbindet. Allerdings haben Hydroxylapatite eine sehr lange Resorptionszeit, sodass sie sich auch noch nach Jahren histologisch nachweisen lassen. Manchmal kann es bei Hydroxylapatiten zu einer bindegewebigen Einscheidung kommen und außerdem besteht die Gefahr von entzündlichen Gewebereaktionen. Neben den Knochenersatzmaterialien xenogenen Ursprungs scheint ein völlig synthetisch hergestelltes Knochenersatzmaterial der Firma Artoss diese Nachteile nicht mehr zu haben. Dieses neu entwickelte Knochenersatzmaterial NanoBone® wird in einem speziellen Sol-Gel-Verfahren hergestellt. Durch dieses Verfahren besitzt es eine ideale Nanostruktur, die als Leitschiene für Osteoblasten notwendig ist. Neben der sehr guten osteokonduktiven Eigenschaft soll dieses Knochenersatzmaterial ein ideales Resorptionsverhalten (mehr als 98% Resorption nach acht Monaten) besitzen. Dadurch besteht die Chance, dass für dieses Knochenersatzmaterial die beiden größten Nachteile bisheriger Knochenersatzmaterialien auf Hydroxylapatitbasis (Resorptionszeit und Infektionsrisiko) nicht mehr gültig sind. Klinische Studien werden in kommender Zeit die bislang hauptsächlich in Tierversuchen erworbenen Ergebnisse entweder bestätigen oder widerlegen.
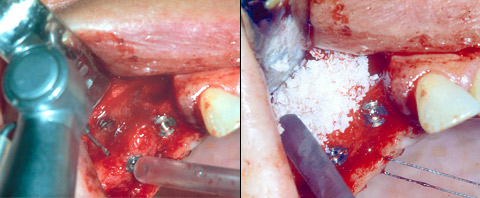
Abb. links Laterales Knochendefizit bei Zustand nach Implantation. Abb. rechts Augmentierter Bereich mit Knochenersatzmaterial.
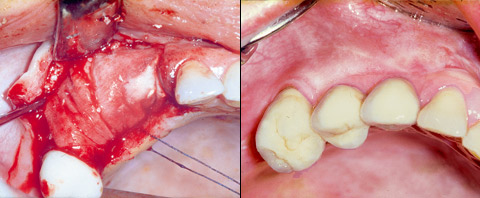
Abb. links Abdeckung des Knochenersatzmaterials mit Membran. Abb. rechts Zustand nach Implantatversorgung Regio 13,14.
Neben den Hydroxylapatiten werden in Deutschland Knochenersatzmaterialien auf Trikalziumphosphatbasis (TCP) verwendet. Wie auch die Hydroxylapatite haben die Trikalziumphosphate sehr gute osteokonduktive Eigenschaften. Des Weiteren zeichnen sie sich durch eine gute Biokompatibilität und eine gute Resorbierbarkeit aus. Allerdings sind Trikalziumphosphate kein natürlicher Knochenbestandteil, wobei es auch teilweise in kristallines Hydroxylapatit umgebaut werden kann. Zudem besteht die Gefahr, dass die synthetisch auf Trikalziumphosphatbasis hergestellten Knochenersatzmaterialien ein zu schnelles Resorptionsverhalten zeigen.
Um die Vorteile der Knochenersatzmaterialien beider Gruppen bestmöglich zu nutzen, entwickelten u.a. die Firma Straumann mit Bone Ceremic® oder die Firma DOT mit Bonit® ein Knochenersatzmaterial, welches zu 60% aus Hydroxylapatit und zu 40% aus Trikalziumphosphat besteht. Bislang fehlen jedoch klinische Studien, welche beweisen, dass sich gerade diese Kombination als Knochenersatzmaterial besonders gut eignet. Neben Hydroxylapatiten und Trikalziumphosphaten gibt es noch weitere alloplastische Knochenersatzmaterialien, wie z.B. die bioaktive Glaskeramik, das polymere Knochenersatzmaterial oder Kalziumsulfate, welche zwar in klinischen Untersuchungen viele o.g. Anforderungen erfüllt hatten, allerdings eher selten eingesetzt werden.
Seitenanfang
Membranabdeckung von Knochenersatzmaterialien
Bei der Frage, ob Knochenersatzmaterialien alleine oder in Kombination mit einer Membran eingesetzt werden sollten, scheiden sich bis heute die Geister. Die Philosophie im Einsatz der Knochenersatzmaterialien zusammen mit einer Membran liegt in der Barrierefunktion der Membran. Diese soll den gefüllten Defekt vor dem Einwandern der „schnelleren“ Fibroblasten gegenüber den „langsameren“ Osteoblasten schützen. Mehrere Studien haben gezeigt, dass der Einsatz einer Membran für die Dimensionstreue durch eine Reduzierung der Resorption aller wichtiger Weich- und Hartgewebsstrukturen notwendig ist. Des Weiteren schützt eine Membran das Blutkoagel und verhindert den Verlust des Knochenersatzmaterials, welcher bis zu 61% betragen kann, wenn keine Membran eingesetzt wird. Im Gegensatz dazu findet man in der Literatur auch kritische Stimmen zum Einsatz einer Membran in Kombination mit einem Knochenersatzmaterial. Ein Grund dafür ist, dass eine Membran schwierig zu platzieren sei, die Operationszeit damit verlängert und zusätzliche Kosten verursacht werden. Bei nichtresorbierbaren Membranen ist zusätzlich immer noch ein Zweiteingriff zum Entfernen der Membran erforderlich. Es wird auch beschrieben, dass Knochenersatzmaterial allein eine Weichgewebseinwanderung inhibiert, da es selbst als physikalische Barriere dienen kann. Außerdem soll der Einsatz einer Membran sogar den Verlust der Weichgewebsdicke verursachen, da die Barrierefunktion einer Membran die Versorgung des Wundlappens durch den umgebenden Knochen verhindert und eine alleinige Versorgung über die Lappenbasis zu einem Verlust der Weichgewebsdicke führen kann. Das größte Argument keine Membran zu benutzen, liegt in der Membranexposition und der dadurch erhöhten Gefahr, eine Infektion hervorzurufen. Die Inzidenz dafür wird zwischen 30–50% beschrieben. Wahrscheinlich wird die Erfahrung jedes Einzelnen die Frage beantworten, ob man Knochenersatzmaterial allein oder in Kombination mit einer Membran benutzen sollte.
Einsatz von Knochenersatz
Anfänglich kam Knochenersatz hauptsächlich in der Mund-, Kiefer- und Gesichtschirurgie zum Einsatz. Dabei wurde sowohl in der Traumatologie als auch in der Tumorchirurgie autologer Knochen zu rekonstruktiven Zwecken verwendet. Nur die Defektauffüllung nach Zystektomien konnten in der zahnärztlichen Chirurgie mittels Knochenersatzmaterialien gut versorgt werden. Aber schon seit vielen Jahren ist mit dem stetigen Wachstum der Implantologie ein Knochenersatz in jeder chirurgisch orientierten Praxis nicht mehr wegzudenken. Waren vor Jahren oft noch wirtschaftliche Gründe, d.h. dass die Kosten für ein Implantat über den Möglichkeiten des Patienten lagen, der limitierende Faktor, so kann man heute beobachten, dass oft das fehlende Knochenangebot eine Implantation unmöglich machen kann, da mindestens eine vertikale Dimension von 6–8mm und in transversaler Richtung von 5mm benötigt werden. Und genau dort kann dann ein Knochenersatz Abhilfe schaffen. Bei großen Knochendefiziten reicht ein Ersatzmaterial allerdings nicht aus. Der „Goldstandard“ liegt dabei immer noch in der Transplantation von autogenem Knochen allein oder bei kleinerer Transplantatentnahme in Kombination mit einem Knochenersatzmaterial.
Socket preservation
Seit einiger Zeit gewinnt die präimplantäre Chirurgie immer mehr an Bedeutung. Um einem Alveolenkollaps vorzubeugen, sollte man Zähne knochenschonend, d.h. mit Periotom und/oder Luxator ohne den Einsatz einer Zange, extrahieren. Allerdings reicht es wohl heutzutage nicht mehr aus, eine Alveole sich seiner eigenen Heilung zu überlassen, da es schon in den ersten drei Jahren post extractionem zu einem Verlust der Knochenhöhe von 40–60% kommen kann. Um diesem entgegenzuwirken, ist der Erhalt der Alveole in der Implantologie immer dann von größter Bedeutung, wenn aus den verschiedensten Gründen ein Sofortimplantat oder eine verzögerte Sofortimplantation nicht möglich ist. Streng nach dem Motto „when we take something out, we should put something back“ (Ashman) wird dann in der ridge bzw. socket preservation (Alveolarkammprophylaxe) Knochenersatzmaterial in die frische Extraktionsalveole appliziert. Dabei hat sich wohl schon fast jedes Knochenersatzmaterial in vielen klinischen Studien als geeignet erwiesen. Wie auch im Einsatz mit einer Membran muss jeder selbst seine eigene perfekte Alveolarkammprophylaxe entwickeln, um dann später ein Implantat mit ausreichender Knochenbedeckung primär stabil einbringen zu können.
Fazit
Zusammengefasst lässt sich feststellen, dass in der heutigen Zeit Knochenersatz in der zahnärztlichen Chirurgie ein fester Bestandteil der therapeutischen Möglichkeiten geworden ist. Die Möglichkeiten beginnen beim autologen Knochen, d.h., dass dem zu Transplantierenden auch das Transplantat entnommen wird. Geläufige Spenderregionen sind von extraoral der Beckenkamm und von intraoral der Unterkiefer. Um die Morbidität und das Risiko eines Zweiteingriffes, welcher bei autologen Knochentransplantaten immer vorliegt, zu umgehen, stellen autologer Knochen (Empfänger und Spender sind zwei Individuen derselben Spezies) und Knochenersatzmaterialien eine gute Alternative dar. Speziell die Knochenersatzmaterialien haben den Vorteil der großen Verfügbarkeit, dem fehlenden Infektionsrisiko und der sehr guten osteokonduktiven Eigenschaft. Vielleicht wird auch in naher Zukunft bei einem Knochenersatzmaterial in klinischen Studien eine osteoinduktive Eigenschaft nachgewiesen.
Autoren: ZA Tillmann Frauendorf, Prof. Dr. med. Wolfgang Sümnig







