Implantologie 03.12.2013
Periimplantäre Erkrankungen: Diagnose, Behandlung und Prävention
share
Periimplantäre Erkrankungen sind für Patienten ernsthafte Probleme, die den Implantaterhalt langfristig infrage stellen können und unmittelbar eine Entzündungsbelastung für den Körper darstellen. Für Zahnärzte bedeuten sie große therapeutische Herausforderungen.
Zu den periimplantären Erkrankungen zählen die periimplantäre Mukositis und die Periimplantitis, beides entzündliche Prozesse der Gewebe in unmittelbarem Kontakt zum Implantat. Bei der Mukositis sind nur die Weichgewebe entzündet, bei der Periimplantitis liegt zusätzlich auch noch ein Knochenverlust vor. All dies geschieht als Reaktion auf den bakteriellen Biofilm Plaque.
Allgemein gilt als anerkannt, dass etwa 10 Prozent der Implantate und 20 Prozent der Patienten von diesem Problem betroffen sind (Mombelli et al. 2012). Diagnostiziert werden diese Erkrankungen durch die Kombination von visueller Inspektion, Sondieren (Luterbacher et al. 2000) und Röntgenuntersuchung (Etter et al. 2002), wobei Ausgangsbefunde nach Eingliedern des Zahnersatzes zum späteren Vergleich obligat sind (5. ITI Consensus Statements 2013). In der Praxis stellt sich das klinische Management als denkbar schwierig heraus. So zeigt uns die aktuelle Studienlage, dass die nicht chirurgische Therapie der Periimplantitis nicht funktioniert. Frühe Diagnose und rasches chirurgisches Eingreifen scheinen daher geboten. Angesichts der zur Verfügung stehenden chirurgischen Maßnahmen und den einhergehenden Problemen, wie eher selten akzeptable ästhetische Resultate bei resektiver Chirurgie mit Implantoplastik, werden immer komplexere Methoden vorgeschlagen, z.B. das Kombinieren von resektiven und regenerativen Vorgehen mit teilweiser Implantoplastik. Wenn dann zusätzlich ein Bindegewebstransplantat aus ästhetischen Gründen zeitgleich empfohlen wird, kann der Leser sich bei zunehmender Komplexität des Eingriffs die sinkende Vorhersagbarkeit und Praxistauglichkeit errechnen. Es stellt sich daher dringend die Frage, ob und wie sich das Auftreten periimplantärer Erkrankungen verhindern oder reduzieren lässt.
Ätiologische Faktoren
Eine gute Evidenzlage bestätigen uns die folgenden ätiologischen Faktoren der periimplantären Erkrankungen: inadäquate Hygiene, Vorgeschichte einer Parodontitis, Qualität der Parodontaltherapie, Frequenz und Qualität des Recalls sowie Rauchen. Wir wissen, dass die Entzündungsprozesse am Implantat denen der Parodontitis sehr ähneln, wenn auch nicht ganz die gleichen. Das Entzündungsinfiltrat dringt bei Implantaten in der Regel ausgedehnter und schneller in tiefe Gewebsbereiche vor, und ein selbstlimitierender Effekt, wie er bei der Parodontitis beobachtet werden kann, scheint an Implantaten zu fehlen.
Wo beginnt die Prävention?
In einer Studie zur experimentellen periimplantären Mukositis beim Menschen konnte eindeutig gezeigt werden, dass die Mukositis entsteht, wenn Maßnahmen zur Mundhygiene ausgesetzt werden, und auch, dass bei Wiederaufnahme entsprechender Mundhygienepraktiken die Entzündungen komplett reversibel sind, wenn auch Letzteres etwas länger braucht als bei einer Gingivitis am Zahn (Salvi et al. 2012). Frühes Erkennen einer periimplantären Mukositis und deren Behandlung stellt also die einfachste Periimplantitisprävention dar, die uns zur Verfügung steht. Dazu ist wesentlich, dass die Position der Implantate und die Suprakonstruktionen so gewählt werden, dass sie einen guten Zugang sowohl für das klinische Sondieren als auch für die tägliche, häusliche Mundhygiene prinzipiell erlauben. Von Serino & Ström 2009 wissen wir, dass in Situationen, die keinen Zugang für Hygiene erlauben, das Auftreten von Periimplantitis sogar 48 Prozent betragen kann. In diesem Sinne beginnt die Prävention der Periimplantitis bereits bei der korrekten Planung und Positionierung der Implantate und Herstellung von reinigbaren Suprakonstruktionen. Obwohl für andere ätiologische Faktoren wie iatrogene Einflüsse, z.B. Zementreste, Fehlen keratinisierter Gingiva, nicht vollständig von Knochen umgebener Implantatoberfläche, aber auch Diabetes mellitus und Alkoholkonsum, die Evidenzlage eher limitiert ist, sollten diese dennoch nicht unterschätzt werden. So ist beispielsweise die Entfernung von Zement bei überhängenden Konstruktionen oft nicht oder nur unzureichend möglich. Die Auswirkungen von verbleibenden Zementresten können schwere periimplantäre Entzündungen sein. Mit verschraubten Rekonstruktionen lässt sich dieses Problem eliminieren. Bei Schwierigkeiten mit dem Zugang zum Sondieren lassen sich verschraubte Versorgungen auch zu diesem Zwecke abnehmen, und sollte ein chirurgischer Zugang zum Implantat notwendig werden, erleichtert die Abnehmbarkeit der Versorgung den Eingriff erheblich.
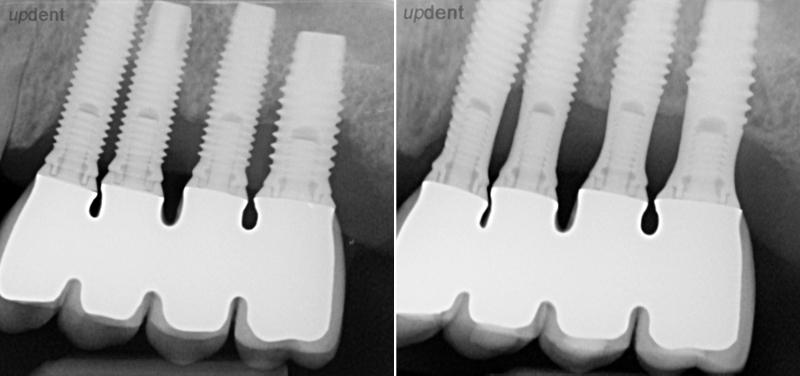
Abb. 1: Röntgenologisch sichtbarer periimplantärer Knochenabbau, deutlich erkennbar der beschränkte Zugang für Hygienemaßnahmen durch zu nahe beieinanderstehende Implantate. – Abb. 2: Konsolidierung der Knochenkontur 15 Monate nach resektiver Chirurgie mit Implantoplastik, deutlich erkennbar auch der teils beachtliche Substanzabtrag an den Implantaten.
Vorgeschichte von Parodontitis wesentlich
Einen wesentlichen Einfluss auf die Langzeitüberlebensrate von Implantaten hat die Vorgeschichte einer Parodontitis. So sind die Überlebensraten nach 10 Jahren bei Patienten mit moderater Parodontitis 94,2 Prozent und bei Patienten mit schwerer Parodontitis mit 90 Prozent deutlich niedriger im Vergleich zu 98 Prozent bei parodontal gesunden Patienten (Roccuzzo et al. 2010). Entsprechend betrugen die Implantatverluste bei Patienten mit moderater Parodontitis 5,8 Prozent, bei Patienten mit schwerer Parodontitis 10 Prozent und bei parodontal gesunden Patienten 2 Prozent. Innerhalb der Gruppe der Parodontitispatienten konnte zudem in dieser Studie eindeutig gezeigt werden, dass die Patienten, die nicht am regelmäßigen Recall teilnahmen, fast doppelt so häufig Periimplantitis aufwiesen als die, die regelmäßig zum Recall kamen (47,2 Prozent vs. 27 Prozent, p = 0,002). Ein regelmäßig und qualitativ hoch ausgelegter Recall vermag also deutlich zur Reduzierung des Auftretens von Periimplantitis und Implantatverlust beizutragen.
Parodontale Resttaschen – ein Risiko?
Wie steht es um parodontale Resttaschen, sind diese ein Risiko für Periimplantitis? Auch hier zeigen sich eindeutig Zusammenhänge. In einer Studie, die teilbezahnte Patienten über acht Jahre beobachtet, zeigen die Ergebnisse, dass Parodontitispatienten, die Resttaschen (d.h. mindestens eine Tasche ≥ 6mm) aufweisen, zu 17,4 Prozent einen Knochenverlust > 3 mm an Implantaten aufweisen, während es bei ausbehandelten Parodontitispatienten ohne Resttaschen nur 3 Prozent sind. Im Vergleich, bei den parodontal gesunden Patienten trat entsprechender Knochenverlust an 3,3 Prozent der Implantate auf (Lee et al. 2012). Dies legt nahe, anzunehmen, dass durch konsequente Parodontaltherapie und Recall auch bei Parodontitispatienten das Risiko für das Auftreten periimplantärer Erkrankungen annähernd auf das gesunder Patienten gesenkt werden kann.
Entscheidungsdilemma: Implantate beim Parodontitispatienten
Doch auch wenn dies für die Mehrzahl der parodontal erkrankten Patienten gelten mag, gibt es Ausnahmen. In einer Veröffentlichung von Donos & Laurell & Mardas 2012 wird sehr anschaulich das Entscheidungsdilemma zum Thema Implantate beim Parodontitispatienten dargelegt. In der Parodontologie ist bekannt, dass es eine kleine Untergruppe der Parodontitispatienten gibt, bei denen keine Therapie auf lange Sicht Erfolg hat und Zahnerhalt garantiert. Diese sogenannten refraktären Parodontitispatienten oder auch „downhill“ oder „extreme downhill“ Patientengruppen erleben fortschreitenden Attachmentverlust auch bei konsequenter Therapie, kontinuierlicher Diagnose und Behandlung potenziell reinfizierter Stellen und Recall (Hirschfeld & Waserman 1978). Zudem unterscheiden wir chronische und aggressive Parodontitiden, deren Unterscheidung bei fortgeschrittenem Stadium und ohne Verlaufsgeschichte nicht immer so eindeutig ist. Dazu kommen verschiedene Kombinationen mit Rauchen und anderen systemischen Faktoren. Dieselben Faktoren, die zu erhöhter Empfänglichkeit für Parodontitis führen, mögen auch das Risiko für Periimplantitis erhöhen (Fardal & Linden 2008).
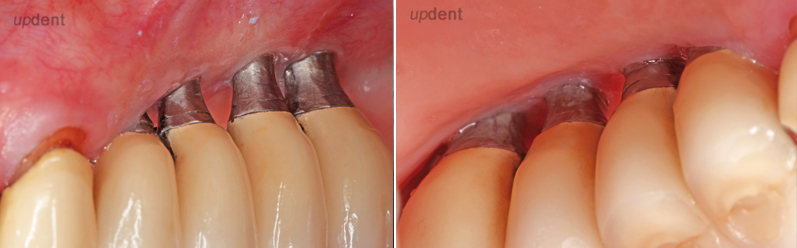
Abb. 3: Klinischer Zustand nach resektiver Chirurgie mit Implantoplastik, entzündungsfrei aber mit wenig verbleibender keratinisierter periimplantärer Mukosa bukkal. Patientin kommt regelmäßig zum 3-monatigen Recall. – Abb. 4: Von palatinal deutlich zu sehen der erschwerte Zugang für Hygienemaßnahmen, bedingt durch den resultierenden Unterschied im Niveau der Gewebe.
Und die Mikrobiota?
Zwischen Periimplantitis und Parodontitis gibt es verblüffend viele Ähnlichkeiten betreffend der ätiologischen Faktoren, auch was die Mikrobiota betrifft. Eine mögliche Erklärung ist die, das parodontale Pathogene von betroffenen Zähnen auf Implantate übertragen werden (Mombelli et al. 1995, Papaioannou et al. 1996). Das Vorhandensein putativer Pathogene an Implantaten ist in der Tat mit höheren Sondierungswerten und klinischer Entzündung korreliert. Es muss jedoch betont werden, dass allein das Vorhandensein von Pathogenen kein absoluter Vorhersagefaktor für Erkrankungen am Implantat ist. In der Praxis sehen wir gelegentlich Periimplantitis bei Patienten, die nicht die klassischen Risikofaktoren zeigen. Im Übrigen lassen sich die parodontalen Pathogene auch nicht durch Extraktion aller Zähne eliminieren (Quirynen & Van Assche 2011).
Risikoanalyse
Eine Risikoanalyse auf Patientenniveau sollte folgende Parameter berücksichtigen: Prozentualer Index des Bluten auf Sondieren, Vorhandensein von Resttaschen ≥ 5 mm, Anzahl verlorener Zähne, Attachmentverlust oder Knochenniveau in Relation zum Alter des Patienten, systemische und genetische Faktoren, Rauchen. Demnach können Patienten eingestuft werden als solche mit niedrigem, mittlerem und hohem Risikoprofil. Bei Patienten mit mittlerem Risiko sollten verbleibende Parodontaltaschen mit weiterführenden Mitteln eliminiert oder reduziert werden, bevor es zur Implantation kommt. Ein Beispiel für einen Patienten mit hohem Risikoprofil wäre einer, der eine signifikante Anzahl von Resttaschen hat, die auf Sondieren bluten, mit suboptimaler Hygiene und/oder Rauchgewohnheit und/oder schlecht eingestelltem Diabetes mellitus. Bei solchen Patienten sollte die weiterführende Parodontaltherapie zur Taschenelimination und Zahnerhalt im Vordergrund stehen und eine Versorgung mit Implantaten zeitlich möglichst lang nach hinten hinausgeschoben werden. Auch sollten andere restaurative Alternativen in Erwägung gezogen werden. Das Erkennen des Risikoprofils eines Patienten setzt voraus, dass eine mögliche Parodontalerkrankung diagnostiziert und der Patient einer entsprechenden Therapie zugeführt wird. Auch bedarf es der in der Parodontaltherapie üblichen längeren Beobachtungszeiträume mit entsprechend regelmäßig erneuter Evaluierung der parodontalen Situation, bevor eine Einschätzung dazu gemacht werden kann, wie die individuelle Reaktion auf die Therapie ausfällt.
Klinische Erfahrung und Evidenz bedeutend
In Zeiten, in denen sogar vorgeschlagen wurde, Implantate mit Periimplantitis frühzeitig „proaktiv“ oder „strategisch“ zu extrahieren, damit zukünftiger Knochenverlust verhindert wird und möglichst schnell ein neues Implantat gesetzt werden kann, halte ich es für wichtig, sich auf die klinische Erfahrung und Evidenz zu besinnen, die uns klar bestätigt, was vorhersagbar funktioniert. In der Parodontologie können wir auf eine lange Tradition guter wissenschaftlicher Untersuchungen zurückschauen. Die Therapiekonzepte sind für die große Mehrzahl der Parodontitispatienten vorhersagbar erfolgreich und bei konsequenter Durchführung ist Zahnerhalt und die Gesunderhaltung von Implantaten über viele Jahre sehr gut möglich. Prävention ist ein Gesamtkonzept, bei dem das Herstellen und Aufrechterhalten klinischer Situationen, die das Risiko für das Auftreten von periimplantären Erkrankungen minimieren, im Vordergrund stehen. Empfehlungen zu diesem Thema finden Sie auch in den 5. ITI Consensus Statements 2013 (Gruppe 5).










