Laserzahnmedizin 24.03.2015
Lasertherapie von fibromatöser Prothesenstomatitis
share
Die Zahl der älter werdenden Menschen steigt und mit ihnen auch die Zahl der durch das Tragen von Prothesen entstehenden Erkrankungen. In der Alterszahnmedizin werden zunehmend Prothesenfibrome diagnostiziert, die meist von einer Prothesenstomatitis begleitet werden. Bei einer Behandlung der erkrankten Areale sind altersgerechte, minimalinvasive Konzepte zur chirurgischen Korrektur und Bearbeitung gefordert. Wie der folgende Fall zeigt, ist der Diodenlaser hierbei ein sicheres Werkzeug zur blutarmen und gleichzeitig schnellen Intervention bei der Schaffung gesunder Tegumente.
Eine durch demografische und sozioökonomische Entwicklungen immer häufiger auftretende Diagnose in der zahnärztlichen Praxis ist die schlecht sitzende, herausnehmbare prothetische Versorgung älterer Patienten. Oftmals zu beobachten sind neben der eingeschränkten Mundhygiene durch diverse Erkrankungen, die durch das zunehmende Alter progrediente Züge erfahren können, auch immer wichtiger werdende ökonomische Aspekte, die eine geriatrische Umarbeitung in Form einer Korrektur des vorhandenen Zahnersatzes oder gar einer Neuanfertigung unmöglich machen. Daher sind Prothesenrandfibrome oder generelle fibromatöse Veränderungen des tragenden Teguments immer häufiger zu beobachten. Die älteren Patienten, welche auch meistens von kardiologischen, hämatologischen und endokrinen Erkrankungen gekennzeichnet sind, bedürfen einer relativ raschen, jedoch trotzdem gut organisierten und möglichst minimalinvasiven chirurgischen und medikamentösen Intervention.
Fibröse Hyperplasie
Der Terminus „Epulis“ ist eine rein klinische Beschreibung einer lokalisierten Gingivawucherung, bei der unterschiedliche histopathologische Diagnosen nicht ausgeschlossen sind. Daher wird in der histopathologischen Klassifikation nach Axhausen und hauptsächlich in den deutschsprachigen Ländern dieser Terminus verwendet, wobei die WHO-Klassifikation von der „fibrösen Hyperplasie“ redet und diese die histologische Befundung mit aufnimmt. Daher sollte nach der histopathologischen Festlegung der sogenannten Epuliden folgende Termini benutzt werden:
- pyogenes Granulom,
- fibröse Hyperplasie oder
- peripheres Riesenzellgranulom.
Die fibröse Hyperplasie ist als meist breitbasige, derbe Wucherung der Gingivaschleimhaut definiert. Die Sonderformen und die am meisten diagnostizierten Veränderungen der fibrösen Hyperplasie in der zahnärztlichen Praxis bilden die Prothesenrandfibrome und die sogenannten Reizfibrome. Das Reizfibrom liegt ubiquitär in der Mundhöhle und häufig auf Höhe der Interkalarlinie. Sie sind in der Regel reaktive, entzündlich bedingte, lokalisierte Läsionen. Das Prothesenrandfibrom bzw. Prothesenfibrom ist häufig multipel und kulissenartig gestaffelt. Die Oberfläche ist gelegentlich ulzeriert, wobei die ätiologischen Ursachen in der Prothesenbeweglichkeit liegen und der provozierten Entzündung durch Mastikation und Sprache.
Prothesenstomatitis
Eine Infektion des Prothesenlagers ist die Folge eines multifaktoriellen Geschehens. Zur Auslösung einer entzündlichen Schleimhautreaktion und zur Entstehung klinischer Symptome müssen Einflüsse wie eine mangelhafte Prothesenhygiene, diätetische Faktoren oder systemische Erkrankungen hinzukommen. Folgende Aufteilung zur Pathogenese kann vorgenommen werden:
- 1. Mechanisches Trauma als Folge einer schlecht passenden oder rauen Prothesenbasis, einer zu hohen, vertikalen Kieferrelation, einer fehlerhaften Okklusion oder durch Parafunktionen.
- 2. Mikrobielles Trauma infolge toxischer Produkte der bakteriellen Plaque an der Unterfläche der Prothesenbasis.
- 3. Endogene Ursachen, wie der Xerostomie-Faktor bei Diabetes und der reduzierten Immunabwehr als Folge einer Bestrahlungstherapie oder Chemotherapie.
- 4. Werkstoffkundliche Aspekte in Form einer seltenen aber möglichen allergischen Reaktion des Teguments.
Folgende Typen der Prothesenstomatitis werden unterschieden:
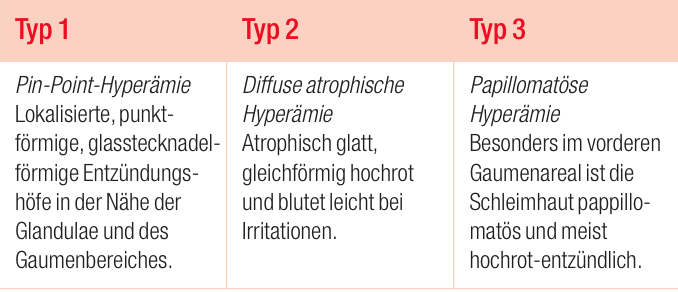
Therapiekonzept
In unserer Praxis wird an diesen Erkrankungsformen sowohl chirurgisch als auch medikamentös, konzeptionell und zielgerichtet therapiert. Falls nötig werden fachärztliche Konsile mit anderen Disziplinen eingeleitet. Am Anfang stehen eine Fotodokumentation, ein Candida-Test und eine Probeexzision mittels Laser zur pathohistologischen Bestimmung. Nach erfolgter Klassifikation durch das pathohistologische Labor erfolgt eine aktive stufenweise Eliminierung der Ätiologien wie folgt (Abb. 1).
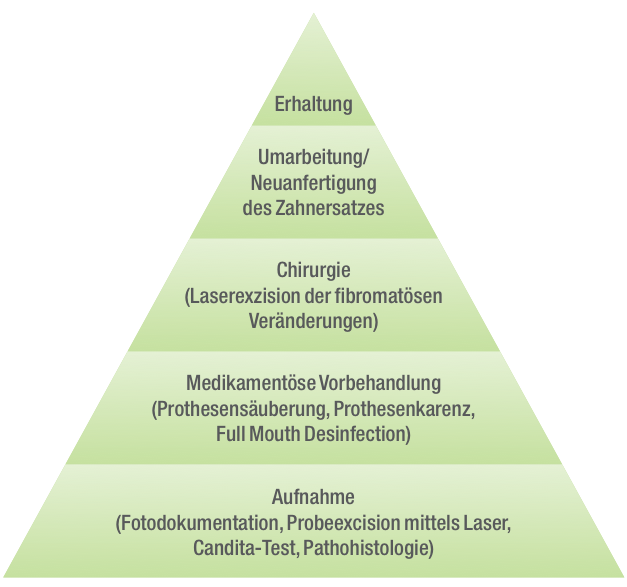
Abb. 1: Therapiepyramide der fibromatösen Prothesenstomatitis.
Phase 1
In Phase 1 ist zunächst eine Desinfektion und Säuberung der betroffenen Prothese und gegebenenfalls auch der antagonistischen Prothese durchzuführen. Es folgt die Anwendung der Full Mouth Desinfection sowohl bei zahnlosen als auch bei teilbezahnten Patienten bei einer gleichzeitigen, einwöchigen Prothesenkarenz. Wesentlicher Bestandteil der Full Mouth Desinfection ist die häusliche Anwendung von 0,2%igen Chlorhexidinlösungen und -gelen auf den Schleimhautarealen. Je nach klinischem Bild ist die Anwendung zwei- bis dreimal täglich zu verordnen. Erst nach dieser ersten Phase erfolgt die nächste Stufe der Therapiepyramide.
Phase 2
Phase 2 sieht eine Laserexzision der fibromatösen Veränderungen vor, bei dem ein minimalinvasives Glätten der Tegumentarchitektur zur Eliminierung von Gingivataschen und „Schlupfwinkel“ (detailliertes Vorgehen siehe Fallbericht) erfolgt.
Phase 3
Nach der Laserexzision erfolgt eine circa fünf- bis siebentägige, nächtliche Prothesenkarenz und tagsüber eine Applikation von Miconazol (Dumicoat®) an der Unterseite der Prothesenbasis. Zudem wird eine kohlenhydratarme Kost empfohlen und es erfolgen Instruktionen zur regelmäßigen Reinigung der Prothesenunterfläche mit weicher Bürste.
Phase 4
In Phase 4 erfolgt eine Umarbeitung des Zahnersatzes in Form einer Unterfütterung und die Einleitung einer prothetischen Neuanfertigung.
Phase 5
In der letzten Phase geht es um die Erhaltung der Prothese. Hier werden systemische Recalls in der Prophylaxeabteilung (viermal jährlich Prothesenreinigung) und zahnärztliche Nachsorgen durchgeführt.
Fallbericht
Die Patientin kam in unsere Praxis mit dem Wunsch einer Exzision von geschwollenen Veränderungen entlang ihrer Implantate. Diese beeinflussten den Tragekomfort ihrer Oberkieferprothese bzw. die Funktion der Druckknöpfe und deren Mechanismus zur Stützung der Prothese (Abb. 2).
Anamnese
Die Anamnese zeigte eine tägliche Einnahme von ASS 100 aufgrund kardiologischer, hämatologischer Erkrankungen, daher auch die Einnahme mehrerer Präparate zur Stabilisierung des Herz-Kreislauf-Systems sowie einer Altersdiabetes. Die vorhandenen Prothesen waren bereits zehn Jahren in situ (Abb. 3). Die Patientin äußerte auch den Wunsch einer anschließenden Neuanfertigung der Prothetik sowohl im Ober- als auch Unterkiefer. Die röntgenologische Beurteilung erfolgte durch ein Orthopantogramm (Abb. 4). Hier zeigten sich achsenverschobene Implantate im Oberkiefer und eine für das Alter der Patientin nachvollziehbare Atrophie der knöchernen Strukturen.
Das klinische Bild zeigte mehrere Prothesenfibrome, welche lappen- und pilzförmig entlang der Implantate, aber auch an den tragenden Schleimhautarealen tumöros ansetzten und teils breitbasig, teils punktuell das ganze Tegument belegten. Hinzu kam eine durchgehend rötliche Veränderung, welche auf eine Prothesenstomatitis rückschließen ließ.
Einsatz des Diodenlasers
Nach einer einwöchigen, medikamentösen Vorbehandlung und der Kennzeichnung des Behandlungsraumes durch Warnschild und Warnleuchte sowie der Einhaltung sämtlicher Lasersicherheitsparameter (Brillen etc.), wurde das Operationsgebiet mit dem Präparat Ultracain D-S 1:200.000 (Sanofi-Aventis,Frankfurtam Main) anästhesiert und insgesamt 1,50 ml in Form einer fortlaufenden Anästhesie infiltriert. Zur Verwendung kam dabei ein 970-nm-Diodenlaser (SIROLaser Advanced, Klasse IV; Sirona, Bensheim; Software 2.0.6).
Unter dem Menüpunkt „Fibrom“ wurden 6 W im Dauerlichtmodus (cw) und ein daraus resultierendes Tastverhältnis von 50 Prozent eingestellt. Das Arbeitshandstück wurde mit einer 300 μm (Kerndurchmesser) Faser und einer Aktivierung über den Fingerschalter verwendet. Mit streichenden, untermittierenden Führungsbewegungen wurden zunächst die Bereiche entlang der Implantate bearbeitet, bis auch die peripheren kleineren und größeren Prothesenfibrome entfernt worden waren. Somit wurde das Gingivarelief mittels Laser geglättet. Immer wieder wurden Carbonisierungsrückstände von der Laserspitze entfernt, wodurch der Gesamteingriff circa fünf Minuten dauerte (Abb.5 und 6). Die Nachsorge eine Woche nach dem Eingriff zeigte ein heilendes Bild des Teguments mit weitaus gesunder Koloration der Gingivaanteile. Auffallend war, dass auch die Schwellung der Schleimhautareale nachgelassen hatte (Abb. 7). Es wurden keine postoperativen Schmerzen und Narbenbildungen beobachtet.
Fazit
In der Geriatrischen Zahnmedizin werden zunehmend Prothesenfibrome und die meist dadurch verursachte Begleiterkrankung Prothesenstomatitis, welche Träger von Candida albicans sein kann, diagnostiziert. Altersgerechte, minimalinvasive Konzepte zur chirurgischen Korrektur und Bearbeitung erkrankter Areale werden daher immer wichtiger. Der Diodenlaser ist hierbei ein sicheres Werkzeug zur blutarmen und gleichzeitig schnellen Intervention bei der Schaf- fung gesunder Tegumente. In der Planung neuer Versorgungen kann der Laser eine funktionstüchtige Basis für den Zahnersatz schaffen, ohne Narbenbildung und postoperative Wundheilungsstörungen zu verursachen. Der 970-nm-Diodenlaser sollte sowohl in der präprothetischen Chirurgie als auch in der risikobehafteten Geriatrischen Zahnmedizin seinen festen Platz haben.
Hier gibt's die vollständige Literaturliste









 Proto-Cam® Smart
Proto-Cam® Smart  Patientenbrille P07.P1P11.1001
Patientenbrille P07.P1P11.1001  Laserschutz-Lupenbrille F27P1M03
Laserschutz-Lupenbrille F27P1M03  IPL-Brille F22P5L04 für Behandlungspersonal
IPL-Brille F22P5L04 für Behandlungspersonal  F18P1C02 für Dentallaser Anwendungen
F18P1C02 für Dentallaser Anwendungen  WaterLase MDX
WaterLase MDX  Waterlase Epic X
Waterlase Epic X  Waterlase Express
Waterlase Express  Maskensystem Axess™
Maskensystem Axess™  Accutron-Doppelmaskensystem seda-view®
Accutron-Doppelmaskensystem seda-view® 






