Prophylaxe 02.06.2023
Schmelz-Matrix-Proteine in der Dentalhygiene?
share
Der S3-Leitlinie der European Federation of Periodontology ist in der Anpassung der Deutschen Gesellschaft für Parodontologie zu entnehmen, dass eine regenerative Therapie bei entsprechender Indikation in der dritten Therapiestufe durchgeführt werden soll. Unter anderem ist der Einsatz eines Schmelz-Matrix-Protein-Derivates (EMD) eine dieser Therapiemöglichkeiten.1 Eine Anwendung in Kombination mit einer Reinstrumentierung von Resttaschen ist hier ebenfalls möglich.2 Es stellt sich die Frage, ob die sogenannte Flapless-Anwendung mit Schmelz-Matrix-Protein-Derivaten vor dem Hintergrund des deutschen Delegationsrahmens als zahnärztliche Leistung an die Dentalhygiene delegiert werden kann. Eine Literaturrecherche, die sich auf die beschriebene Vorgehensweise des Methodikteils von neun Studien konzentriert und zusammenfasst sowie die Nomenklatur der Interventionen finden in diesem Beitrag Berücksichtigung. Abschließend sind Abrechnungspositionen und der Delegationsrahmen miteinander in Verbindung zu bringen.
EMD wird in der parodontalen Therapie seit gut drei Jahrzehnten eingesetzt und untersucht.3 Bei den für die parodontale Regeneration verwendeten Schmelz-Matrix-Proteinen handelt es sich um das Sekret der Zellen der Hertwigschen Epithelscheide tierischen (porcinen) Ursprungs.4 Die Schmelzmatrix beinhaltet circa 90 Prozent Amelogenin und regt die Bildung von neuem azellulärem Zement auf der Wurzeloberfläche an.5, 6 Während der Odontogenese sind die Schmelz-Matrix-Proteine für die Differenzierung der Progenitorzellen zur Bildung von Wurzelzement, Ligamentfasern und Alveolarknochen verantwortlich.7 Sie haben Einfluss auf die Zellproliferation und Differenzierung.8 Sculean et al. (2000) dokumentierten „new attachment“ und Knochenneubildung nach Anwendung von Schmelz-Matrix-Protein-Derivaten (z. B. Emdogain®, Straumann).9 In 2008 dokumentierten Sculean et al. die Neubildung von Zement und desmodontalem Faserapparat.10 Bosshardt kommt in seinem Review (2008) zu dem Ergebnis, dass Schmelz-Matrix-Proteine zu einer Adhäsionszunahme der Zellen des desmodontalen Faserapparats und der osteogenen Zellen führen. Die Proliferation der Fibroblasten des Parodontalligaments sowie die Angiogenese werden besonders begünstigt und angeregt. Sie wirken sich positiv auf die Wundheilung aus.
Proinflammatorische Zytokine, die in einer frühen Wundheilungsphase beteiligt sind, werden von Schmelz-Matrix-Proteinen herunterreguliert. Die Moleküle, die wachstums- und reparaturfördernde Eigenschaften haben, werden heraufreguliert. Des Weiteren haben Schmelz-Matrix-Proteine Einfluss auf Einzelvorgänge in der Genexpression. Hierunter fallen Transkriptionsfaktoren, die mit der Differenzierung der Progenitorzellen von Chondro-, Osteo- und Zementoblasten verbunden werden. Zudem hat es eine stimulierende Wirkung auf die Transkription und Translation der Proteinsynthese spezieller interzellulärer Matrixmoleküle und eine regulierende Wirkung auf den Knochenumbau.11 Gaßmann et al. (2009) dokumentierten den Einfluss von Schmelz-Matrix-Proteinen auf chemotaktische Abläufe, Migration und Apoptose von CD4+ T-Helferzellen.12 Somit wirken Schmelz-Matrix-Proteine auf biologische Prozesse ein und lösen eine Reihe von positiven Kaskaden im Wundheilungsprozess aus.11, 13
Seit mehr als 20 Jahren ist bekannt, dass die Vermeidung eines chirurgischen Eingriffs einen Mehrwert für Patienten darstellt.14 Bereits Jahre vor der Markteinführung von Emdogain® FL (Straumann) auf der IDS im Jahr 2019 zeigten Studien erfolgreiche Ergebnisse nach Applikation von EMD in parodontale Defekte mithilfe einer nichtchirurgischen Vorgehensweise.2, 15 Mit der seit 2019 modifizierten Applikationskanüle von Emdogain® FL ist es möglich, das Schmelz-Matrix-Protein-Derivat flapless in den parodontalen Defekt bzw. in die Residualtasche in verschiedenen Therapiestufen der systematischen Parodontaltherapie zu applizieren.16 Außerdem sind Schmelz-Matrix-Proteine in der Lage, ihre Eigenschaften bei der Behandlung von periimplantären Entzündungen zu entfalten.17, 18
Nach einer systematisch durchgeführten Parodontitistherapie kommt es zu einer epithelialen Tiefenproliferation und somit zur Bildung eines langen Saumepithels. Hierbei handelt es sich um parodontale Reparation.19 Um eine parodontale Regeneration zu initiieren, ist es nach einem parodontalen Eingriff notwendig, das entstandene Blutkoagulum zu stabilisieren und eine epitheliale Tiefenproliferation zu verhindern.20 Die parodontale Regeneration ist ein komplexer Vorgang und zeichnet sich idealerweise durch die vollständige Wiederherstellung des zerstörten Zahnhalteapparats in Funktion und Struktur aus. Beteiligt sind das Wurzelzement, das parodontale Ligament, die Gingiva und der Alveolarknochen.21 Eine wesentliche Rolle kommt im Rahmen der parodontalen Regeneration der komplikationslosen, primären gingivalen Heilung zu.22 Die parodontale Regeneration setzt das Verbleiben von gesunden Zellen voraus, die in der Lage sind, diese zu fördern. Das parodontale Ligament und das Wurzelzement haben eine Schlüsselfunktion im Regenerationsprozess. Progenitorzellen aus den perivaskulären Bereichen des Granulationsgewebes im parodontalen Defekt wandern zur Wurzeloberfläche und differenzieren sich dort unter dem Einfluss von EMD zu Zementoblasten und den parodontalen Ligamentzellen. Neu gebildete Ligamentfasern bilden einen Befestigungsapparat und inserieren in neu gebildetem Wurzelzement. Die ossären Progenitorzellen migrieren in Richtung Ligamentfasern, proliferieren und reifen ebenfalls. Gemeinsam heften sie sich an das Wurzelzement.23
Es stellt sich die Frage, ob die sog. Flapless-Anwendung vor dem Hintergrund des deutschen Delegationsrahmens als zahnärztliche Leistung an die Dentalhygiene delegiert werden kann. Bekanntermaßen können (Teil-)Leistungen aus den Therapiestufen eins, zwei und vier laut EFP-Leitlinie delegiert werden. Für die Delegation kommen vorzugsweise die Mitarbeiter aus der Dentalhygiene infrage.24, 25 Für diese Delegation ist es zum einen wichtig, zu eruieren, welche Indikationsvoraussetzungen gegeben sind und was mit flapless im Rahmen der nichtchirurgischen regenerativen Parodontaltherapie zu verstehen ist. Zum anderen sind die Nomenklatur der Interventionen, Abrechnungspositionen und der Delegationsrahmen miteinander in Verbindung zu bringen.
Indikation/Kontraindikation
Die klinische Anwendung von Schmelz-Matrix-Protein-Derivaten (Emdogain®) hat sich durch die Produkteinführung von Emdogain®FL erweitert. Mit einem minimalinvasiven nichtchirurgischen Vorgehen soll parodontale Regeneration gefördert werden.2 Die Anwendung wird bei parodontalen Defekten als indiziert gesehen, wenn eine Sondierungstiefe von ≥ 5 mm bis ≤ 9 mm vorliegt und sie frei von Furkationsbeteiligung ist.31 Als eine weitere Indikation kann das Vorliegen einer periimplantären Mukositis gesehen werden. Hier werden Sondierungstiefe und BOP (Bleeding on Probing) signifikant reduziert.17 Die Morphologie des Zahns und die damit verbundenen komplexen lokalen Begebenheiten können aufgrund ihres negativen Einflusses auf die Durchführung der Therapie eine Kontraindikation darstellen.27 So verhält es sich ebenfalls bei Patienten mit mangelnder Mundhygiene, Entzündungen mit Pusaustritt, bei starken Rauchern und schlecht zu kontrollierenden systemischen Erkrankungen, wie z. B. einem schlecht eingestellten Diabetes mellitus.28
Vorgehensweise
In Anwenderinformationen und Behandlungsprotokollen wird die Reinigung der Wurzeloberfläche vor der Applikation von Schmelz-Matrix-Protein-Derivaten empfohlen.29 Es fallen Begriffe wie Scaling and Root Planing im Zusammenhang mit der Vorbereitung der Wurzeloberfläche.30 Sayn (2022) spricht von subgingivalen Reinigungsverfahren.31 Ein mechanisches Debridement ist Bestandteil der Vorbereitung zur Behandlung einer periimplantären Mukositis z. B. mit Emdogain®FL.32 Hahner et al. (2021) formulieren die Unterschiede zwischen den verschiedenen Begrifflichkeiten im Zusammenhang der subgingivalen Instrumentation wie folgt:
- Scaling: Entfernen von Biofilm und supra- und subgingival gelegenem Zahnstein von der Zahnoberfläche.
- Root Planing (Wurzelglättung): Glätten der nach Scaling aufgerauten Wurzeloberfläche.
- Parodontales Debridement: Entfernen oder Zerstören der Ablagerungen auf der Zahnoberfläche ohne absichtliches Abtragen von Wurzelzement wie beim Root Planing. Ziel ist der Erhalt des Wurzelzements zum Aufrechterhalten oder Reetablieren eines gesunden parodontalen Milieus.
- Subgingivale Kürettage: Entfernen des veränderten und nekrotischen Taschenepithels und des darunterliegenden Bindegewebes aus einer parodontalen Tasche zum Schaffen einer akuten chirurgischen Wunde.33
Die Ergebnisse der Literaturrecherche zeigten, dass Aimetti et al. (2017) das Flapless-Vorgehen als ein geschlossenes chirurgisches Vorgehen bezeichneten. Hier erfolgte die Durchführung des Flapless-Vorgehens durch ein Debridement der Wurzeloberflächen mithilfe von Miniküretten und feinen Ultraschallinstrumenten.26 Ein mechanisches Debridement bestand bei Faramarzi et al. (2015) aus der Anwendung von Ultraschallscaler und Pulver-Wasser-Strahlgerät auf Glycinbasis.17 Im Jahr 2022 führten Anoixiadou et al. unter der Bezeichnung minimally invasive non-surgical technique ein Scaling and Root Planing (SRP) mit Verwendung von Miniküretten und piezoelektrischem Ultraschallgerät unter Lokalanästhesie durch.34 Bei der Reinstrumentierung unter Lokalanästhesie verwendeten Jentsch et al. (2021) Miniküretten und Ultraschallspitzen für das Debridement.2 Ein subgingivales, mechanisches Debridement mit Ultraschallkunststoffspitzen und ein Pulver-Wasser-Strahlgerät mit subgingivaler Düse und auf Glycinbasis beschrieben Kashefimehr et al. (2017).18 Graziani et al. führten 2019 ein supra- und subgingivales Debridement und Scaling mit Ultraschallspitzen durch und bezeichneten es als SRP.35 Ein Debridement mit Miniküretten und feinen Ultraschallspitzen war das Verfahren von Aimetti et al. (2016).36 Ein SRP mit Hand- und Ultraschallinstrumenten führten Wyganowska-Świątkowska et al. (2013) zur Vorbereitung auf die EMD-Applikation durch.37
Studien ab Mitte der 1980er-Jahren zeigen, dass eine restlose Entfernung von Zahnstein und Konkrementen weder mit einem nichtchirurgischen noch mit einem chirurgischen Vorgehen möglich ist und sich das Reinigungsergebnis mit zunehmender Sondierungstiefe verschlechtert.38–41 Eine zahnhartsubstanzschonende Reinigung ist durch die Nutzung von Pulver-Wasser-Strahlgeräten für den supra- und subgingivalen Bereich durch speziell konzipierte Düsen und Pulverarten heute möglich.42 Eine Weichgewebstraumatisierung sowie die Entfernung von Granulationsgewebe sollte vermieden werden, da es zu Attachmentverlust und gingivalen Rezessionen führt.26, 35, 36
Zugang zur Parodontaltasche
Der Zugang zur Parodontaltasche und der Wurzeloberfläche konnte zwei Studien entnommen werden und erfolgte hier durch die Anwendung eines Gingivaretraktors und eines mikrochirurgischen Zahnspiegels.36, 26 Schallhorn et al. (2021), Aimetti et al. (2017) sowie Anoixiadou et al. (2022) verwendeten in ihren Behandlungen ein Operationsmikroskop und/oder eine Lupe.15, 26, 34 In der Studie von Di Gianfilippo et al. (2021) zeigen die Ergebnisse, dass der mikrochirurgische Ansatz in der parodontalen Chirurgie, zu dem auch die Anwendung von Operationsmikroskopen und Lupen gehört, eine positive Auswirkung auf Heilungsprozesse und klinische Ergebnisse hat.43
Trocknungs- und Blutstillungsverfahren
Miron et al. (2012) stellten in ihrer Untersuchung fest, dass die Wurzeloberfläche möglichst frei von Blut sein sollte, um eine gleichmäßige Adsorption von EMD auf der Wurzeloberfläche erzielen zu können.44 Dies lässt drauf schließen, dass das Blutstillungsverfahren vor der Applikation von EMD bei der Flapless-Anwendung eine wichtige Rolle spielt. Die Herangehensweise zum Trocknungs- und Blutstillungsverfahren wurde zum einen mithilfe des Einbringens von Gaze und kieferorthopädischer Zahnseide (Superfloss) sowie durch die Verwendung von Luftspray durchgeführt.35 Zum anderen kamen manuelle Kompression, Gaze, Papierspitzen, Mulltupfer und Kunststoffschaumschwämmchen zur Anwendung.2, 26, 36
Oberflächenkonditionierung
Die Applikation von Ethylendiamintetraessigsäure (EDTA) fand, mit Ausnahme einer, in allen Studien statt.2, 15, 18, 26, 34–37 In zwei Studien erfolgte die Applikation von EDTA mithilfe steriler, stumpfer Spritzen.2, 25 Kashefimehr et al. (2017) verwendeten in ihrer Studie eine Insulinspritze.18 Die Spülung der Tasche und der Wurzeloberfläche erfolgte in sieben Studien mit Kochsalzlösung.2, 15, 18, 26, 34, 36, 37 Graziani et al. spülten 2019 die Tasche mit Wasserspray sowie über die Spülfunktion der Ultraschallspitze.35 Faramarzi et al. (2015) machten keine Angabe dazu.17
EMD-Applikation
Die Applikation von EMD erfolgte 2019 in der Studie von Graziani et al. und 2021 in der Studie von Jentsch et al., mit steriler, stumpfer Spritze.2, 35 Eine Insulinspritze kam 2017 bei Kashefimehr et al. zum Einsatz.18 Die sechs anderen Studien machten keine weiteren Angaben hierzu.15, 17, 26, 34, 36, 37 In keiner der neun selektierten Studien, die für diese Literaturrecherche herangezogen wurden, berichteten die Autoren von der Anwendung und Applikation von Emdogain®FL.2, 15, 17, 18, 26, 34–37
Komprimierung des Margo gingivae und Recall-Intervall
Von einer Komprimierung des Margo gingivae unter Zuhilfenahme von Gaze berichteten drei Studien.2, 26, 36 Ein regelmäßiges Recall-Intervall mit Mundhygieneinstruktionen und/oder Biofilmmanagement wurde in allen Studien außer in der von Kashefimehr et al. durchgeführt.2, 15, 17, 26, 34–37 Allgemein betrachtet, zeigen die radiologischen sowie klinischen Ergebnisse der neun selektierten Studien schon zum damaligen Zeitpunkt einen Nutzen von EMD in Kombination mit einer Flapless-Anwendung.2, 15, 17, 18, 26, 34–37
Abrechnungspositionen und der Delegationsrahmen
Nach heutigem Kenntnisstand sieht die Therapiestufe drei der systematischen Parodontitistherapie einen parodontalchirurgischen Eingriff bei entsprechender Indikation vor. Regenerative Maßnahmen können unter anderem mit EMD durchgeführt werden. Die Vorgehensweise bezüglich der Zugangslappenbildung wurde hier offengelassen. Eine Flapless-Anwendung fand in der neuen S3-Leitlinie weder in Therapiestufe drei noch in der unterstützenden UPT in Therapiestufe vier Berücksichtigung.1
Mehr als zehn Millionen Menschen in Deutschland leiden an einer schweren Parodontitis.45 Die Mehrheit der Menschen in Deutschland ist entweder gesetzlich oder privat krankenversichert, ein kleiner Teil gar nicht. Eine regenerative Therapie findet in den aktuellen PAR-Richtlinien und somit im Einheitlichen Bewertungsmaßstab für zahnärztliche Leistungen (BEMA) keine Berücksichtigung. Es handelt sich damit um eine Leistung, die mit den Positionen der Gebührenordnung für Zahnärzte (GOZ) abgerechnet wird. Das Einbringen von EMD in einen parodontalen Defekt während einer Therapiestrecke oder im Rahmen der UPT kann entweder mit der 4110 der GOZ oder über eine Analogberechnung nach § 6 (1) der GOZ zusätzlich zu den entsprechenden BEMA-Positionen privat in Rechnung gestellt werden. Fällt die Vorbereitung der Wurzeloberfläche in die GOZ, werden die Nummern 4070 und/oder 4075 in Rechnung gestellt. Hier ist der Wortlaut und Inhalt mit einer parodontalchirurgischen Therapie verbunden.31 Geht es um einen chirurgischen Eingriff wie das Scaling and Root Planing, handelt es sich um eine selbst zu erbringende Leistung von Zahnärzten. Sollte im Vorfeld festgestellt werden, dass Teilleistungen dieser Positionen keinen chirurgischen Eingriff darstellen, sind diese vorzugsweise an die Dentalhygiene delegierbar.24, 25 Ziller (2022) weist auf die unzeitgemäße Leistungsbeschreibung der GOZ-Nr. 4070 und 4075 und die (Teil-)Delegation hin, wenn es sich um nichtchirurgische Interventionen im Rahmen dieser Gebührennummer handelt.25 Daher hat die Bundeszahnärztekammer nach Beratung mit Vertretern der privaten Krankenversicherungen und der Beihilfe eine Liste von Analogpositionen veröffentlicht, durch die eine an den S3-Leitlinien orientierte Parodontaltherapie besser abgebildet werden kann.47
Das frühere Scaling and Root Planing ist vom wesentlich minimalinvasiveren subgingivalen Debridement abgelöst worden.33 Das EMD kann bei entsprechender Indikation während der Parodontaltherapie in den Therapiestufen zwei und vier flapless, sprich ohne einen invasivchirurgischen Eingriff zur Lappenbildung, angewandt werden. 29, 30
Bei aller berufspolitischen Erwägung ist auch im Auge zu behalten, was weitere Studien zur Wirksamkeit der Verwendung von Derivaten, wie Emdogain® FL, zeigen werden. So wird im systematischen Review und einer Metaanalyse mit Bezug auf die Studien von Graziani et al. (2019)35, Jentsch et al. (2021)2 und Schallhorn et al. (2021)15 von Estrin et al. (2022)46 kein statistisch signifikanter Unterschied zwischen der nichtchirurgischen Parodontalbehandlung mit und ohne EMD gezeigt.
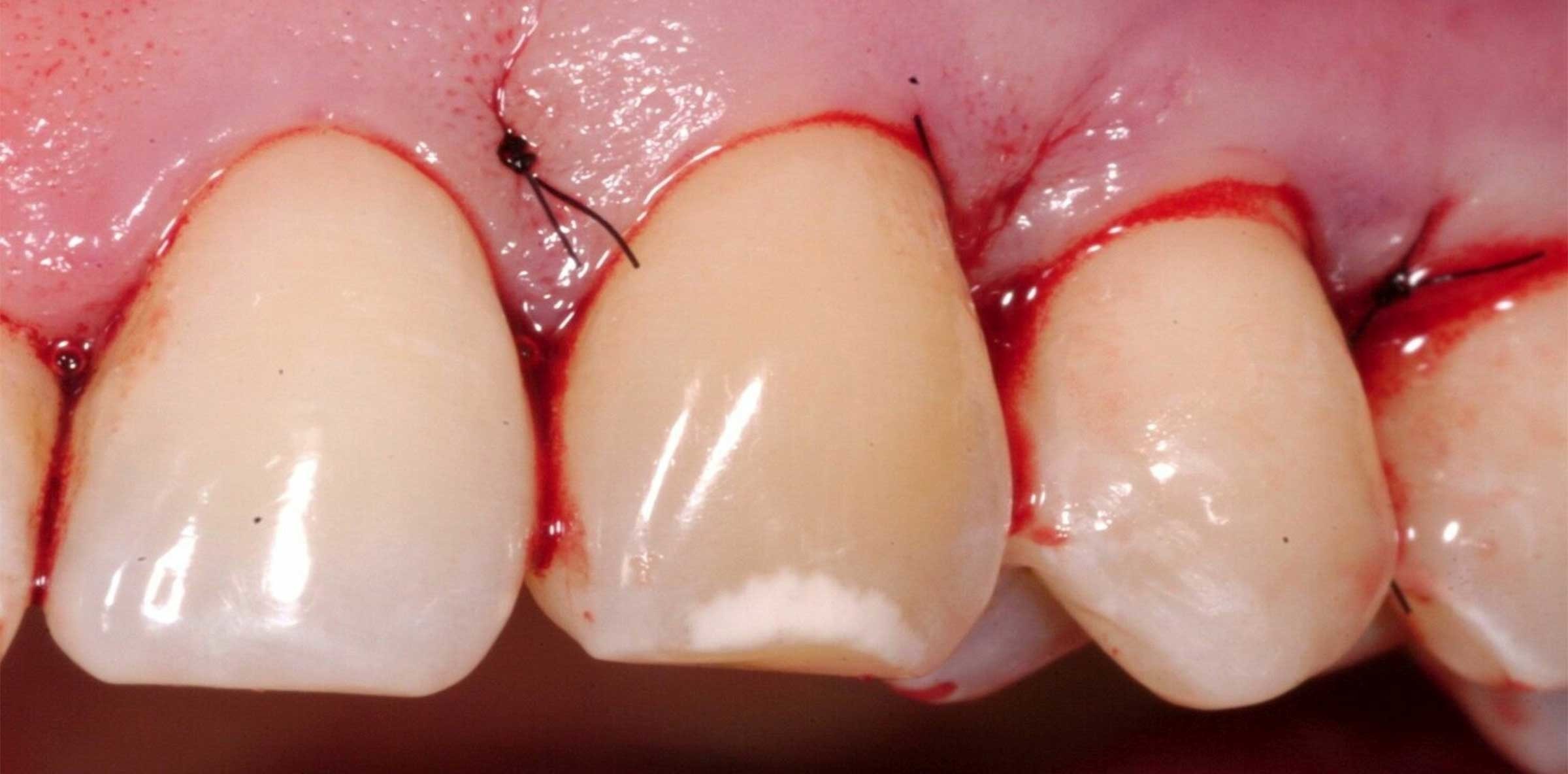
Abb. 1: Nahtverschluss nach EMD-Applikation im Rahmen eines chirurgischen Eingriffs. Die Vermeidung eines chirurgischen Eingriffs bedeutet einen Mehrwert für Patienten. © Juliane Petring, B.Sc., Prof. Dr. Peter Hahner, Prof. Dr. Georg Gaßmann
Schlussfolgerung
Die Recherche zeigt, dass die Behandlungsabfolge und Vorgehensweise keinem standardisierten Protokoll folgten. Die Komplexität ergibt sich aus dem Zusammenspiel des offen formulierten Delegationsrahmens und den nicht mehr zeitgemäßen Inhalten der GOZ bezüglich der Parodontaltherapie sowie der Nomenklatur der Interventionen im Rahmen der subgingivalen Instrumentation. Die Inhalte des deutschen Delegationsrahmens für Zahnmedizinische Fachangestellte werden kontrovers diskutiert und erlangten mit der Einführung der neuen PAR-Richtlinien im Juli 2021 hohe Aufmerksamkeit. Da (Teil-)Leistungen der Therapiestufen eins, zwei und vier delegierbar sind, stellt sich die Frage, ob die sog. Flapless-Anwendung vor dem Hintergrund des deutschen Delegationsrahmens als zahnärztliche Leistung an die Dentalhygiene delegierbar ist. Parodontal-regenerative Eingriffe und Verfahren können in verschiedenen Stufen indiziert sein und sollten Bestandteil eines parodontalen Konzeptes sein, das kurative sowie präventive Interventionen beinhalten kann.
Das Ziel dieses Beitrags war, durch eine Literaturrecherche in Erfahrung zu bringen, wie die Flapless-Anwendung von EMD durchgeführt wird, um Rückschlüsse auf die Delegierbarkeit des regenerativen Verfahrens im Rahmen der systematischen Parodontaltherapie ziehen zu können. Die Ergebnisse zeigen, dass die Vorbereitung der Wurzeloberfläche durch unterschiedliche Umsetzungen der Instrumentierung erfolgte, entweder maschinell, manuell oder in Kombinationsverfahren. Die Verdrängung der Gingiva, um bis zum Boden des parodontalen Defekts zu gelangen, erfolgte teilweise durch eine gezielte Retraktion der Gingiva. Die Applikation selbst wurde zum damaligen Zeitpunkt entweder mit der Applikationsspritze von Emdogain® durchgeführt oder mit zweckentfremdeten Spritzen. Es kann der Schluss gezogen werden, dass in den in der Literaturrecherche berücksichtigten Studien die Applikation von EMD mit Emdogain® bei einer Flapless-Anwendung mit einer stärkeren Manipulation der Weichgewebe verbunden war als mit dem heute verfügbaren Emdogain®FL. Aufgrund der Nomenklatur der Instrumentierung und der nicht eindeutig nachvollziehbaren klinischen Situationen in den einzelnen Studien, war nicht erfassbar, inwiefern es sich um Indikationen handelte, die ein Root Planing oder die Entfernung von Granulationsgewebe oder das „Aufdehnen“ der Gingiva gerechtfertigt hätten. Daher würde es sich um eine chirurgische und somit eine nicht delegierbare Leistung handeln. Die Delegierbarkeit der Flapless-Anwendung ist zum jetzigen Zeitpunkt nicht eindeutig allgemeingültig zu beantworten, sondern muss eine Einzelfallentscheidung sein. Die im deutschen Delegationsrahmen aufgeführten Qualifikationsvoraussetzungen sowie die beispielhaft aufgeführten delegierbaren Leistungen führen zu einer Interpretationsmöglichkeit seitens der Zahnärzte und der zahnmedizinischen Mitarbeiter. Liegt eine entsprechende Indikation für eine parodontale, nichtchirurgische regenerative Intervention vor und Zahnärzte entscheiden sich für eine Delegation, müssen die Qualitätssicherung und der Patientenschutz gewährleistet sein.
Eine Literaturliste steht hier für Sie bereit.
Dieser Beitrag ist in dem PJ Prophylaxe Journal erscheinen.
Bitte beachten Sie, dass CME-Artikel nach zwei Jahren ihre Gültigkeit verlieren.