Implantologie 06.06.2018
Knochenregenerationsmaterial bei Periimplantitistherapie
share
Periimplantitis ist eine der medizinischen Herausforderungen des 21. Jahrhunderts. Weltweit suchen Implantologen und Parodontologen immer wieder nach zuverlässigen und umsetzbaren therapeutischen Lösungen. Anhand eines klinischen Fallbeispiels zeigen die Autoren ihr bevorzugtes Protokoll einer Periimplantitisbehandlung auf. Dabei kommen ein biomimetisches Knochenersatzmaterial sowie eine resorbierbare Kollagenmembran zum Einsatz.
Periimplantitis wird definiert als eine lokale Läsion, die mit einem Knochenverlust um ein osseointegriertes Implantat einhergeht, während die periimplantäre Mukositis eine reversible entzündliche Veränderung der das Implantat umgebenden Mukosa ist.
Die Diagnose der periimplantären Mukositis erfolgt durch Sondierung, der eine Blutung folgt. Die Mukositis wird oft nicht als ernst eingestuft und auch von den Patienten nicht ernst genommen.Basierend auf unterschiedlichen Untersuchungen variiert die Prävalenz einer Periimplantitis zwischen 2 und 58 Prozent aller Implantate (Koldsland O.C. et al.). Ein 2011 veröffentlichter Cochrane-Report resümierte, dass die Evidenz bekannter Periimplantitisbehandlungen insuffizient ist und ein Bedarf an mehr Forschung auf diesem Gebiet besteht (Esposito M. et al.).
Im vorliegenden Report wird anhand eines klinischen Fallbeispiels Schritt für Schritt die Erfahrung des Autors mit seinem bevorzugten Protokoll der Periimplantitisbehandlung aufgezeigt.
Zur Verwendung kommen das Periimplantitis-Set Implacure® (MedTech Dental AG, Vertrieb Dtl.: mds GmbH) und ein regeneratives, biomimetisches Knochenersatzmaterial (CERASORB® M, Hersteller: curasan AG, Vertrieb: mds GmbH) zum Aufbau des verlorenen Knochens.
Beschreibung des OP-Protokolls
- Bildung und Mobilisierung eines Mukoperiostlappens für einen ungehinderten Zugang zum Defektbereich. Wenn möglich, Suprakonstruktion entfernen.
- Sorgfältige Kürettage des infizierten Bereichs mit gründlicher Entfernung aller Weichgewebsanhaftungen am Knochen.
- Reinigung der Implantatoberfläche, sowohl des apikalen Teils, der später mit dem Knochenersatzmaterial in Berührung kommt, als auch des krestalen Teils, der später mit der Mukosa in Kontakt kommt, unter Einsatz verschiedener Fräsen.
- Applikation einer sterilen Gaze zur Bedeckung aller freiliegenden Knochenoberflächen. Anschließend Befeuchten der Gaze mit steriler Kochsalzlösung, um die Anhaftung der Gaze am Knochen zu verbessern.
- Aufbringen eines Gels aus 37 % Phosphorsäure und 2 % Chlorhexidin auf die gesamte freiliegende Implantatoberfläche zur Desintegration des verbliebenen Biofilms.
- Nach zwei Minuten wird das Gel durch gründliches Spülen mit Kochsalzlösung entfernt. Anschließend Entfernen der Gaze.
- Die Implantatoberfläche wird mit einer sterilen Gaze vollständig bedeckt und die Gaze anschließend mit einer Natriumhyaluronat-Piperacillin-Tazobactam-Lösung imprägniert und für fünf Minuten belassen.
- Gaze entfernen.
- Das Knochenersatzmaterial wird in einem sterilen Gefäß mit einer Natriumhyaluronat-Piperacillin-Tazo- bactam-Lösung und Defektblut oder PRP angemischt und anschließend ohne Druck in den Defekt eingebracht. Defektdeckung mit einer resorbierbaren Kollagenmembran, die zuvor mit der antibiotischen Lösung imprägniert wurde.
- Wundverschluss durch Readaptation des Lappens und Naht.
Patientenfall
Ein 59-jähriger Patient erschien in der Praxis und beklagte ein leichtes Exsudat im Bereich seiner Frontzahnimplantate (Abb. 1). Die initiale Untersuchung mit Sondierung ergab eine tiefe zirkuläre Tasche um die Implantate. Eine Mobilität der Implantate wurde jedoch nicht festgestellt. Die röntgenologische Untersuchung bestätigte den Verdacht einer fortgeschrittenen Periimplantitis um die kürzlich gesetzten Implantate (Abb. 2).
Der Beschreibung des Protokolls folgend wurde ein Mukoperiostlappen gebildet, um den massiven vierwandigen Defekt vollständig darstellen zu können (Abb. 3). Mithilfe diamantierter Fräsen wurde die Implantatoberfläche mechanisch gereinigt (Abb. 4). Es folgte die chemische Reinigung der Oberfläche mit anschließender antibiotischer Imprägnierung (Abb. 5 und 6).
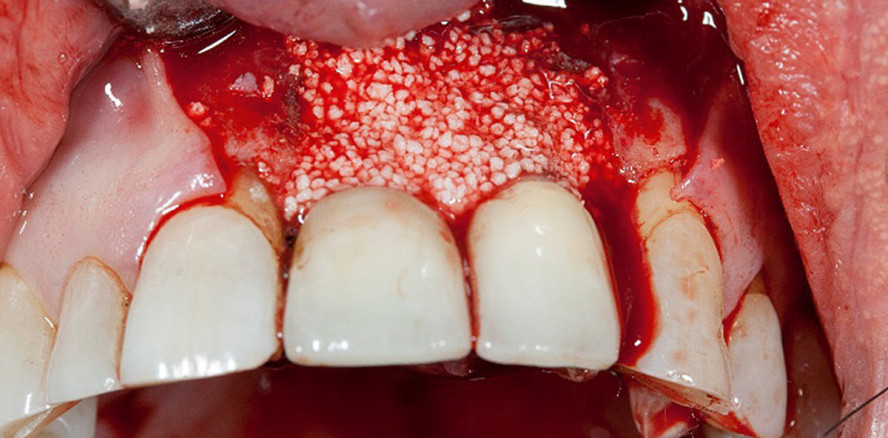
Nach Abschluss der Vorbereitungen wurde wie beschrieben das aus phasenreinem b-Tricalciumphosphat beste- hende Knochenersatzmaterial, welches mit seinen Mikro-, Meso- und Makroporen optimale Voraussetzungen für ein knöchernes Remodelling bietet, eingebracht (Abb. 7).
Schließlich wurde das Operationsgebiet mit der bioresorierbaren Membran abgedeckt und der Lappen mittels intermittierender Nähte zu einem vollständigen und dichten Wundverschluss readaptiert (Abb. 8). Die unmittelbar post OP angefertigte Röntgenaufnahme zeigt den aufgefüllten Defekt (Abb. 9). 24 Monate später kann man auf der Kontrollaufnahme eine gute knöcherne Konsolidierung auf Höhe der Schmelz-Zement-Grenze der Nachbarzähne erkennen (Abb. 10).
Diskussion
Periimplantäre Läsionen reagieren nicht sehr gut auf eine verbesserte Mundhygiene und professionelle Reinigung, was bei Parodontitis sehr effektiv ist. Dies soll nicht bedeuten, dass Prävention gegen eine Periimplantitis durch gute Mundhygiene und professionelle Zahnreinigung überflüssig sind. Hat sich jedoch erst einmal eine Periimplantitis entwickelt, ist die konservative Therapie ineffizient. Nichtchirurgische Ansätze mittels Laser oder Pulverstrahl weisen dürftige Erfolge auf. Systemische Chemotherapie und mechanisches Debridement sind auch weitgehend erfolglos.1–3
Als ebenfalls erfolglos hat sich der Einsatz Photodynamischer Therapie erwiesen. Zusammenfassend kann man sagen, dass nichtchirurgische Therapieansätze nicht geeignet sind, um Periimplantitis zuverlässig einzudämmen.1,4
Der einzig Erfolg versprechende Therapieansatz scheint die chirurgische Lösung zu sein. Eine chirurgische Resektionsbehandlung ist aber nur teilweise effektiv. 2003 stellte Leonhardt fest, dass chirurgische und antimikrobielle Behandlungen für einen Zeitraum von fünf Jahren in mehr als der Hälfte der Fälle erfolgreich war. Heitz-Mayfield et al. konnten 2008 aufzeigen, dass ein antimikrobielles Protokoll mit chirurgischem Zugang über Mobilisation eines Lappens in 90 Prozent der Fälle auf einen Zeitraum von einem Jahr das Fortschreiten der Periimplantitis unterbinden, wobei allerdings in mehr als 50 Prozent dieser Fälle die Blutung auf Sondierung persistierte.5
Unglücklicherweise eignen sich nicht alle Periimplantitisfälle für eine Regeneration. Bei Implantaten mit dünnen fazialen und lingualen Wänden entsteht typischerweise nicht die Kraterform mit vier Wänden. In einigen dieser Fälle geht der Defekt mit einem vollständigen Verlust der umgebenden knöchernen Begrenzungen einher, was die regenerative Maßnahme als eine unvorhersehbare Behandlungsalternative zurücklässt.
In allen vorgeschlagenen Behandlungsansätzen erweist sich die Implantatoberflächendekontamination als der kritische Schritt. Die komplexe Topografie moderner Implantate bietet ein ideales Rückzugsgebiet für bakterielles Wachstum. Die Dekontamination dieser Oberflächen erscheint manchmal unmöglich, vor allem, wenn man den nichtchirurgischen Weg wählt. Es gibt verschiedenste Optionen für die Oberflächendekontamination. Antiinfektive Behandlungen mit Chlorhexidin, Tetracyclin, Metronidazol, Zitronensäure, Laser und photodynamischer Applikation dienen der Desinfektion des Implantats. Mechanisches Debridement mit Titan-, Plastik- oder Stahlküretten, Implantoplastie oder Pulverstrahl soll den Biofilm entfernen. Die meisten Kliniker wählen eine Kombination aus diesen Therapien in der Annahme, dass die Oberflächendekontamination somit erfolgreich ist.
Implantoplastie gewährleistet eine absolute Dekontamination der Implantatoberfläche, jedoch existieren vier wesentliche Bedenken: Hitzeproduktion, Ablagerung von Fräsmaterial im umgebenden Gewebe, Beschädigung der Implantatoberfläche und Schwächung der Implantatstruktur. Die Hitzeentwicklung kann durch eine sorgfältige und reichliche Irrigation sowie eine angepasste Bohrerwahl eingedämmt werden. Einige Autoren vermuten, dass Ablagerungen aus Frässpänen sich klinisch nicht in Abstoßungsreaktionen zeigen. Die Reduktion der Mikro- und Makrorauigkeit der Implantatoberfläche bringt überwiegend Vorteile in der Behinderung von Bakterienkolonisation. Und schlussendlich ist die notwendige Abtragungsdicke am Implantat nicht ausschlaggebend für eine reduzierte Stabilität.6,7
Zusammenfassung
Die vorliegenden wissenschaftlichen Erkenntnisse und die klinischen Erfahrungen mit dem vorgestellten System lassen daher den Schluss zu, dass mit dem vorliegenden Protokoll ein für den Kliniker nachvollziehbares System für eine erfolgreiche Sanierung periimplantärer Defekte zur Verfügung steht, wenn gleichzeitig verloren gegangene Knochensubstanz regenerativ ersetzt wird. Hier hat sich das vollsynthetisch hergestellte, biomimetische b-TCP- Granulat bewährt. Durch eine Restitutio ad Integrum ist es möglich, das geschwächte Implantatlager nicht nur mechanisch, sondern auch biologisch in einen funktionellen Zustand zu versetzen, was die Grundvoraussetzung für eine langfristig erfolgreiche Sanierung ist.
Weiterer Autor: Dr. Gregor Thomas
Die vollständige Literaturliste gibt es hier.
Dieser Beitrag ist im Implantologie Journal 6/2018 erschienen.