Implantologie 27.02.2018
Behandlung von parodontalen und periimplären Infektionen
share
Anwendung eines antimikrobiellen Präparats
Die Kombination eines mechanischen Debridements unterstützt von einer sorgfältigen Dekontamination mithilfe eines antimikrobiellen Präparats auf Basis von Chloraminen, bietet eine gut dokumentierte nichtchirurgische Option zur Behandlung von parodontalen Entzündungen. In dieser Fallstudie wird die Übertragung dieses Konzepts auf die erfolgreiche Dekontamination einer periimplantären Mukositis vorgestellt.
Die steigende Zahl an Patienten mit Zahnimplantaten geht einher mit einer zunehmenden Zahl von Erkrankungen des periimplantären Hart- und Weichgewebes.1 Trotz einer hohen Überlebensrate nach zehn Jahren von circa 95 Prozent ist eine signifikante Zunahme an Spätkomplikationen, charakterisiert durch einen periimplantären Knocheneinbruch, zu verzeichnen.2–8 Die Prävalenz für Periimplantitis, fünf bis zehn Jahre nach Implantation, liegt im Bereich von 10 bis 20 Prozent.9,10 Begleitet von einer mangelnden Mundhygiene des Patienten, führen diese periimplantären Läsionen unbehandelt zum Verlust des Implantats und der entsprechenden Suprakonstruktion.11–14
Parodontale vs. periimplantäre Entzündungen
Parodontitis und Periimplantitis sind bakteriell bedingte Entzündungen, bei denen es bereits zu einer weitgehend irreversiblen Zerstörung von Teilen des Zahnhalteapparates bzw. des periimplantären Gewebes (Bindegewebe und Knochen) gekommen ist. Beide Krankheitsbilder weisen ähnliche Symptome auf und stellen sich klinisch u.a. durch positives Sondierungsbluten, Rubor, ödematöses Gewebe, Suppuration und Sondierungstiefen von mehr als 4 mm dar.15 Beide Erkrankungen werden durch bakterielle Plaque induziert, einem pathogenreichen Biofilm, der eine hohe Resistenz gegen lokale Therapiemaßnahmen aufweist. Der Verlauf beider Krankheiten ähnelt sich. Zunächst erfolgt eine Entzündung des parodontalen bzw. periimplantären Weichgewebes, im weiteren Verlauf setzen dann resorptive Prozesse des Hartgewebes ein.16–18 Insbesondere tiefe Taschen um Zähne oder Implantate begünstigen die Bildung von strukturierten pathogenen Biofilmen.18,19 Die Entzündungsneigung von Implantaten ist deutlich höher als die von gesunden Zähnen. Zudem verläuft die Entzündung der periimplantären Mukosa intensiver und der anschließende Übergriff auf periimplantäre Knochenstrukturen erfolgt schneller als bei einer Parodontitis.20,21
Aufgrund der zumeist schlechten Prognose einer Behandlung von Periimplantitiserkrankungen ist die frühzeitige Erkennung und Behandlung von periimplantären Entzündungen elementar für einen Langzeiterfolg von Implantaten.
Dekontaminationsstrategien
Grundbaustein eines erfolgreichen Behandlungskonzepts ist eine Dekontamination, also die gründliche Reinigung und Desinfektion der befallenen Areale.22,23
Es bieten sich verschiedene Verfahren an, wie z. B. Lasersysteme inklusive der Photodynamischen Therapie, Pulverstrahlverfahren sowie verschiedenste antimikrobielle Agentien – entweder als alleinige Dekontaminationsverfahren oder in verschiedensten Kombinationstherapien.24,25 Insbesondere antimikrobielle Agentien stellen eine vielversprechende und praktikable Option zur lokalen Dekontamination dar, da sie je nach Substanzklasse sowohl hochwirksam gegen Pathogene sind als auch kostengünstig in der Anwendung.24,25
Chloramine als wirksame Antiseptika
Chloramine (NCA) werden durch das Mischen einer Aminosäure- und einer Hypochloritlösung gebildet. Es ist bekannt, dass Hypochlorit alleine deutlich wirksamer zur Implantatdekontamination im Vergleich zu Standarddesinfektionsmitteln ist.26,27 Eine Verwendung in der Behandlung von periimplantären Entzündungen wird aber kritisch beurteilt, da Hypochlorit eine irritierende Wirkung auf das umliegende Gewebe aufweist, zumindest bei höheren Konzentrationen.28
NCA sind hochphysiologische Verbindungen, die eine wesentliche Rolle im natürlichen menschlichen Abwehrsystem spielen.29–31 Sie weisen wie Hypochlorit eine ausgeprägte antimikrobielle Wirksamkeit auf und bewirken so eine signifikante Inaktivierung sämtlicher Arten von Pathogenen. Im Gegensatz zu Hypochlorit, das aufgrund seiner unspezifischen Wirkweise sowohl auf gesunde als auch auf erkrankte Gewebearten einwirkt, wirken Chloramine (NCA) spezifisch auf degenerierte infizierte Gewebestrukturen sowie kurzkettige Proteine und Kohlenhydrate als potenzielle pathogene Stoffwechselprodukte, ohne wesentlichen Einfluss auf intakte Bindegewebestrukturen zu haben. Somit ist die Anwendung von Chloraminen als gewebeverträglich einzustufen.32
Die ausgeprägte antimikrobielle Wirkung von Chloraminen konnte in mehreren Untersuchungen im Vergleich zu den beiden häufig angewendeten intraoralen Desinfektionsmitteln, Chlorhexidin (CHX) sowie Wasserstoffperoxid, gezeigt werden. Hierbei zeigten sich Chloramine vorteilhaft gegenüber den etablierten Mitteln, insbesondere bei der Inaktivierung von Parodontalpathogenen bei niedrigen Desinfektionsmittelkonzentrationen sowie bei der Inaktivierung eines etablierten Biofilms.33,34 Bislang erfolgt der klinische Einsatz von Chloraminen vor allem bei der Behandlung persistierender entzündlicher Zahntaschen im Rahmen der unterstützenden Parodontitistherapie (UPT).35
Patientenfall 1
Das folgende Fallbeispiel zeigt exemplarisch die Verwendung eines Chloraminpräparats in der nichtchirurgischen Behandlung eines Furkationsdefektes.Der Patient präsentierte sich mit einer tiefen Tasche von 5 mm in Regio 26 (Abb. 1). Weiterhin konnte ein Furkationsdefekt Klasse II mit Sondierungsbluten als Zeichen der parodontalen Entzündung festgestellt werden (Abb. 2). Als Adjuvans zur Dekontamination wurde ein Chloraminpräparat verwendet (PERISOLV®, REGEDENT GmbH). Das Produkt ist ein Zwei-Komponentenpräparat, bestehend aus einer 0,95-prozentigen HClO-Lösung sowie einer Aminosäurelösung. Vor Gebrauch werden die beiden Komponenten gemischt. Dabei entstehen aus Hypochloriger Säure (HClO) sowie den Aminosäuren die kurzlebigen Chloramine (NCA) als aktive Substanzklasse. Zur initialen Dekontamination wurde das Chloraminpräparat in den Defekt appliziert (Abb. 3). Nach einer Einwirkzeit von circa 30 Sekunden erfolgte eine Kürettage mithilfe von Ultraschallinstrumenten (Abb. 4). Anschließend erfolgte eine zweite Applikation des Chloraminpräparats, gefolgt von einer Wurzelglättung (Abb. 5).
Die Reevaluation erfolgte nach sechs Monaten. Der Patient gab zu diesem Zeitpunkt keine Beschwerden an. Die Messung der Sondierungstiefe in Regio 26 ergab einen deutlich verbesserten Wert von 3 mm und eine Reduktion der Furkationsbeteiligung auf Klasse I (Abb. 6 und 7). Zudem waren keine Entzündungszeichen mehr feststellbar (BOP negativ).
Aufgrund der Materialeigenschaften und der positiven Ergebnisse bei der nichtchirurgischen Behandlung von tiefen Zahntaschen wird das Chloraminpräparat auch im Rahmen dekontaminierender Maßnahmen bei der Behandlung von periimplantären Entzündungen angewendet. Durch die antimikrobielle Eigenschaft, gepaart mit der degranulierenden Wirkung zur Verbesserung der Reinigungseffizienz, ist insbesondere die adjuvante Behandlung kontaminierter Implantatoberflächen in Kombination mit einer mechanischen Reinigung indiziert, entweder bei einer chirurgischen oder einer nichtchirurgischen Vorgehensweise.
Patientenfall 2
Das zweite Fallbeispiel zeigt exemplarisch die Vorgehensweise bei der Behandlung einer periimplantären Mukositis im Rahmen einer Implantat-Maintenance-Therapie.
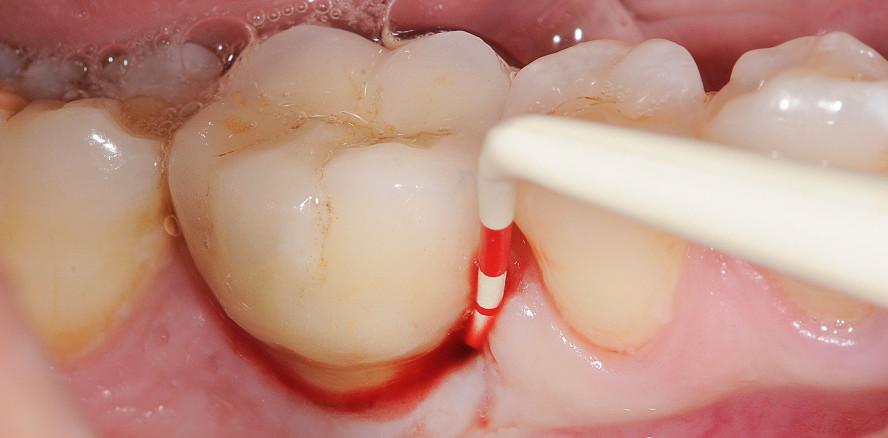
Der 33-jährige Patient (Nichtraucher) wurde zur Behandlung einer periimplantären Mukositis in Regio 46 überwiesen. Das Implantat 46 mit zementierter Restauration wies eine Sondierungstiefe von ≤ 5 mm mit deutlichen Entzündungszeichen im Sinne von Sondierungsblutung auf (BOP positiv; Abb. 8). Der Behandlungsplan beinhaltete zunächst eine initiale Antiinfektiöse Therapie (Full Mouth-Hygiene). Der Patient wurde über die Bedeutung der regelmäßigen und gründlichen Mundhygiene zur Beseitigung des Biofilms, als entscheidende Voraussetzung für den Therapieerfolg der Mukositisbehandlung und die gute entzündungsfreie Langzeitprognose des Implantats, sensibilisiert. Im Anschluss wurde ein subgingivales Debridement aller pathologisch auffälligen Zahntaschen durchgeführt. Zur Behandlung der periimplantären Mukositis wurde die Tasche um Implantat 46 mit dem zuvor aktivierten Präparat gefüllt (Abb. 9). Nach einer Einwirkzeit von 30 Sekunden erfolgte ein nichtchirurgisches mechanisches Debridement des Implantats durch einen Ultraschallscaler mit Kunststoffspitze (Abb. 10). Im Anschluss erfolgte eine zweite Applikation des Chloraminpräparats zur Optimierung der Dekontamination.
Die Reevaluation der antimikrobiellen Mukositisbehandlung erfolgte nach sechs Monaten (Abb. 11). Es zeigte sich eine absolut gesunde Situation in Regio 46 ohne Entzündungszeichen (BOP negativ). Es hatte sich zudem eine stabile Gewebemanschette eingestellt (Sondierungstiefe ≤ 4 mm).
Die vollständige Literaturliste gibt es hier.
Der Fachbeitrag ist im Implantologie Journal 3/2018 erschienen.