Oralchirurgie 31.03.2026
Chronische Trockenheit, chronische Leiden? Das Sjögren-Syndrom im Fokus
share
Epidemiologisch zählt das Sjögren-Syndrom weltweit zu den häufigsten systemischen Autoimmunerkrankungen. Die berichtete Prävalenz variiert jedoch aufgrund der sehr heterogenen Studienlage und der Studiendesigns in Diagnostik, Klassifikationskriterien und Versorgungsstrukturen.6, 8, 9
Die Gesamtprävalenz des Sjögren-Syndroms wird in europäischen Populationen auf bis zu 0,4 bis 0,6 Prozent geschätzt. Trotz der vergleichsweise hohen Prävalenz gilt das Sjögren-Syndrom weiterhin als deutlich unterdiagnostiziert.9, 10 Frühe Symptome wie Mundtrockenheit, trockene Augen oder unspezifische Fatigue werden von Betroffenen wie auch von Behandler/-innen häufig als altersbedingt, medikamentenassoziiert oder stressbedingt interpretiert und entsprechend nicht weiter abgeklärt.6, 11, 12 Mehrere Studien zeigen, je nach Studiendesign und Kohortengröße, dass zwischen dem Auftreten erster Symptome und der endgültigen Diagnosestellung im Mittel 3,1 bis 6,3 Jahre vergehen können.11, 13–16 Diese diagnostische Verzögerung betrifft sowohl das primäre als auch das sekundäre Sjögren-Syndrom und trägt wesentlich zur Krankheitslast sowie zur Entwicklung irreversibler Organmanifestationen bei.12, 14
Epidemiologisch charakteristisch ist eine ausgeprägte Geschlechtsdisposition mit einem Frauenanteil von bis zu 90 Prozent.17 Diese Geschlechterverteilung legt eine wesentliche Rolle hormoneller Faktoren, insbesondere östrogener Einflüsse, sowie geschlechtsspezifischer Unterschiede der Immunregulation nahe.18, 19
Der Erkrankungsgipfel liegt typischerweise im mittleren Erwachsenenalter zwischen dem 40. und 65. Lebensjahr.7, 17, 20 Gleichwohl sind auch juvenile Manifestationen beschrieben, was auf eine altersunabhängige pathogenetische Suszeptibilität hinweist.19, 21
Über die glanduläre Beteiligung hinaus handelt es sich beim Sjögren-Syndrom jedoch um eine systemische Erkrankung mit potenzieller Manifestation in nahezu allen Organsystemen. Nosologisch wird zwischen dem primären Sjögren-Syndrom und dem sekundären Sjögren-Syndrom unterschieden. Das primäre Sjögren-Syndrom tritt als eigenständige systemische Autoimmunerkrankung ohne begleitende Grunderkrankung auf. Demgegenüber entwickelt sich das sekundäre Sjögren-Syndrom im Kontext anderer systemischerAutoimmunerkrankungen, insbesondere der rheumatoiden Arthritis, des systemischen Lupus erythematodes oder der systemischen Sklerose.6, 22, 23 Beide Formen weisen ein ähnliches klinisches Beschwerdebild auf, unterscheiden sich jedoch hinsichtlich Begleiterkrankungen, diagnostischer Einordnung, prognostischer Aspekte sowie therapeutischer Strategien. Insbesondere das Ausmaß extraglandulärer Manifestationen und das Risiko lymphoproliferativer Erkrankungen variieren zwischen primärer und sekundärer Form.24
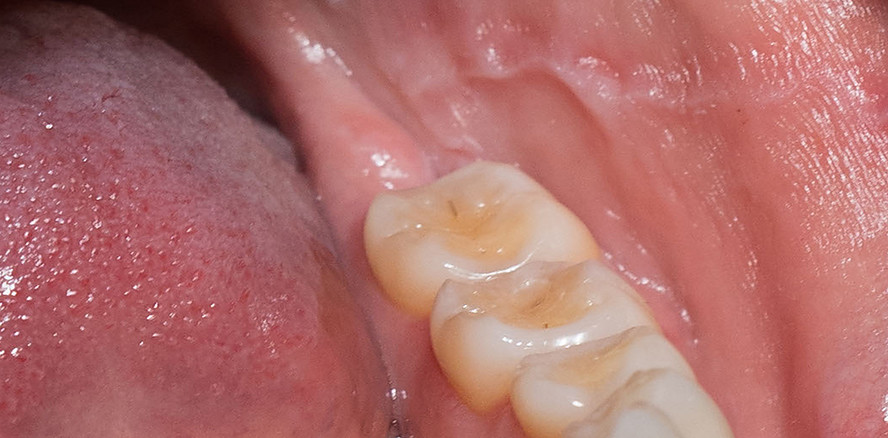
Die Auswirkungen des Sjögren-Syndroms auf die gesundheitsbezogene Lebensqualität sind erheblich.13 Neben der klassischen Sicca-Symptomatik entwickeln viele Patient/-innen systemische Manifestationen wie Arthralgien, Myalgien, neurologische Symptome oder pulmonale Beteiligungen.1, 6 Insbesondere die chronische Fatigue stellt eines der klinisch bedeutsamsten Symptome dar und ist mit einer hohen subjektiven Belastung für die Betroffenen verbunden. Sie ist signifikant mit funktionellen Einschränkungen im beruflichen, sozialen und psychischen Lebensbereich assoziiert.11, 25 Im oralen Bereich kann die persistierende Hyposalivation zu funktionellen Einschränkungen beim Sprechen, Kauen und Schlucken führen.26 Studien zeigen weiterhin ein deutlich erhöhtes Risiko für Karies, Parodontitis und entzündliche oder atrophische Veränderungen der oralen Schleimhäute.1, 24 Da diese Symptome häufig früh im Krankheitsverlauf auftreten, kommt insbesondere der Zahnmedizin und Oralmedizin eine Schlüsselrolle in der Früherkennung des Sjögren-Syndroms zu.6, 27
Pathogenese und Pathophysiologie des Sjögren-Syndroms
Die Pathogenese des Sjögren-Syndroms ist ein multifaktorielles Zusammenspiel. Es besteht eine komplexe Interaktion zwischen genetischen, umweltbedingten und immunologischen Faktoren, die in einer chronischen, autoimmun vermittelten Entzündung exokriner Drüsen, insbesondere der Speichel- und Tränendrüsen, resultieren.1, 6 Genetische Assoziationen umfassen HLA-Risikovarianten wie beispielsweise HLA-B8/DR328 sowie Polymorphismen in immunregulatorischen Genen wie IRF5 und STAT4, die mit einer verstärkten Typ-I-Interferonantwort in Verbindung stehen.29
Genetische Risikofaktoren, insbesondere Polymorphismen in Genen wie STAT-4 und ILT6, sowie HLA-Allele (zum Beispiel HLA-B8 und DR3) tragen zur Suszeptibilität bei,30 während potenzielle umweltbedingte Trigger chronische virale Infektionen umfassen.31 Glandutrope Viren wie das Epstein-Barr-Virus (EBV) sowie humane Retroviren werden beschrieben. Diese können eine initiale Schädigung des Drüsenepithels begünstigen.1, 32 Die genauen initiierenden Mechanismen sind jedoch noch nicht abschließend geklärt.
Ein zentrales pathogenetisches Konzept ist die sogenannte autoimmune Epitheliitis. Danach fungieren Epithelzellen der Speichel- und Tränendrüsen nicht nur als Zielstrukturen der Immunantwort, sondern übernehmen selbst eine aktive Rolle in der lokalen Immunmodulation unter anderem durch Antigenpräsentation sowie die Produktion proinflammatorischer Zytokine und Chemokine.33 Antigenpräsentierende Zellen, darunter plasmacytoide dendritische Zellen undMonozyten, erkennen solche Signale und fördern die Aktivierung des angeborenen Immunsystems. Dabei kommt es zu einer ausgeprägten Interferonaktivität (Typ-I und Typ-II, u. a. IFN-α und IFN-γ).34 Die charakteristische „Interferon-Signatur“ gilt als zentrales pathogenetisches Merkmal und trägt zur Chronifizierung der Entzündung bei.35, 36 Parallel werden proinflammatorische Zytokine (z. B. IL-12) sowie der B-Zell-aktivierende Faktor BAFF exprimiert, wodurch die adaptive Immunaktivierung weiter verstärkt wird.37 Im adaptiven Teil des Immunsystems differenzieren CD4⁺-T-Zellen u. a. zu Th1-, Th17- und Tfh-Zellen und perpetuieren die Entzündung über Zytokine wie IFN-γ, IL-17, IL-4, TNF-α und IL-1.33, 38 Diese Mikroumgebung fördert zugleich B-Zell-Aktivierung und -Expansion.
Die B-Zell-Hyperaktivität stellt ein weiteres Kernmerkmal des Sjögren-Syndroms dar. Unter dem Einfluss von B-cell activating factor (BAFF) und T-Zell-vermittelter Hilfe kommt es zur Autoantikörperproduktion (Anti-SSA/Ro- und Anti-SSB/LaAntikörper) und zur Ausbildung ektoper keimzentrumsähnlicher Strukturen in den Drüsen.37–39 Die lymphoiden Infiltrate tragen zur Gewebezerstörung und exokrinen Insuffizienz bei. Langfristig ist die persistierende B-Zell-Stimulation mit einem deutlich erhöhten Risiko für B-Zell-Non-Hodgkin-Lymphome, insbesondere vom MALT-Typ, assoziiert.39, 40 Histopathologisch zeigen sich fokale lymphozytäre Infiltrate (Abb. 3), die mit einer fortschreitenden Zerstörung des Drüsenparenchyms und einer Beeinträchtigung der sekretorischen Funktion einhergehen.41
Diagnostischer Algorithmus und Klassifikation des primären Sjögren-Syndroms
Im Folgenden wird der Fokus auf das primäre Sjögren-Syndrom gelegt, da orale Manifestationen häufig zu den frühesten und zugleich dominierenden Krankheitszeichen zählen. Zudem erfordert die Erkrankung interdisziplinär abgestimmte Präventions- und Therapiestrategien, um orale Folgeschäden zu minimieren und die Lebensqualität der Betroffenen langfristig zu erhalten.27, 28 Für die diagnostische Einordnung des primären Sjögren-Syndroms werden heute vor allem die American College of Rheumatology(ACR)/European League Against Rheumatism(EULAR)-Klassifikationskriterien (2016) herangezogen, die objektive Befunde in einem gewichteten Punktesystem zusammenführen und damit eine international vergleichbare Klassifikation erlauben.42 Ausgangspunkt des diagnostischen Vorgehens sind klinische Sicca-Symptome, insbesondere eine über mindestens drei Monate persistierende Mund- und/oder Augentrockenheit ohne hinreichende alternative Erklärung, die als klinische Screening-Konstellation gilt. Auf dieser Grundlage erfolgt eine stufenweise weiterführende Diagnostik, die objektive Funktionsuntersuchungen der exokrinen Drüsen, serologische Marker sowie histopathologische Verfahren umfasst.
Im Rahmen des Punktesystems werden objektive Funktionsparameter der exokrinen Drüsen berücksichtigt. Ein unstimulierter Gesamtspeichelfluss von ≤ 0,1 ml/min sowie ein pathologischer Schirmer-Test mit einer Benetzungsstrecke von ≤ 5 mm innerhalb von fünf Minuten an mindestens einem Auge werden jeweils mit einem Punkt gewertet.42
Darüber hinaus fließt ein pathologischer okularer Färbetest in die Bewertung ein, definiert durch einen Ocular Staining Score von ≥ 5 oder einen Van-Bijsterveld-Score von ≥ 4, der ebenfalls mit einem Punkt berücksichtigt wird. Höher gewichtet sind Anti-Ro/SSA-Autoantikörper (3 Punkte) sowie die Labialdrüsenbiopsie mit Nachweis einer fokalen lymphozytären Sialadenitis und Fokus-Score ≥ 1 Fokus pro 4 mm² (3 Punkte).42
Die histopathologische Einordnung erfolgt klassisch nach Chisholm und Mason.43 Histologisch gilt die fokale lymphozytäre Sialadenitis als klassifikationsrelevant, wenn der Fokus-Score mindestens 1 Fokus/4 mm² erreicht; ein Fokus entspricht dabei einem lymphozytären Zellaggregat von ≥ 50 Zellen.44 Insbesondere bei seronegativen Patient/-innen hat die Labialdrüsenbiopsie hohen diagnostischen Stellenwert und unterstützt die Klassifikationssicherung wesentlich. Die Klassifikation als primäres Sjögren-Syndrom wird bei einer Gesamtpunktzahl von ≥ 4 angewendet, nachdem Ein- und Ausschlusskriterien berücksichtigt wurden.44 Ausschlusskriterien umfassen unter anderem eine frühere Kopf-Hals-Radiatio, aktive Hepatitis-C-Infektion mit Virusreplikation, HIV/AIDS, Sarkoidose, Amyloidose, Graft-versus-Host-Erkrankung sowie IgG4-assoziierte Erkrankungen. Liegt eine dieser Konstellationen vor, erfolgt keine Klassifikation als primäres Sjögren-Syndrom, auch wenn einzelne Befunde positiv sind. Ergänzend empfehlen EULAR-basierte Ansätze eine organspezifische Diagnostik abhängig von Symptomatik und Krankheitsaktivität, strukturiert u. a. über den EULAR Sjögren’s Syndrome Disease Activity Index (ESSDAI45). Ziel ist die frühe Erfassung extraglandulärer Manifestationen und die rechtzeitige Identifikation schwerwiegender Komplikationen wie lymphoproliferativer Entwicklungen.45, 46
Differenzialdiagnosen beim primären Sjögren-Syndrom
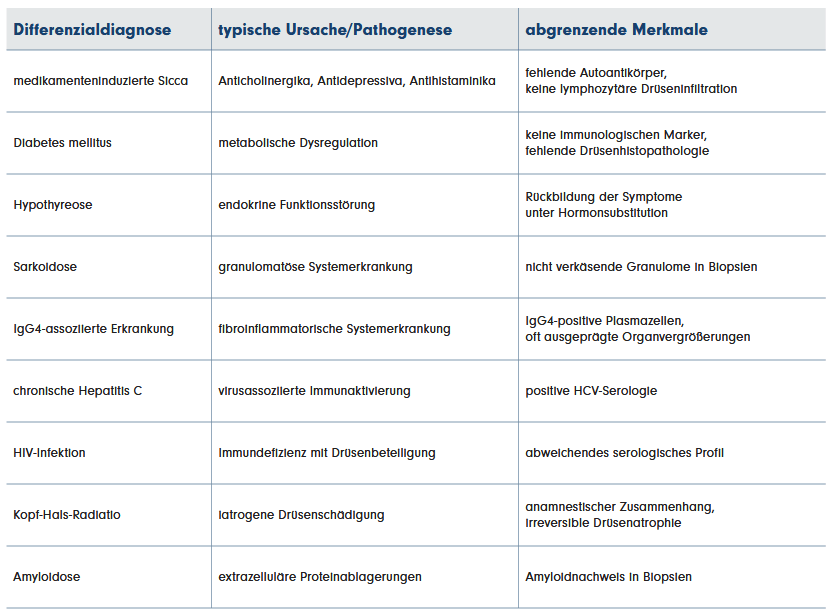
Die Diagnose erfordert eine strukturierte differenzialdiagnostische Abklärung, da Mund- und Augentrockenheit in der Allgemeinbevölkerung häufig sind und verschiedeneUrsachen haben können.47 Häufig sind medikamenteninduzierte Sicca-Syndrome (z. B. Antidepressiva, Anticholinergika, Antihypertensiva, Antihistaminika), bei denen typischerweise krankheitsspezifische Autoantikörper und histopathologische Zeichen einer lymphozytären Drüseninfiltration fehlen. Auch metabolisch-endokrine Erkrankungen wie Diabetes mellitus oder Hypothyreose können Sicca-Beschwerden verursachen, ohne dass ein Sjögren-typisches immunologisches Muster vorliegt.48 Weitere relevante Differenzialdiagnosen sind Sarkoidosen (histologisch nicht verkäsende Granulome) und IgG4-assoziierte Erkrankungen (IgG4-positive plasmazelluläre Infiltrate, häufig fibroinflammatorische Systembeteiligung).49 Infektiöse Ursachen, insbesondere chronische Hepatitis-C-Infektion, können ein Sjögren-ähnliches Syndrom verursachen; diese Konstellation ist in den ACR/EULAR-Kriterien explizit als Ausschlusskriterium definiert.42 Ebenso sind HIV-Infektionen, Amyloidose und strahleninduzierte Drüsenschäden nach Kopf-Hals-Therapie differenzialdiagnostisch relevant.44 Eine interdisziplinäre Zusammenarbeit ist besonders wichtig, um die Diagnosestellung zu ermöglichen.50 Zusammengefasst noch mal in Tabelle 1 dargestellt.
Organmanifestationen beim primären Sjögren-Syndrom
Je nach Kohorte entwickeln etwa 30 bis 50 Prozent der Betroffenen mit primärem Sjögren-Syndrom im Verlauf mindestens eine klinisch relevante Organbeteiligung.6, 51 Häufigbetroffen ist das muskuloskelettale System mit Arthralgien oder nicht erosiver, meist symmetrischer Arthritis, die klinisch an eine seronegative rheumatoide Arthritis erinnern kann, typischerweise jedoch ohne radiologische Destruktionen verläuft.52
Kutane Manifestationen reichen von trockener Haut und Raynaud-Symptomatik (Vasospasmus der Finger und Zehen) bis zu palpabler Purpura im Rahmen einer leukocyto-klastischen Vaskulitis. Letztere ist prognostisch bedeutsam und kann mit Kryoglobulinämie und erhöhtem Lymphomrisiko assoziiert sein.40
Pulmonale Manifestationen des Sjögren-Syndroms verlaufen häufig subklinisch und betreffen vor allem interstitielle Lungenerkrankungen, insbesondere die lymphozytäre interstitielle Pneumonie sowie die nichtspezifische interstitielle Pneumonie. Klinisch äußern sich diese Formen typischerweise durch chronischen Husten und belastungsabhängige Dyspnoe.53, 54
Renale Manifestationen betreffen überwiegend das tubulointerstitielle Kompartiment (chronische tubulointerstitielle Nephritis) mit möglicher distaler renal-tubulärer Azidose, Hypokaliämie oder Nephrokalzinose. Glomeruläre Erkrankungen sind seltener und häufiger mit Kryoglobulinämie verknüpft.55 Neurologisch treten v. a. periphere Neuropathien auf; zentrale Manifestationen sind seltener, aber klinisch relevant und diagnostisch anspruchsvoll.56
Von besonderer klinischer Relevanz ist das lymphoproliferative Risiko. Patient/-innen mit primärem Sjögren-Syndrom weisen ein erhöhtes Risiko für B-Zell-Non-Hodgkin-Lymphome auf, insbesondere extranodale Marginalzonenlymphome (MALT-Typ). Warnzeichen sind u. a. persistierende Parotisschwellungen, Lymphadenopathie, Splenomegalie, Purpura sowie serologische Risikomarker wie niedriges C4 odermonoklonale Gammopathie.37, 57 Aktivitätsscores wie der ESSDAI ermöglichen eine standardisierte Erfassung der Organbeteiligung und können zur Steuerung von Diagnostik und Therapie genutzt werden.45 Ergänzend dargestellt in Abbildung 4.
Die Bedeutung der rheumatologischenZusammenarbeit beim primären Sjögren-Syndrom
Aufgrund der variablen klinischen Manifestation ist das primäre Sjögren-Syndrom eine interdisziplinäre Versorgungsaufgabe. Während Sicca-Symptome häufig zuerst in Zahnmedizin, Augenheilkunde oder Hals-Nasen-Ohren-Heilkunde auffallen, liegt die Koordination von Diagnostik, Verlaufsbeurteilung und Systemtherapie typischerweise in der Hand der Rheumatologie.58 Rheumatologische Expertise ist insbesondere für die Interpretation komplexer serologischer Muster (Anti-SSA/Ro, Hypergammaglobulinämie, Hypokomplementämie, Kryoglobulinämie) bedeutsam, da diese nicht nur diagnostische Relevanz besitzen, sondern auch prognostische Hinweise auf etwaige Organbeteiligungen und Lymphomrisiko geben können.40 Im klinischen Alltag übernimmt die Rheumatologie zudem die strukturierte Aktivitätserfassung, u. a. über den ESSDAI.45 Eine weitere Kernaufgabe ist die Langzeitüberwachung einschließlich Lymphom-Risikokontrolle, bei der klinische Warnzeichen und serologische Veränderungen früh erkannt und abgeklärt werden müssen.59 Auch im Bereich klinischer Studien und translationaler Forschung sind rheumatologische Zentren zentrale Treiber neuer, zielgerichteter Therapiekonzepte.60 Für zahnmedizinische und mund-kiefer-gesichtschirurgische Kontexte ist die enge Anbindung an rheumatologische Strukturen besonders relevant, da orale Befunde Hinweise auf systemische Aktivität geben können und umgekehrt präventive orale Maßnahmen die Morbidität wesentlich beeinflussen.61
Therapieempfehlungen beim primären Sjögren-Syndrom
Die Behandlung ist überwiegend symptomorientiert und richtet sich nach Art und Ausmaß der Organbeteiligung. Die Empfehlungen umfassen einen gestuften Ansatz mit symptomatischer und systemischer Behandlung, wobei die Evidenzlage insgesamt begrenzt ist.62 Das Ziel ist, die Sicca-Beschwerden zu reduzieren, Organfunktionen zu erhalten und die Lebensqualität zu verbessern.6, 46
Bei Keratokonjunktivitis sicca bilden Patientenschulung und die Vermeidung austrocknender Medikamente die Basis; Tränenersatzmittel werden regelmäßig eingesetzt.46, 48 Die lokale Anwendung von Cyclosporin A hat sich seit einigen Jahren als sehr wirksam erwiesen und kann auch über lange Zeit durchgeführt werden.63 Zusätzlich kann auch ein zuerst temporärer und schließlich ein permanenter Verschluss der Tränenabflusswege durch die Applikation von sog. Punctum Plugs (Tränenwegsstöpsel) hilfreich sein. Die Behandlung führt dazu, dass die künstliche Tränenflüssigkeit über längere Zeit das Auge feucht hält.64
Bei Stomatitis sicca stehen neben der Reduktion xerostomiefördernder Medikation insbesondere konsequente Maßnahmen zur Kariesprophylaxe einschließlich regelmäßiger Fluoridierung im Vordergrund. Ergänzend können Speichelersatzpräparate sowie zuckerfreie Kaugummis zur Linderung der Symptomatik beitragen.46, 48 Die Elektrostimulation der Speicheldrüsen stellt einen experimentellen Therapieansatz dar, dessen klinische Wirksamkeit bislang nur durch eine begrenzte Evidenzbasis gestützt wird.65
Bei Rhinitis sicca werden primär lokal pflegende und befeuchtende Maßnahmen empfohlen; der Einsatz abschwellender Nasentropfen sollte aufgrund des Risikos einer Schleimhautschädigung vermieden werden.46 Bei überwiegend glandulärer Symptomatik stehen lokale Maßnahmen (Tränen- und Speichelersatz) sowie sekretagog wirksame Substanzen wie Pilocarpin im Vordergrund.66 Für Pilocarpin liegen randomisierte Studiendaten zur Symptomverbesserung vor, wobei cholinerge Nebenwirkungen (u. a. Schwitzen, Flush, Übelkeit) zu berücksichtigen sind.67
Bei geringer Krankheitsaktivität (bis zu 70 Prozent der Fälle) sind symptomatische Lokaltherapien und orale Medikamente ausreichend. Bei systemischen Manifestationen kommen je nach Schweregrad Glukokortikoide und konventionelle Immunsuppressiva (z. B. Methotrexat, Azathioprin, Mycophenolatmofetil) zum Einsatz.46 Hydroxychloroquin wird häufig bei Arthralgien verwendet, zeigt jedoch nur begrenzte Effekte auf Sicca-Symptome und Fatigue; wegen Retinopathierisiko sind ophthalmologische Kontrollen erforderlich. Eine klare Evidenz wird weiterhin diskutiert.6, 68 Grundsätzlich wird ein stufenweises, individuell angepasstes Vorgehen unter Berücksichtigung glandulärer und extraglandulärer Manifestationen empfohlen.46
Therapieausblick
Zielgerichtete Therapien für das Sjögren-Syndrom befinden sich in der Weiterentwicklung und stehen zunehmend im Fokus der wissenschaftlichen Forschung.60, 69 B-Zell-gerichtete Therapien, darunter Rituximab, haben inkonsistente Ergebnisse hinsichtlich der Verbesserung der glandulären Funktion gezeigt,70, 71 vereinzelt konnte allerdings Linderung der Symptome bei Patient/-innen mit primärem Sjögren-Syndrom zu frühen Zeitpunkten beschrieben werden.72 Neue therapeutische Strategien untersuchen zusätzlich multiple Zielstrukturen, darunter BAFF (Belimumab), T-Zell-Kostimulation (Abatacept) sowie neu entstehende Ansätze wie JAK-Inhibitoren.69, 73
Die Versorgung benötigt weiterhin einen interdisziplinären Ansatz unter Einbeziehung von Rheumatologie, Ophthalmologie, Zahnmedizin, Hals-Nasen-Ohren-Heilkunde, Nephrologie, Pneumologie und Neurologie. Zukünftige Fortschritte werden durch ein besseres Verständnis immunologischer Endotypen, Biomarker-Stratifizierung und fortgeschrittener Datenmethoden erwartet, um stärker personalisierte Therapiestrategien zu entwickeln.48, 69
Fazit
- Das Sjögren-Syndrom ist weit mehr als eine Erkrankung mit isolierter Mund- und Augentrockenheit. Die chronische Sicca-Symptomatik stellt häufig lediglich den sichtbaren Ausdruck einer systemischen Autoimmunerkrankung dar, die mit erheblichem Leidensdruck, eingeschränkter Lebensqualität und potenziell schwerwiegenden Organmanifestationen einhergeht. Insbesondere die Kombination aus chronischer Fatigue, extra-glandulärer Organbeteiligung und einer häufig jahrelangen diagnostischen Verzögerung prägt den Krankheitsverlauf maßgeblich.
- Die Prävalenz liegt bei 0,4 bis 0,6 Prozent der europäischen Bevölkerung und Frauen sind weitaus häufiger betroffen als Männer.74
- Eine frühzeitige und strukturierte Diagnostik anhand validierter Klassifikationskriterien ist entscheidend, um das Sjögren-Syndrom zuverlässig von anderen Ursachen der Sicca-Symptomatik abzugrenzen. Bei einer Verdachtsdiagnose sollte eine Überweisung zum Rheumatologen erfolgen. Aktivitätsscores wie der ESSDAI ermöglichen hierbei eine standardisierte Erfassung der systemischen Krankheitsaktivität und bilden eine wichtige Grundlage für die weitere Therapieplanung.
- Therapeutisch steht weiterhin eine symptom- und organspezifische Behandlung im Vordergrund. Durch konsequente lokale Maßnahmen, gezielte systemische Therapien bei Organbeteiligung sowie eine enge interdisziplinäre Zusammenarbeit lässt sich die Krankheitslast jedoch deutlich reduzieren.
- Perspektivisch eröffnen endotypbasierte, zielgerichtete Therapieansätze neue Möglichkeiten für eine individualisierte Behandlung.
Autoren: Nirina Götze, Dr. Claudia Sachse, Dr. Helena Bächer, Prof. Dr. Anna-Karina Maier, Prof. Dr. Susanne Nahles