Parodontologie 15.08.2016
Aggressive und chronische Parodontitis
share
Vorhersehbarer Zahnverlust oder Zahnerhalt durch ein individuelles Behandlungskonzept?
Die Behandlung von Patienten mit aggressiver (AgP) oder schwerer chronischer Parodontitis (CP) stellt für das Praxisteam eine therapeutische Herausforderung dar. Häufig wird Zähnen mit fortgeschrittenem Attachmentverlust bei AgP erst gar keine Chance gegeben und sie werden frühzeitig extrahiert. Oder es wird wiederholt versucht, rekurrierende akute parodontale Entzündungen mit lokalen Maßnahmen „in den Griff zu bekommen.“ Der Erfolg ist meist nur vorübergehend und die Behandlung endet später ebenfalls mit der Extraktion. Ohne ein geeignetes Behandlungskonzept bleibt, unabhängig von der Diagnose, ein langfristiger Therapieerfolg bei AgP und CP aus.
Parodontitisprävalenz und zahnärztliche Prävention
Die chronische Parodontitis ist eine der weltweit häufigsten chronischen Entzündungserkrankungen (Kassebaum et al., 2014), wobei das Erkrankungsrisiko mit dem Alter zunimmt und für Deutschland im Seniorenalter eine Prävalenz von über 70% angegeben wird (Holtfreter et al., 2009). Die AgP hingegen betrifft häufiger jüngere Patienten und die Prävalenz liegt in Europa bei 0,1 bis 0,3% (Saxen, 1980; Saxby, 1987). Bei Patienten mit afrikanischer Abstammung berichten Autoren aber von deutlich höheren Prävalenzraten von bis zu 2,5% (Susin et al., 2014).
Setzt man als allgemeinen Konsens voraus, dass das Ziel der zahnärztlichen Prävention ein Langzeiterhalt der natürlichen Bezahnung in einem gesunden, funktionellen, schmerzfreien und ästhetischen Zustand ist (Schweizerische Zahnärzte Gesellschaft, 2000), ergibt sich die Frage, warum eine frühzeitige adäquate Behandlung der Parodontitis häufig ausbleibt.
Lässt sich dies pauschal mit unterschiedlichen Erwartungen an die parodontale Erhaltungsfähigkeit von Zähnen erklären? Zweifellos kann nach dem Verlust strategisch wichtiger Zähne in Folge einer Parodontitis die Kaufähigkeit nur durch prothetische und/oder teils aufwendige implantatchirurgische Maßnahmen wiederhergestellt werden. Häufig führen diese dann aber infolge biologischer oder technischer Komplikationen zu weiteren Zahnverlusten und prothetischen Reparaturen und verursachen demzufolge hohe Folgekosten (Laurell et al., 1991; Pjetursson et al., 2004; Schmidlin et al., 2010; Bragger et al., 2011; Schwendicke et al., 2014; Schwendicke et al., 2016).
Früherkennung und präventive Behandlung der Parodontitis
Primäres Ziel muss deshalb ein frühzeitiger Therapiebeginn sein, denn beginnende parodontale Erkrankungen erfordern einen geringeren Therapieaufwand als fortgeschrittene und verursachen damit niedrigere Kosten. Auch wenn die während der letzten Jahrzehnte sinkende Anzahl von fehlenden Zähnen im Erwachsenenalter ermutigend ist (Micheelis und Bauch, 1999; Micheelis und Schiffner, 2006), scheint es dennoch nach wie vor ein erhebliches Verbesserungspotenzial zu geben. Studienergebnisse aus Skandinavien dokumentieren, dass mithilfe einer frühzeitigen präventiven Betreuung der Patienten erfolgreiche Zahnerhalte über 65 Jahre möglich sind (Schätzle et al., 2004). So fehlen den Senioren im direkten Vergleich mit der gleichen Altersgruppe in Deutschland nur halb so viele Zähne (König et al., 2010). Zusammengefasst hat in Skandinavien die Prävalenz der Parodontitis bei gleichzeitig besserer Mundhygiene und steigender Anzahl an erhaltenen Zähnen abgenommen (Skudutyte-Rysstad et al., 2007; Hugoson et al., 2008).
Eine wesentliche Rolle bei der Frage des Zahnerhaltes spielt die Prognose des weiteren Erkrankungsverlaufs. Dabei spielt das Ausmaß der Destruktion zu Beginn der Behandlung über weite Strecken nur eine untergeordnete Rolle. Sie bedingt den Aufwand der Therapie, aber nicht notwendigerweise ihren Ausgang. Erst während des Verlaufs der unterstützenden Parodontitistherapie (UPT) nach erfolgreichem Abschluss der aktiven Therapiephase kann eine zuverlässige prognostische Einschätzung der Erhaltungsmöglichkeiten im Rahmen einer Reevaluation erfolgen. Dadurch können auch im parodontal kompromittierten Gebiss hohe Überlebensraten nachfolgender prothetischer Versorgungen erreicht werden (Graetz et al., 2013b). Allerdings ist nicht nur die Mundhygiene relevant. Interaktionen der Parodontitis mit anderen Erkrankungen, wie beispielsweise Diabetes mellitus, beeinflussen die Prävalenz und den Schweregrad der parodontalen Entzündung (Taylor et al., 1996; Khader et al., 2006; Preshaw et al., 2012) ebenso wie das Rauchen (Chambrone et al., 2010) und können somit weitere Zahnverluste bedingen (Faggion et al., 2007).
Um auch in Deutschland zu einem (mehr) präventiven Behandlungskonzept zu finden, sollten erste Anzeichen parodontaler Veränderungen durch ein parodontales Screening frühzeitig erkannt werden. Insbesondere die klinische Diagnostik mit der parodontalen Sonde stellt hier eine wirksame Methode dar. Eine aktuelle Übersichtsarbeit beschreibt eindeutig, dass Parodontitis keine „leise“ Erkrankung ist, d.h. nicht ohne klinische Anzeichen verläuft (Buset et al., 2016). Ein zeitsparendes und effektives Mittel zur Früherkennung ist der Parodontale Screening Index (PSI), dessen Ergebnis auf einen bestimmten Grad der Behandlungsbedürftigkeit hinweist. Auch wenn nach dem einheitlichen Bewertungsmaßstab für zahnärztliche Leistungen (BEMA) der PSI nur alle zwei Jahre abgerechnet werden darf, sollte dieser Schnelltest insbesondere bei Patienten mit erhöhtem Risiko für parodontale Erkrankungen häufiger durchgeführt werden.
Allerdings ist zu beachten, dass es sich beim PSI tatsächlich um ein Screening handelt. Schlägt er an, ist eine umfassende parodontale Diagnostik erforderlich. Erst durch sie kann die Diagnose einer Parodontitis gestellt werden. Daraus ergibt sich auch, dass der PSI ungeeignet zur Feststellung des Erkrankungszustandes bzw. zur Verlaufsbeobachtung und Erkennung von Rezidiven bei Patienten ist (Eickholz, 2010a), bei denen bereits eine parodontale Erkrankung festgestellt wurde oder die sich in der UPT befinden. In diesem Falle muss eine vollständige parodontale Diagnostik erfolgen (Eickholz, 2007a).
Zusätzliches diagnostisches Hilfsmittel können Röntgenbilder sein. Selbst Bissflügelaufnahmen, die im Zuge einer Kariesdiagnostik bei jungen Patienten von Zeit zu Zeit angefertigt werden, können eine beginnende AgP bereits frühzeitig aufdecken (Cogen et al., 1992; Sjodin et al., 1993). Gerade für eine solch lokalisierte Erkrankungsform, bei welcher häufig die Inzisiven und ersten Molaren zuerst betroffen sind (Lang et al., 1999), sollte grundsätzlich eine Beurteilung des Verlaufs des Limbus alveolaris erfolgen. Neben einer familiären Häufung der Parodontalerkrankung und ein außer der Parodontitis klinisch gesunder Patient gilt insbesondere das rasche Voranschreiten der parodontalen Destruktion als primäres Kennzeichen der AgP (Armitage, 1999; Lang et al., 1999). Diese drei Hauptmerkmale wirken insgesamt leicht beurteilbar, jedoch kann beispielsweise bereits die Definition „schnelle Progression“ Fragen aufwerfen. Fortgeschrittene Destruktionen bei Jugendlichen und jungen Erwachsenen bis 20 Jahre lassen auf eine rasche Progression schließen, wenn man annimmt, dass die Erkrankung in der Pubertät begann. Aber wie bewertet man die Situation bei einem 40-Jährigen? Hat die Destruktion im Alter von 20 Jahren begonnen, so kann man eine langsame Progression annehmen und es handelt sich eher um eine schwere CP. Dagegen könnte die Erkrankung auch erst einige Jahre zuvor begonnen haben und damit sehr rasch verlaufen sein.
Aktive Parodontitistherapie im fortgeschrittenen Erkrankungsstadium
Grundsätzlich gibt es in Abhängigkeit der beiden Diagnosen „aggressive“ oder „chronische Parodontitis“ keine Unterschiede im Therapieansatz, was anhand eines stufenartigen Therapieschemas der Klinik für Zahnerhaltung und Parodontologie in Kiel erläutert werden soll. Hierbei erfolgen in der Hygienephase eine individuelle Instruktion und Motivation des Patienten zur Mundhygiene mit einem Schwerpunkt auf der Interdentalraumpflege sowie professionelle Zahnreinigungen (PZR). Die antiinfektiöse Parodontitistherapie umfasst ein nichtchirurgisches Debridement der Wurzeloberflächen aller erkrankten, erhaltungsfähigen Zähne mit Sondierungstiefen (ST) ≥ 4mm. Bei sehr schweren Verlaufsformen der AgP und CP kann die mechanische antiinfektiöse Therapie mit einer unterstützenden systemischen Antibiose kombiniert werden. In der Regel kann aber auch bei AgP und schwerer CP zuerst rein mechanisch antiinfektiös, entsprechend des Konzeptes der Universität Göteborg, behandelt werden (Schaller, 2016).
Bei mangelndem Therapieerfolg der mechanischen Behandlung bzw. einem Fortschreiten der Parodontitis trotz adäquater Therapie wird grundsätzlich eine erneute gründliche Analyse der Risikofaktoren, wie z.B. Rauchen, hohe Plaque-Scores oder Blutzuckerspiegel, vorgenommen und in einem Patientengespräch diskutiert, um ggf. auf das Patientenverhalten noch intensiver einzuwirken. Insbesondere bei Vorliegen mehrerer ungünstiger Faktoren ist der zusätzliche Nutzen einer unterstützenden systemischen Antibiose neben der reinen mechanischen Therapie fraglich (Harks et al., 2015). Kurzfristig kann aber gerade der adjuvante systemische Einsatz von Antibiotika bessere klinische Erfolge in Kombination mit geschlossenem Vorgehen ergeben und das Ausmaß parodontalchirurgischer Maßnahmen dadurch ggf. verringern (Mestnik et al., 2010; Mombelli et al., 2011).
Reevaluation der aktiven Parodontitistherapiephase
Optional können zwischen antiinfektiöser Therapie und Reevaluation Kontrolltermine zur Überwachung der häuslichen Mundhygiene und PZR vereinbart werden. Drei Monate nach geschlossener Therapie schließt sich eine erste Reevaluation an. Zähne mit verbleibenden, gut zugänglichen Taschen von ≥ 5 mm Sondierungstiefe (ST) z.B. an einwurzeligen Zähnen können ggf. erneut subgingival gereinigt werden. An Lokalisationen, die bei der ersten Reevaluation Grenzwerte von 6 mm mit fehlenden Entzündungszeichen aufweisen, initial aber sehr hohe ST zeigten, kann der Therapieentscheid zum offenen parodontalchirurgischem Vorgehen auch länger herausgezögert werden (Schlagenhauf, 2013). Hingegen unverändert tiefe Taschen bzw. Taschen mit Entzündungszeichen an schwer zugänglichen Stellen wie Furkationen oder unterminierenden infraalveolären Defekten werden einer offenen Parodontalbehandlung zugeführt. In der korrektiven Phase können dann bei Bedarf zusätzlich zu einer offenen Therapie regenerative oder resektive Verfahren zur Therapie von geeigneten Knochentaschen und/oder mehrwurzeligen Zähnen Anwendung finden.
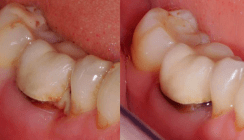
Je nach Ausmaß der parodontalen Destruktionen, der Höhe der initialen ST und Art der gewählten Behandlungsmaßnahmen kann die parodontale Heilung unterschiedlich lange Zeit in Anspruch nehmen. Bei mäßig tiefen Taschen und gleichförmigem Knochenabbau können die parodontalen Gewebe bereits nach wenigen Monaten ausgeheilt sein. Bei ausgedehnten infraalveolären Defekten dagegen kann die knöcherne Ausheilung auch über einen Zeitraum von sechs Monaten hinaus andauern. Deshalb sollte eine prothetische Rehabilitation nach abschließender Reevaluation frühestens circa drei bis zwölf Monate nach aktiver Parodontitistherapie geplant und umgesetzt werden. Unabhängig davon muss während des Heilungsverlaufs eine regelmäßige Überwachung der Mundhygiene in dreimonatigen Abständen gewährleistet werden. Gerade bei Fällen mit generalisiertem, weit fortgeschrittenem Attachmentverlust wird möglichst das Konzept der geschlossenen Zahnreihe angestrebt, um prothetischen Behandlungsbedarf zu vermeiden. Molaren mit fortgeschrittenem Furkationsbefall und verbleibenden hohen ST, die der Mundhygiene unzugänglich sind, können bei anatomisch günstigen Voraussetzungen durch Radektomie häufig in einen parodontal stabileren Zustand überführt werden (Eickholz, 2010b). Ziel ist es, entweder bereits vorhandenen Zahnersatz damit zu stabilisieren (Abb. 1c), oder eine verkürzte Zahnreihe bzw. Folgeextraktionen aufgrund ungenügender Pfeilerqualität der Nachbarzähne zu verhindern.
Inhalte und Struktur der unterstützenden Parodontitistherapiephase (UPT)
Nur die regelmäßige Teilnahme an einer systematischen UPT kann den Langzeiterfolg jeglicher parodontalen Therapie sichern (Axelsson und Lindhe, 1981; König et al., 2001). Das individuelle Recallintervall sollte erstmalig nach abschließender Reevaluation der aktiven Behandlungsphase festgelegt werden und kann zwischen drei und zwölf Monaten variieren. Zu den Inhalten der Nachsorgesitzungen gehören neben der Erfassung des gingivalen Entzündungszustandes (z.B. Bluten auf Sondieren – BOP), der Effektivität der häuslichen Mundhygiene (z.B. Plaque-Controll-Record – PCR) mit anschließender Mundhygieneinstruktion (Schwerpunkt Interdentalraumpflege) auch eine schonende, auf die Entfernung des Biofilms zielende professionelle Zahnreinigung mit subgingivaler Instrumentierung der Wurzeloberflächen bei ST ≥ 4 mm mit BOP und/oder ≥ 5 mm ohne BOP. Abschließend erfolgt die Politur aller Glattflächen (z.B. Napf/Paste) und interdental (z.B. mit EVA-System/Spirex). Alternativ kann heute das reine Biofilmmanagement auch mit niedrig-abrasiven Pulvern und einem entsprechendem Pulver-Wasser-Strahlgerät erfolgen, was zeitsparend, zahnhartsubstanzschonender und compliance-fördernd zu sein scheint (Sculean et al., 2013; Bastendorf, 2015). Abschließend werden alle freiliegenden Wurzeloberflächen fluoridiert.
Mindestens einmal im Jahr erfolgt die Erhebung des Zahnstatus einschließlich der ST, besser noch des Attachmentlevels und der Furkationsbeteiligung. Zahnflächen mit erhöhtem Risiko zu fortschreitenden Destruktionen sollten aber häufiger kontrolliert werden! Nur so kann gewährleistet werden, dass Rezidive frühzeitig erkannt und adäquate therapeutische Maßnahmen eingeleitet werden. Wiederkehrende Entzündungen können mit therapeutischen Maßnahmen wie der alleinigen Instrumentierung oder in Kombination mit lokaler bzw. systemischer Applikation von Antibiotika und/oder parodontalchirurgischen Eingriffen behandelt werden. Eine regelmäßige Risikobeurteilung zur Vermeidung einer Progression und folgender Zahnverluste hilft bei der Strukturierung der UPT. Ein valides Mittel sowohl für die AgP als auch die CP stellt die Risikoprofilanalyse nach Lang und Tonetti (2003) dar. Diese Systeme können aber nie zu 100 Prozent sicher sein (Eickholz, 2007b), da es immer noch unbekannte oder nicht vollständig verstandene Variablen wie z.B. psychosoziale Einflüsse (Graetz et al., 2013a) in der Ätiologie und Pathogenese der Parodontitis gibt. Trotzdem helfen diese Analysen, Patienten mit hohem Behandlungsbedarf von denen mit niedrigem Behandlungsbedarf zu unterscheiden und damit Behandlungszeiten in der Praxis sinnvoll zu planen.
Chancen und Grenzen der Parodontitistherapie
Unabhängig von der Diagnose „chronische“ oder „aggressive Parodontitis“ – gute Erfolgsaussichten bestehen bei konsequenter Therapie und Nachsorge für beide Erkrankungsformen. Durch eine lebenslange und individuell angepasste Kontrolle des dentalen Biofilms ist es möglich, den parodontalen Zustand zu stabilisieren bzw. zumindest die Progression der Erkrankung deutlich zu verzögern (Abb. 1 und 2). Somit ist in den meisten Fällen ein Zahnverlust nach Parodontitistherapie unter der Voraussetzung einer regelmäßigen UPT ein eher seltenes Ereignis mit rund 0,1 Zahn/Jahr über einen Untersuchungszeitraum von 10 Jahren (Chambrone et al., 2010; Nibali et al., 2013). Selbst bei Patienten mit fortgeschrittener AgP oder CP werden Überlebensraten der Zähne von 60 bis 97 Prozent innerhalb von einem Jahrzehnt beschrieben (Kamma und Baehni, 2003; Pretzl et al., 2008; Mros und Berglundh, 2010; Bäumer et al., 2011; Graetz et al., 2011). Für jegliche parodontale Behandlungsstrategie gilt jedoch: Je jünger die Patienten und je lokalisierter die Destruktion initial ist, insbesondere bei AgP, umso höher sind die Erfolgsaussichten (Merchant et al., 2014).
Es zeigen sich also bei beiden Parodontitisformen ähnlich gute Erfolgsaussichten hinsichtlich eines Zahnerhaltes, welche keinesfalls schlechter sind als die heutigen Überlebenswahrscheinlichkeiten von Implantaten (Karoussis et al., 2003; Roos-Jansaker et al., 2006a; Roos-Jansaker et al., 2006b; Roos-Jansaker et al., 2006c; Ong et al., 2008; Matarasso et al., 2010). Damit ist es strategisch sinnvoll, zunächst eine Parodontitisbehandlung durchzuführen, Zähne zu erhalten und eine Implantation so weit wie möglich hinauszuzögern bzw. ganz zu vermeiden (Nyman und Lindhe, 1976, Yi et al., 1995, Tan et al., 2004). Eine frühzeitige Extraktion parodontal geschädigter Zähne mit anschließender Implantation und entsprechendem Nachsorgeprogramm ist nach aktuellen Kosten-Nutzen-Analysen langfristig die teurere und weniger nachhaltige Alternative gegenüber dem beschriebenen Zahnerhaltungsversuch (Schwendicke et al., 2014; Schwendicke et al., 2016).
Konklusion
Der Früherkennung parodontaler Erkrankungen kommt eine besondere Bedeutung zu, da sowohl die chronische als auch die aggressive Parodontitis erfolgreich therapiert werden können, insbesondere wenn frühzeitig geeignete Behandlungsschritte eingeleitet werden. Dagegen ist in fortgeschrittenen Fällen bei Patienten mit Risikofaktoren die Therapie bei generalisierten aggressiven und chronischen Verlaufsformen der Parodontitis deutlich aufwendiger. Eine zeitnahe adäquate systematische Parodontitistherapie mit anschließender regelmäßiger professioneller Betreuung in einer UPT ermöglicht dennoch gute Langzeitergebnisse, unabhängig ob eine AgP oder CP vorliegt.
Danksagung
Die Autoren danken allen ehemaligen Mitarbeitern der Abteilung, insbesondere den ehemaligen Leitern Herrn Prof. H. C. Plagmann und Herrn Dr. A. Rühling für die Behandlung der langzeitdokumentierten Patienten und Etablierung der wissenschaftlichen Datenbank Parodat.
Weitere Autoren: Anna Plaumann, Konstantin Gomer und Dr. Sonja Sälzer.