Implantologie 07.09.2023
Autologes Blutkonzentrat PRF im Weichgewebsmanagement
share
Der Verlust eines Zahnes bedeutet für den Patienten in der Regel nicht nur eine funktionelle, sondern auch eine ästhetische Einschränkung. Um dies zu kompensieren und sowohl Funktionalität als auch Ästhetik bestmöglich wiederherzustellen, ist eine Versorgung mit einem Zahnimplantat die ideale Lösung. Für die Patienten stellt dies in der Regel die komfortabelste und bevorzugte Methode der Wiederherstellung dar.
Damit eine Implantatversorgung erfolgreich durchgeführt und zudem eine vernünftige Osseointegration und ein Langzeitüberleben des Implantats ermöglicht werden kann, sind einige biologische, biomechanische und klinische Vorrausetzungen nötig. Ein nicht zu vernachlässigender Aspekt ist ein effizientes Weichgewebsmanagement. Der Einsatz von autologem Blutkonzentraten wie PRF (Platelet Rich Fibrin) kann in Bezug auf die Weichgewebsheilung als Promotor der sekundären Wundheilungskaskade fungieren und so unterstützend dafür sorgen, dass ein suffizientes Weichgewebe für eine erfolgreiche Implantation regeneriert wird.
Hintergrund
Die moderne Implantologie hat in den vergangenen Jahren dank neuer Innovationen und optimierter Behandlungsansätze enorme Fortschritte gemacht. Mittlerweile wird eine implantatgetragene prothetische Versorgung gern der konventionellen Versorgung vorgezogen, sofern es technisch realisierbar und für die Patienten finanziell leistbar ist. Innovationen wurden dabei nicht nur auf Implantatseite, wie die Entwicklung unterschiedlicher Implantatformen (zylindrisch, gerade oder konisch), besonderer Implantatlängen oder auch in Hinblick auf den Abschluss mit dem umgebenden Gewebe – Bone Level vs. Tissue Level – gemacht.1–4 Auch auf Materialseite wurden Implantatsysteme immer weiter, entwickelt – Titaniumimplantate mit speziellen Oberflächenmodifikationen oder Keramikimplantaten.5 Auch wenn die Charakteristika eines Implantats ausschlaggebend für die erfolgreiche Implantation und das Langzeitüberleben des Implantats sein können, so kommt es letztendlich auch auf das zur Verfügung stehende Gewebeangebot im geplanten Implantationsgebiet, die Implantationstechnik sowie auch gegebenenfalls begleitende Augmentationen an.6, 7 Ein ausreichendes Knochen- und Weichgewebsangebot ist unerlässlich für eine erfolgreiche Implantation (Abb. 1). Ausschlaggebend ist dabei nicht nur, dass ausreichend Gewebe zur Verfügung steht, sondern auch welche Qualität diese hat. Bei einer geplanten Implantatversorgung nach Extraktion eines nichterhaltungswürdigen Zahnes wird daher in der modernen Zahnmedizin auf regenerativ unterstützende Verfahren, wie die Socket bzw. Ridge Preservation unter Zuhilfenahme von entsprechendem Gewebeersatzmaterial, gesetzt.8, 9
Der Einsatz von Biomaterialien verschiedener Ursprünge, wie allogenes, xenogenes, synthetisches oder sogar phykogenes Material, zur Füllung der Extraktionsalveole wird häufig in Kombination mit einer Weichgewebsersatzmembran, z. B. aus Kollagen, verwendet. Dies dient nicht nur der Unterstützung der Regeneration im Rahmen einer Guided Bone Regeneration (GBR), sondern auch der Stabilisierung und Erhaltung des vorhandenen Knochenangebots.
Nach wie vor scheint der Fokus bei der Geweberegeneration in Zusammenhang mit einer geplanten Implantation vorrangig auf dem Knochengewebe zu liegen. Dabei stellt das Weichgewebe, das später das Implantat umgibt, einen nicht zu vernachlässigenden kritischen Faktor dar. Dies betrifft sowohl die finale Ästhetik als auch die Funktionalität und das langfristige komplikationsfreie Implantatüberleben.10, 11
Ist kein ausreichendes Weichgewebsangebot bei der Implantation vorhanden, erhöht sich das Risiko für unerwünschte Komplikationen, die gegebenenfalls zum Implantatverlust führen können. Zudem führt es zu einem minderwertigen ästhetischen Outcome und zu der Notwendigkeit weiterer Eingriffe, um vorhandene Defizite auszugleichen. Je später im Behandlungsschema Maßnahmen getroffen werden, um Weichgewebsdefizite auszugleichen, desto höher ist das Risiko für Komplikationen. Ein effizientes Weichgewebsmanagement in die Implantationsplanung zu integrieren, kann daher entscheidend zum funktionellen und ästhetischen Erfolg der Prozedur beitragen.11 Idealerweise sollten daher bereits am Anfang nach der Zahnextraktion Maßnahmen zur Unterstützung der Geweberegeneration einschließlich des Weichgewebes getroffen werden. Erreicht werden kann dies, wenn bei der Socket bzw. Ridge Preservation auch Biomaterialien für die gestützte Weichgewebsregeneration getroffen werden – Guided Tissue Regeneration (GTR). Auch hier kommen Biomaterialien verschiedenen Ursprungs infrage. Häufig werden natürliche polymerbasierte Biomaterialien wie z. B. Kollagenmembranen zur Abdeckung des Knochenersatzmaterials und damit auch des Defektareals per se eingesetzt.12 Es kommen aber auch synthetische Materialien zum Einsatz.13 Auch wenn der Nutzen unbestritten vorhanden ist, so haben doch alle nicht-autologen Materialien den entscheidenden Nachteil, dass sie – bedingt durch die notwendigen Herstellungsschritte – biologisch inert sind. Es sind keine aktiven biologischen Komponenten in Form von Gewebevorläuferzellen oder wichtige wachstumsfaktorfreisetzender Immunzellen, wie sie im autologen Gewebe üblicherweise vorkommen und die Geweberegeneration aktiv zu unterstützen, inkludiert. Zwar kommen durch das passive oder aktive Benetzen mit dem patienteneigenen Blut körpereigene Zellen auf bzw. in die Membran und stellen somit die erste Basis für die Regeneration dar, jedoch sind diese nur in geringer Dichte vorhanden. Eine Möglichkeit, eine biologisch aktive Membran für die Weichgeweberegeneration zu gewinnen, ist die Verwendung von aus autologen Blutkonzentrat hergestellten festen PRF (Platelet Rich Fibrin) Matrices, die zu einer Membran gepresst werden.
Merke
- Verschiedene Faktoren haben Einfluss auf den Implantationserfolg und das langfristige Implantatüberleben: das Implantat selbst, das gewählte Implantationsverfahren sowie die Gegebenheiten an der Implantationsposition per se.
- Das Weichgewebemanagement darf nicht vernachlässigt werden.
Autologe Blutkonzentrate
Unter autologen Blutkonzentraten fasst man die aus patienteneigenem Blut durch spezifische Zentrifugationsprotokolle gewonnen Matrices zusammen, in denen durch die Zentrifugation bestimmte periphere Blutzellen und/oder im Blut enthaltene Wachstumsfaktoren aufkonzentriert werden. Autologe Blutkonzentrate werden bereits seit vielen Jahren intensiv erforscht und kommen in der Medizin zum Einsatz – verstärkt auch in den letzten Jahren in der Zahnmedizin. Einer der bekanntesten Vertreter ist zum Beispiel das Platelet Rich Plasma (PRP), bei dessen Herstellung, wie der Name schon sagt, die Aufkonzentration von Thrombozyten (engl.: Platelets) im Vordergrund steht.14 Weitere Vertreter sind Plasma Rich in Growth Factors (PRGF), dessen Herstellungsprotokoll auf erhöhte Wachstumsfaktorkonzentrationen abzielt, oder auch Leucocyte- and Platelet Rich Plasma (L-PRP), das eine Weiterentwicklung des PRPs durch zusätzlichen Fokus auf die Aufkonzentration von Leukozyten darstellt.15, 16 Einer der jüngeren Vertreter der autologen Blutkonzentrate stellt das Platelet Rich Fibrin (PRF) dar, in dem eine hohe Konzentration von Thrombozyten, aber auch anderen Komponenten, in einer Fibrinmatrix zu finden ist.17 Allen Blutkonzentraten ist dabei gemein, dass sie aus patienteneigenem Blut, das im Rahmen einer üblichen Blutabnahme gewonnen wird, und einem spezifischen Zentrifugationsprotokoll gewonnen werden. Die Herstellungsprotokolle variieren jedoch erheblich voneinander: es kommen deutlich unterschiedliche Zentrifugationsprotokolle zum Einsatz, die sich in der Anzahl der Zentrifugationsschritte, wie auch in den Zentrifugationsparametern an sich unterscheiden. Darüber hinaus können je nach Blutkonzentrattyp auch der Zusatz von weiteren Agentien wie Antikoagulantien zum Einsatz kommen.18 Auch wenn alle Varianten gemeinsam haben, dass es sich um ein autologes Produkt, um nicht zu sagen Biomaterial, handelt, das die elegante Eigenschaft hat, dass keine unerwünschten Abstoßungs- oder sogar allergische Reaktionen zu erwarten sind und somit einen hohen Grad an Sicherheit für den Einsatz bietet, so kann ein solches, je nachdem wie komplex und/oder zeitaufwendig ein Herstellungsprotokoll ist, geeigneter oder ungeeigneter es für den Einsatz in der täglichen Praxis sein.
Merke
- Autologe Blutkonzentrate werden über spezifische Zentrifugationsprotokolle aus patienteneigenem peripherem Blut hergestellt.
- Je nach Blutkonzentratvariante sollen unterschiedliche Komponenten aufkonzentriert werden.
Platelet Rich Fibrin (PRF)
Ein mittlerweile sehr bekannter Vertreter der autologen Blutkonzentrate stellt das PRF dar. Dieses zeichnet sich durch ein einfaches Ein-Schritt-Zentrifugationsprotokoll und das Fehlen von zusätzlichen Additiven aus. Ziel dieses von Choukroun et al. in 2006 entwickelten autologen Blutkonzentrates ist es, eine Fibrinmatrix zu generieren, die reich an Thrombozyten und damit einhergehend an den von Thrombozyten freigesetzten Wachstumsfaktoren ist.17, 19–22 Sowohl PRF wie auch die zuvor genannten autologen Blutkonzentrate wurden über die Jahre weiterentwickelt. Es wurde eine leukozytenreiche Variante, das L-PRF, entwickelt und eine flüssige Variante, das sogenannte injectable PRF (i-PRF).23, 24
Eine wichtige Weiterentwicklung insbesondere für die Vergleichbarkeit in der klinischen Forschung stellt die Einführung des sogenannten Low Speed Centrifugations Concepts LSCC im Zusammenhang mit PRF dar.25
Die stetige Weiterentwicklung der Blutkonzentrate und insbesondere des PRFs hat dazu geführt, dass PRF nicht gleich PRF gesetzt werden kann. In der Literatur publizierte Daten zu klinischen Studien und Fallserien zeigen oft uneinheitliche Zentrifugationsprotokolle in Hinblick auf die verwendete Zentrifugalkraft (relative centrifugal force RCF) und -dauer. Problematisch dabei ist, dass Veränderungen dieser Parameter zu einer unterschiedlichen Struktur und zellulären Zusammensetzung des finalen PRFs führen.26 Entsprechend beeinflusst wird auch der für die Geweberegeneration und -antwort besonders relevante Wachstumsfaktorgehalt.27 Durch die unterschiedlichen Herstellungsprotokolle entstehen auch mutmaßlich unterschiedliche PRF-Varianten unterschiedlicher zellulärer und nicht zellulärer Zusammensetzung. Die Wahrscheinlichkeit ist sehr hoch, dass diese Unterschiede auch zu unterschiedlichen Einflüssen bei den verschiedenen klinischen Indikationen führen können. Die Einführung des systematischen LSCC-Herstellungsprotokolls für PRF, bei der mit konstanten Blutmengen, konstanter Zentrifugationsdauer, aber definiert unterschiedlicher Zentrifugalkraft (RCF) gearbeitet wird, erlaubt den systematischen Vergleich innerhalb der LSCC-PRF-Varianten (PRF-high: 710 xg, PRF-medium: 177 xg, PRF-low: 44 xg), aber auch innerhalb einer PRF-Variante die systematische Untersuchung der Effizienz des eingesetzten PRFs bei der Behandlung einer spezifischen Indikation. Möglich ist die Gewinnung von sowohl festen als auch flüssigen PRF-Matrices mit den LSCC-Protokollen (Abb. 2). Bei Verwendung des systematischen Protokolls in kontrollierten, klinischen Studien lassen sich die Ergebnisse besser vergleichen und so eine stabile Datenlagen für die Beurteilung der Eignung von PRF per se, als auch von einer spezifischen LSSC-PRF-Variante, gewinnen.
Merke
- PRF lässt sich über ein einfaches, praxistaugliches Herstellungsprotokoll gewinnen.
- Veränderungen der Zentrifugationsparameter führen zu einer unterschiedlichen Zusammensetzung an zellulären und nicht zellulären Komponenten im PRF.
- Die Verwendung des systematischen LSCC-Herstellungsprotokolls erlaubt die Vergleichbarkeit von klinischen Daten aus unterschiedlichen klinischen Studien und Fallserien.
Klinische Anwendung von PRF zum Weichgewebsmanagement
Die bereits betonte Wichtigkeit ein effizientes Weichgewebsmanagement bereits früh in die Therapieplanung bei einer Implantation nach Zahnextraktion zu integrieren, macht einen Einsatz von Biomaterialien zu GTR eigentlich nahezu unumgänglich. Die Verwendung von autologen Blutkonzentraten zur Unterstützung der Geweberegeneration auch im Bereich des Weichgewebes bietet einen vielversprechenden Ansatz. Möglich ist es, Kombinationen von kommerziell erhältlichen Membranen mit z. B. flüssiger PRF-Matrix zu verwenden oder auch feste PRF-Matrices gepresst zu Membranen, die analog als Abschluss über eingebrachtes Biomaterial verwendet werden können. Eine weitere Variante ist die ausschließliche Verwendung von PRF, dann gepresst zu sogenannten Plugs, die in die Extraktionsalveole eingebracht werden (Abb. 3). In einer kürzlich veröffentlichten randomisierten, kontrollierten klinischen Studie (Abb. 4) konnte gezeigt werden, dass die Verwendung von fester PRF-Matrix als autologes Biomaterial in der Anwendung zur Socket bzw. Ridge Preservation zu einer signifikant beschleunigten Geweberegeneration des Weichgewebes führte.28 Bereits in den ersten sieben bis zehn Tagen nach Preservation zeigte sich eine signifikant kleinere residuale Wundöffnung durch den Einsatz von PRF im Vergleich zur Kontrolle (natürliche Heilung).
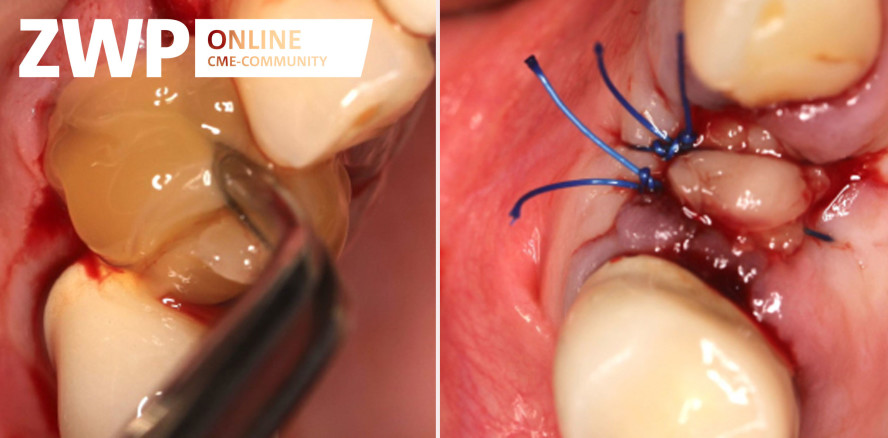
Ein weiterer wichtiger Aspekt ist das Weichgewebsangebot, wie auch die Qualität des Weichgewebes. Ein eher narbiges Weichgewebe, das zudem sichtbar unter Spannung steht, kann zwei maßgebliche potenzielle negative Effekte auf die geplante Implantation haben. Zum einen ist es denkbar, dass die Zugspannung, die durch die Vernarbung entsteht, Druck auf den sich regenerierenden Knochen auslöst. Es wurde bereits beschrieben, dass kontinuierlicher Druck Atrophieeffekte im Kiefer nach sich ziehen kann.29 Es wäre also denkbar, dass im lokal begrenzten Mikromaßstab der Gewebezug einen ähnlichen Einfluss hat und so zumindest dem Gewebezugewinn durch die Knochenregeneration entgegenwirkt. Dies kann möglicherweise über die Stimulation der Osteoklastendifferenzierung geschehen.30 Daraus resultiert unter Umständen ein nicht ausreichendes Knochenangebot in Breite und/oder Höhe im Implantationsgebiet, was weitere Augmentationen für die Implantation nötig macht. Darüber hinaus stellt ein stark narbiges Gewebe auch eine Herausforderung für den Chirurgen bei der Implantations-OP dar. Der spannungsfreie und durch das Implantat vollständig abdeckende Wundverschluss (im Fall von Bone Level Implantaten) oder durch den Implantathals vollständig umschließende Wundverschluss (im Fall von Tissue Level Implantaten) mittels des vorhandenen Weichgewebes, kann unter Umständen nicht erreicht werden (Abb. 5). Weitere Mobilisationsmaßnahmen oder der erneute Einsatz von Biomaterialmembranen kann notwendig werden.
Ein suffizientes Weichgewebe ist also in jedem Fall anzustreben. Ein kritischer Faktor für die Vernarbung sind auch die mechanischen Kräfte, die auf das Weichgewebe bei der Heilung selbst einwirken. Je stärker der Zug, desto größer die Gefahr für die Narbenbildung.31 Beim Alveolenmanagement entstehen mechanische Kräfte auf das Weichgewebe durch einen straffen Wundverschluss, wenn die Wundränder nicht nur spannungsfrei approximiert, sondern zusammengezogen und dann fixiert werden. Der Einsatz von PRF kann hier einen weiteren positiven Beitrag leisten, da durch die Applikation von PRF in die Extraktionsalveole nicht nur die Alveole befüllt, sondern auch verschlossen wird. Die Wundränder können dann vorsichtig und spannungsfrei über den PRF-Clot approximiert werden. Dieses sogenannte Guided Open Wound Healing Concept unterstützt so die Regeneration, ohne zusätzliche unerwünschte mechanische Reize auszuüben. So zeigte sich auch in der bereits zuvor genannten Studie, dass nicht nur eine schnellere Wundheilung in der PRF-Gruppe beobachtet werden konnte, sondern dass darüber hinaus eine gering ausgeprägte Narbenbildung einhergehend mit optisch erkennbar geringer Tension des Weichgewebes beobachtet wurde.28 Ein solch suffizientes Weichgewebe stellt mit Sicherheit eine gute Basis für die Implantatversorgung dar, egal, welcher Implantattyp final geplant wird. Aus weiteren klinischen Studien, in denen der Einfluss auf Knochen- und Weichgewebe, wie auch der Erfolg einer nachgeschalteten Implantation in einem systematischen Ansatz unter der Verwendung von LSCC-PRF untersucht wird, können mit einer ausgedehnteren Datenlage in naher Zukunft belastbare Schlüsse zur Effizienz von PRF in dieser Anwendung gezogen werden.
Merke
- PRF im Einsatz zur Socket Preservation kann zu einer beschleunigten Wundheilung nach Zahnextraktion führen.
- Die Applikation von PRF in einem Guided Open Wound Healing Ansatz kann zu einem narben- und spannungsarmen suffizienten Weichgewebe führen.
Fazit
PRF bietet als autologes Blutkonzentrat einen vielseitigen Einsatz in der GBR und GTR in Vorbereitung auf eine Implantatversorgung. Auch wenn die derzeitige Datenlage noch keine finalen belastbaren Rückschlüsse erlaubt, so weisen die bisherigen Ergebnisse doch auf einen positiven Nutzen der Verwendung von PRF im Weichgewebsmanagement für eine geplante Implantation hin. In weiteren systematischen Studien muss die damit zusammenhängende Hypothese noch abschließend belegt werden.
Weitere Autorin: Dr. Anja Heselich
Dieser Artikel ist im IJ Implantologie Journal erschienen.
Eine Literaturliste steht hier zum Download für Sie bereit.
Bitte beachten Sie, dass CME-Artikel nach zwei Jahren ihre Gültigkeit verlieren.