Implantologie 17.04.2019
Regenerative Behandlung eines Periimplantitisdefekts
share
Im vorliegenden Fallbericht wird eine neue regenerative Behandlungssequenz zur Verbesserung der Gewebesituation im Rahmen der Periimplantitistherapie vorgestellt. Durch die Kombination der mechanischen Reinigung mit Glycinpulver, gefolgt von einer sorgfältigen Implantatdekontamination mithilfe eines antimikrobiellen Präparats auf Hypochloritbasis sowie der chirurgischen Stabilisierung des Gewebes um das Implantat mit einer Ribose-kreuzvernetzten Kollagenmatrix und Unterstützung der Wundheilung durch Hyaluronsäure kann eine knöcherne Ausheilung des periimplantären Defekts erreicht werden.
Die steigende Anzahl an Patienten mit implantatgetragenem Zahnersatz führt automatisch zu einer Zunahme von Erkrankungen des periimplantären Hart- und Weichgewebes.1 Trotz Zehn-Jahres-Überlebensraten von circa 95 Prozent der Zahnimplantate ist auch eine signifikante Zunahme an Spätkomplikationen zu verzeichen.2–4 Diese zeichnen sich in der Regel durch einen periimplantären Knocheneinbruch am Implantat aus.5–8 Die Prävalenz für Periimplantitis liegt in der Größenordnung von 10 Prozent der Implantate und 20 Prozent der Patienten im Zeitraum von fünf bis zehn Jahren nach Belastung der Implantate.9,10 Im Falle einer insuffizienten bzw. nachlassenden Mundhygiene des Patienten führen die periimplantären Läsionen unbehandelt zum Verlust des Implantats und der entsprechenden Suprakonstruktion.11–14
Da bislang keine prospektiven randomisierten Langzeit-Follow-up-Studien existieren, wurden viele Ansätze, aber keine „standardisierte Methode“ zur Periimplantitistherapie beschrieben.
In der nichtoperativen Therapie werden häufig Kombinationen aus mechanischer Reinigung mit Küretten und Airflow-Systemen empfohlen. Adjuvante antiseptische Spülungen, lokale oder systemische Antibiotika sowie Laserbehandlungen sind wirksame Methoden zur kurzfristigen Eradikation von Bakterien. Die Beobachtung der so erzielten Ergebnisse zeigt allerdings, dass spätestens zwölf Monate nach der Therapie die Keime und die Keimbelastung nahe der Ausgangswerte zu erwarten sind.15
Eine chirurgische Therapie mit resektiven oder augmentativen Verfahren rundet die Behandlungspalette ab, da beide Eingriffsformen auf die deutliche Reduktion des Umfangs des vorhandenen Knochendefektes abzielen. Resektive Operationen können eingesetzt werden, um Periimplantatdefekte zu beseitigen, die hygienischen Fähigkeiten wiederherzustellen und das Fortschreiten der Periimplantitis zu reduzieren oder sogar zu stoppen.
Regenerative Ansätze, z. B. mit autologem Knochen und/oder Knochenersatzmaterialien in Kombination mit einer resorbierbaren Membran, sind vielversprechend, wenn es gelingt, die entstandenen Knochendefekte mit neu gebildetem Knochen zuverlässig aufzufüllen. Die „ideale Periimplantitistherapie“ besteht heutzutage somit aus einer Behandlungssequenz von mehreren Ansätzen, die zu einem individuellen Therapieprogramm in Bezug auf die multifaktorielle Ätiologie, Behandlungsoptionen und Studienergebnisse führen.16
In der vorliegenden Arbeit wird eine vielversprechende regenerative Behandlungsmethode eines Periimplantitisdefekts mit der Sequenz mechanische Reinigung, Dekontamination (mithilfe eines auf Hypochlorit-basierten Antiseptikums), Gewebeaugmentation (mit einer Ribose-kreuzvernetzten Kollagenmatrix) und Verbesserung der Wund- und Gewebeheilung (mit Hyaluronsäure) vorgestellt.
Im Gegensatz zur Parodontaltherapie muss bei der Periimplantitistherapie viel häufiger ein chirurgischer Therapieansatz gewählt werden.17
Dekontamination der Implantatoberfläche
Der Behandlungserfolg hängt von einer ausreichenden Darstellung des Defekts durch einen Mukoperiostlappen und die gründliche Reinigung der kontaminierten Implantatoberflächen ab, üblicherweise mittels Kombinationstherapien aus mehreren Reinigungs- und antimikrobiellen Anwendungen.18,19
Eine vielversprechende Option zur adjuvanten Dekontamination von parodontalen und periimplantären Entzündungen stellen lokale Antiseptika auf Basis von Hypochlorit (HOCl) dar (PERISOLV, REGEDENT GmbH). Diese sind Zwei-Komponenten-Präparate, bestehend aus einer 0,95-prozentigen HOCl-Lösung sowie einer Aminosäurelösung. Vor Gebrauch werden die beiden Komponenten gemischt. Dabei entstehen aus HOCl sowie den Aminosäuren kurzlebige sogenannte Chloramine (NCA) als aktive Substanzklasse.NCA sind hochphysiologische Verbindungen, die eine wesentliche Rolle im natürlichen menschlichen Abwehrsystem spielen.20–22
Die ausgeprägte antimikrobielle Wirksamkeit konnte bereits in vitro gezeigt werden, auch auf Biofilme, die sich auf Implantatoberflächen befinden.23,24 Chloramine weisen eine degranulierende Wirkung auf, die die Oberflächenreinigung der komplexen Implantatoberfläche verbessern kann.24–26
In der Behandlung wird das Präparat mehrfach appliziert: Einmal vor der mechanischen Behandlung der Implantatoberfläche, um eine bessere Reinigungsleistung zu erzielen, sowie nach der mechanischen Behandlung zur zusätzlichen Dekontamination.
Augmentation des Defekts
In mehreren Tiermodellen waren regenerative Methoden, insbesondere die gesteuerte Knochenregeneration (GBR), effizienter als das Debridement mit Oberflächendekontaminierung alleine. Die Kombination von Membranen mit Knochenersatzmaterialien waren denjenigen mit Membranen oder Knochentransplantaten allein überlegen.27–29
Aufgrund des häufig ersatzschwachen Lagers und der kritischen Weichgewebesituation stellt die Augmentation von Knochendefekten nach periimplantären Vorerkrankungen eine große Herausforderung dar. Aus diesem Grund bevorzugt der Autor mit seiner Gruppe Ribose-kreuzvernetzte Kollagenmembranen, die insbesondere bei anspruchsvollen Indikationen Vorteile gegenüber konventionellen nativen Präparaten aufweisen.30
In Studien konnte gezeigt werden, dass das Ribose-kreuzvernetzte Kollagen durch seine exzellente Biokompatibilität und Stabilität vom Körper als Leitschiene akzeptiert und zellulär zu Knochen umgebaut wird (Ossifizierung).31–33
Eine 2 mm dicke Ribose-vernetzte gewebeintegrative Kollagenmatrix kann so auch ohne Verwendung von Knochengranulat zu einer signifikanten Verbesserung der Hartgewebesituation führen, insofern diese zwischen ortsständigem Knochen und Mukoperiostlappen platziert wird (OSSIX® VOLUMAX, REGEDENT GmbH).33–35
Da die Kollagenmatrix eine initiale Stabilität aufweist, können kleine knöcherne Einziehungen überbrückt werden, ohne dass ein Kollaps der Matrix befürchtet werden muss. Dies konnten wir in einem Tiermodell zeigen, bei dem bukkal defizitäre Extraktionsalveolen ohne KEM-Auffüllung mit der Kollagenmatrix abgedeckt wurden. Drei Monate nach Augmentation war das erhaltene Knochenvolumen in der Gruppe der Kollagenmatrix sogar statistisch signifikant höher als in der Kontrollgruppe, in der eine GBR-Kombinationsbehandlung mit einer nativen Kollagenmembran und einem langsam resorbierenden bovinen Knochenmineral durchgeführt wurde.34
Dieses Augmentationskonzept lässt sich auch auf die Regeneration von periimplantären Knochendefekten übertragen, die häufig einen kraterförmigen Knochendefekt um das Implantat aufweisen.
Unterstützung der Wund- und Weichgewebeheilung
Augmentationen nach periimplantären Vorerkrankungen bieten zwar potenziell die besten Erfolgsaussichten, jedoch bedeuten sie einen hohen Material- und Kostenaufwand für den Patienten. Aufgrund der limitierten regenerativen Potenz des Knochenlagers und der Komplexität der Oberflächenstruktur und ihrer effektiven Dekontamination besteht immer das Risiko eines Rezidivs bzw. einer Infektion und somit eines Verlusts des Augmentats.Aus diesen Gründen wird in der Literatur immer häufiger die adjuvante Verwendung von regenerativen Agentien (Biologics) vorgeschlagen, um die Erfolgsaussicht zu verbessern.
Neben Schmelz-Matrix-Proteinen und Wachstumsfaktoren weisen insbesondere die deutlich preisgünstigeren Hyaluronsäure-(HA-)Präparate vielversprechende unterstützende regenerative Eigenschaften auf, die die Komplikationsrate potenziell reduzieren.36,37
Es ist bekannt, dass die klinische Anwendung von Hyaluronsäure die bakterielle Kontamination der Wundstelle reduziert, wodurch das Risiko einer postoperativen Infektion verringert und eine vorhersagbarere Regeneration gefördert wird. Darüber hinaus ist bekannt, dass Hyaluronsäure die Neoangiogenese postoperativ stimuliert und zu einer deutlichen Verbesserung/Verkürzung der Wundheilung führt.38,39
In einer kürzlich publizierten prospektiven Vergleichsstudie zur Deckung von gingivalen Rezessionen konnte gezeigt werden, dass mit der begleitenden HAAnwendung (hyaDENT BG, REGEDENT GmbH) eine statistisch signifikant bessere Abdeckung der Zahnwurzel erzielt werden kann. Nach einer Woche postoperativ wiesen mit Hyaluronsäure behandelte Patienten zudem statistisch signifikant weniger Unbehagen und Schwellung auf.40,41
Aufgrund dieser positiven Effekte bietet sich die adjuvante Verwendung von Hyaluronsäure zur Unterstützung der Regeneration bei der Augmentation von Knochendefekten nach periimplantären Entzündungen an.
Fallbericht
Die (Angst-)Patientin (Nichtraucher, gesund) erhielt vor circa acht Monaten eine implantatgetragene Stegversorgung im Oberkiefer. Die Implantate wurden gleichzeitig mit der Extraktion der Restbezahnung vom selben Behandler in den Restknochen inseriert, ohne zu Augmentationsmaßnahmen zu greifen (Abb. 1). Die Implantatintegration dauerte circa drei bis vier Monate. Nach Eingliederung des individuell geformten Stegs aus Titanium beklagt die Patientin circa sechs Monate später eine Druckstelle Regio 22 palatinal (Abb. 2). Klinisch imponiert die palatinale Gingiva mit Schwellung und die Sondierungswerte zeigen sich erhöht. Nach einigen lokalen topischen Anwendungen wird deutlich, dass eine periimplantäre Entzündung der Auslöser der subjektiven Beschwerden ist. Das zu diesem Zeitpunkt angefertigte Röntgenbild zeigt einen ausgeprägten kraterförmigen Knochendefekt um Implantat 22 (Abb. 3).
Der Behandlungsplan sah eine gründliche Dekontamination der exponierten Implantatareale 22 unter Aufklappung vor. Aufgrund des fortgeschrittenen Knochendefekts war ein regeneratives Vorgehen geplant, mit dem Ziel einer knöchernen Regeneration des Defekts.
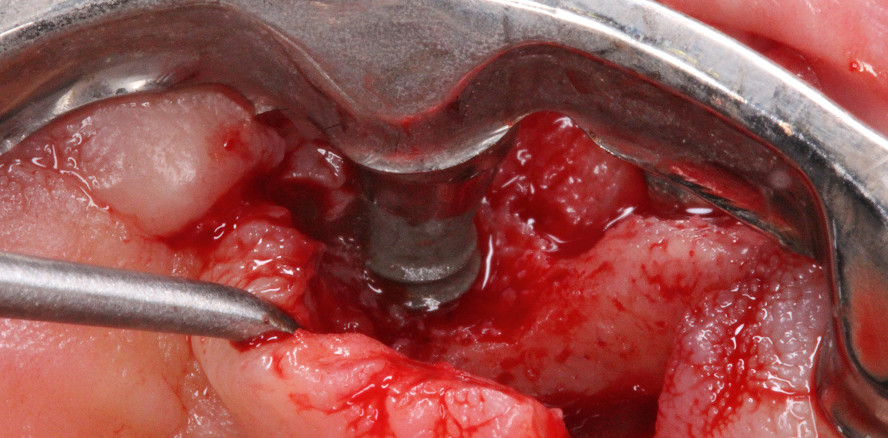
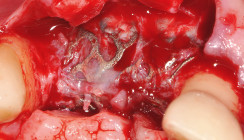
Die Darstellung des Knochendefekts erfolgt mithilfe einer midkrestalen Inzision entlang des Stegs und extendiert distal des 24, um auf eine vertikale Entlastungsinzision zu verzichten. Nach einer gründlichen Degranulation mit Küretten um das Implantat wird das Ausmaß des Knochendefekts sichtbar (Abb. 4). Die exponierten Implantatoberflächen werden mit dem Glycinpulver des Airflow-Geräts (EMS) mechanisch gereinigt.
Zur Dekontamination und Unterstützung der Oberflächenreinigung des Implantats wird ein lokales Antiseptika (PERISOLV, REGEDENT GmbH) auf die Implantatoberfläche appliziert und 30 Sekunden in situ belassen. Nach einer weiteren mechanischen Reinigung erfolgt eine zweite Applikation des Chloraminpräparats (Abb. 5).
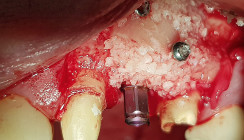
Zur Entfernung von Resten des Antiseptikums wird der Knochendefekt mit physiologischer Kochsalzlösung ausgespült. Zum Auffüllen des Defekts wird anstelle eines Knochenersatzmaterials eine Ribose-kreuzvernetzte Kollagenmatrix verwendet (OSSIX VOLUMAX, REGEDENT GmbH). Die Kollagenmatrix wird mit Hyaluronsäure hydratisiert (hyaDENT BG, REGEDENT GmbH; Abb. 6), mehrfach gefaltet und straff in den Defekt eingebracht. Davor wird die Implantatoberfläche ebenfalls mit dem HA-Gel beschickt, sodass der Wundraum komplett mit Hyaluronsäure abgedeckt ist (Abb. 7). Die Matrix als „Rolle“ erstreckt sich von bukkal nach palatinal um das Implantat. Zur Verbesserung der Wundheilung wird die Matrix vor dem Wundverschluss mit einer dünnen Lage Hyaluronsäure bedeckt (Abb. 8).
Der spannungsfreie vollständige Wundverschluss erfolgt mit einer Kombination aus horizontalen Matratzen- und mehreren Einzelknopfnähten (PTFE 4-0, Biotex, REGEDENT GmbH) unter dem nach wie vor befestigten Steg (Abb. 9). Die Patientin wird angewiesen, zweimal täglich CHX-Gel 1 Prozent auf die operierte Region zu verstreichen. Des Weiteren wird ihr ein Antibiotikum (Doxycyclin 200 mg für zehn Tage) verordnet. Die Nahtentfernung erfolgt zwei Wochen postoperativ. Zu diesem Zeitpunkt zeigte sich das Areal komplett reizfrei mit guten Zeichen einer fortgeschrittenen Wundheilung (Abb. 10 und 11). Der weitere Heilungsverlauf blieb unauffällig.
Bei der Reevaluation drei Monate postoperativ zeigen sich gesunde entzündungsfreie Verhältnisse mit einer deutlich verbesserten Weichgewebemanschette um das Implantat 12 (Abb. 12 und 13), aber auch eine an der Basis des Stegs deutlich auszumachende Rezession auf der distalen Implantatseite.
Die klinische und radiologische Kontrolle erfolgt nach weiteren drei Monaten und zeigt bereits deutliche Zeichen einer Mineralisation in dem ehemaligen kraterförmigen Knochendefekt (Abb. 14 und 15). Da die Patientin durch die eingetretene Rezession ein phonetisches Defizit beklagt, muss der Steg nun abgenommen werden, um das einer Hohlkehlepräparation nachempfundene Querschnittprofil des Stegs vom Zahntechniker rekonturieren zu lassen. Die Umgestaltung des Stegprofils ist notwendig, da sich ansonsten die Prothesenbasis nicht unterfüttern lässt. Während der Umarbeitung entsteht die Gelegenheit, die klinische Befundung des Implantats störungsfrei durchzuführen. Die Sondierungswerte um das Implantat liegen bei 2 bis 3 mm ohne Anzeichen einer Blutung (Abb. 16–19). Nach der Umarbeitung des Stegs und einer Unterfütterung der Kunststoffbasis sind die phonetischen Beschwerden behoben. Ein abschließender OPG-Befund wird nach Ablauf von zwölf Monaten erstellt und demonstriert nahezu komplette knöcherne Ausheilung des periimplantären Defekts an 22 (Abb. 20).
Zusammenfassung
Die Kombination einer sorgfältigen Implantatdekontamination mithilfe eines antimikrobiellen Präparats auf Hypochloritbasis sowie der chirurgischen Stabilisierung der Gewebesituation um das Implantat mit einer Ribose-kreuzvernetzten Kollagenmatrix bietet eine vielversprechende regenerative Behandlungsoption zur Verbesserung der Gewebesituation im Rahmen der Periimplantitistherapie. Durch die adjuvante Anwendung von Hyaluronsäure kann das Risiko eines Rezidivs bzw. einer erneuten Infektion minimiert werden, weil Regenerations- und Wundheilungsprozesse beschleunigt werden.
Die vollständige Literaturliste gibt es hier.
Der Beitrag ist im Implantologie Journal erschienen.
Foto: Autor