Implantologie 03.03.2015
Periimplantitis – Das sollte man wissen
share
Die Implantattherapie ist heutzutage fester Bestandteil des zahnärztlichen Behandlungsspektrums. Trotz einer generell zuverlässigen Anwendung besteht jedoch auch immer das Risiko einer Entzündung von periimplantären Geweben und damit einer periimplantären Mukositis sowie Periimplantitis. Die adäquate Behandlung einer solchen Erkrankung stellt die Zahnmedizin vor eine große Herausforderung. Eine optimale Diagnostik, Vorbehandlung und Nachsorge sind dabei unerlässliche Bestandteile der täglichen Praxis. Folgender Artikel fasst prägnant zusammen, was Zahnärzte über periimplantäre Erkrankungen wissen sollten.
Seit mehr als 20 Jahren stellen enossale Implantate eine wichtige und verlässliche Therapieoption für den Ersatz verloren gegangener Kaueinheiten dar.1–3 Auch wenn die Implantattherapie heute generell verlässlich Anwendung findet und eine hohe Erfolgsrate zu verbuchen ist, können entzündliche Komplikationen wie periimplantäre Mukositis und Periimplantitis entstehen.4 Daher muss der behandelnde Zahnarzt bereits bei der Therapieplanung bestimmte Risikofaktoren ausschließen und ggf. beseitigen. Dies gilt in besonders hohem Maße für Patienten mit Parodontitis,2,4 bei denen Implantate zur Wiederherstellung der Ästhetik und Funktion der verloren gegangenen Kaueinheiten Einsatz finden. Fehlende präventive Maßnahmen bei dieser Patientengruppe führen zu einer hohen Inzidenz für das Auftreten von periimplantärer Mukositis und Periimplantitis.4 Prof. Dr. Andrea Mombelli sprach bereits 2006 vom „Tsunami der Zahnmedizin“. Diese Titulierung impliziert die bevorstehende Herausforderung, welche nicht nur auf spezialisierte Parodontologen, Implantologen und Kieferchirurgen zukommt, sondern jeden Allgemeinzahnarzt treffen kann. Daher sollte jeder Zahnarzt über die klinischen Zeichen der Perimukositis und Periimplantitis genau informiert sein.
Definition und Symptome periimplantärer Erkrankungen
Der Begriff Periimplantitis wurde vor mehr als zwei Jahrzehnten als Begriff für infektiöse pathologische Zustände von periimplantären Geweben eingeführt.2 Die einfache Unterscheidung der Parodontalerkrankungen lässt sich auf die periimplantären Erkrankungen übertragen.5,6 Somit handelt es sich bei der periimplantären Mukositis um eine reversible, bakteriell bedingte Entzündung der suprakrestalen Weichgewebe um osseointegrierte, funktionell belastete Implantate ohne Anzeichen von Knochenverlust. Klinisch imponiert die Mukositis durch Rötung und Schwellung der Weichgewebe. Analog hierzu ist die Gingivitis zu betrachten.
Die Periimplantitis bezeichnet das weitere Voranschreiten der primär bakteriellen Entzündung um osseointegrierte, funktionell belastete Implantate mit progressivem Verlust von periimplantären Knochenstrukturen. Im klinischen Befund ist die erhöhte Sondierungstiefe der entscheidende Parameter. Analog hierzu ist die Parodontitis anzusehen.5,6
Epidemiologie entzündlicher periimplantärer Erkrankungen
1986 schlug Albrektsson Erfolgskriterien für dentale Implantate vor und führte hierzu den Begriff „Implantatüberleben“ ein, welcher lediglich die mechanische Stabilität charakterisierte.7 Jedoch können auch Implantate mit periimplantärer Infektion oder periimplantärem Knochenverlust mechanisch stabil sein. Falls Implantatkomponenten oder die Suprakonstruktionen frakturieren oder periimplantäre Infektionen auftreten, spricht man von Komplikationen, welche ihrerseits in primäre Komplikationen (während der Osseointegration) oder sekundäre Komplikationen (nach funktioneller Belastung und während der Erhaltungsphase) unterteilt werden können.6 Dies gilt nicht für die Sofortimplantation, da die Osseointegration nach funktioneller Belastung noch nicht abgeschlossen ist. Von Implantatversagen spricht man, wenn ein Implantat verloren geht. Bei einer Untersuchungsperiode von zehn Jahren war ein Implantatverlust in einem von 20 Fällen zu verbuchen. Verschiedene Reviews konnten zeigen, dass die Prävalenzangaben sowohl für die Mukositis als auch für die Periimplantitis stark davon abhängig waren, ob sie sich auf das Patientenkollektiv oder die Implantatanzahl beziehen. Darüber hinaus differieren die Definitionen für Mukositis und Periimplantitis innerhalb der Studien.8,9
In einem systematischen Review von Berglundh und Mitarbeitern, die longitudinale, prospektive Studien verglichen, wurden die biologischen und technischen Komplikationen der Implantattherapie herausgearbeitet. Periimplantitis war bei 6,5 Prozent der Implantate diagnostiziert worden. Im Gegensatz dazu lag bei Zitzmann und Berglundh die Periimplantitisprävalenz zwischen 28 bis 56 Prozent beim Patientenkollektiv und 12 bis 43 Prozent der Implantate. Diese gegensätzlichen Ergebnisse unterstreichen die Wichtigkeit einheitlicher Definitionen für Mukositis und Periimplantitis. Eine Übersichtsarbeit von Mombelli und Mitarbeitern,2 welche 29 Artikel einschloss, kam zu einer mittleren Prävalenz von zehn Prozent der Implantate und 20 Prozent der Patienten fünf bis zehn Jahre nach der Implantation. Raucher und Patienten mit Parodontitisvorgeschichte sind mit einer höheren Prävalenz für Periimplantitis assoziiert.2 Eine weitere Arbeit von Atieh et al. 2013 gab für die periimplantäre Mukositis eine Prävalenz von 63,4 Prozent der Patienten und 30,7 Prozent der Implantate an. Für die Periimplantitis wurde eine Prävalenz von 18,8 Prozent des Patientenkollektivs und 9,6 Prozent der Implantate geschätzt.10
Ätiologie periimplantärer Erkrankungen
Die Struktur der ein Implantatabutment umgebenden Mukosa wurde in zahlreichen Studien untersucht. Schon 1991 verglichen Berglundh, Lindhe et al. mit einer tierexperimentellen Studie am Beagle die Struktur der Gingiva um den Zahn mit der periimplantären Mukosa.11
Die periimplantäre Mukosa besteht aus oralem Gingivaepithel, oralem Sulkusepithel und einem nicht keratinisierten Saumepithel und entspricht somit weitgehend der epithelialen Anheftung an den Zahn.11,12 Die Kollagenfasern der periimplantären Mukosa beginnen auf Höhe des krestalen Knochens und verlaufen parallel zur Implantatoberfläche. Dies ist ein wesentlicher Unterschied zum Zahn, bei dem die suprakrestalen Bindegewebsfasern vertikal in das Wurzelzement inserieren. Es existieren also dentogingivale und dentoalveoläre Faserbündel, die lateral, koronal oder apikal verlaufen. Somit wird das Gingivaepithel am Zahn stabilisiert. Im Gegensatz zum Zahn herrschen um das Implantat gefäß- und zellarme Bedingungen vor. Somit ist es nicht verwunderlich, dass die Reaktionen der periimplantären Gewebe bei bakterieller Infektion zu rascheren Destruktionen des Weichgewebes und zu schnellerem Tiefenwachstum der Destruktion führen können.
Nach dem 6. Europäischen Workshop der Parodontologie sind, periimplantäre Erkrankungen infektiöser Natur. Dabei sind die Mikroorganismen, die mit der Periimplantitis assoziiert sind von ähnlicher Zusammensetzung wie bei einer Parodontitis.
Schon kurz nach der Implantation etabliert sich im subgingivalen Bereich ein Keimspektrum, in dem Peptostreptococcus micros, Fusobacterium nucleatum und Prevotella intermedia vorherrschen. Die Periimplantitis zeichnet sich durch ein überwiegend anaerobes, gramnegatives Keimspektrum aus. Viele parodontalpathogenen Keime wurden auch in periimplantären Läsionen gefunden. Hierzu zählen Aggregatibacter actinomycetemcomitans, Bakterien des roten und orangenen Komplexes, wie Porphyromonas gingivalis und Prevotella intermedia, aber auch Staphylococcus aureus, welcher eine Affinität zu Titanoberflächen aufweist. So zeigt es sich, dass die parodontale Situation des Patienten ein entscheidender Faktor für das spätere Auftreten einer periimplantären Infektion darstellt.
Die Akkumulation von bakterieller Plaque an der periimplantären Mukosa führt zur Ausbildung einer Entzündung mit ihren typischen Zeichen. Besteht solch ein Biofilm länger, weitet sich die periimplantäre Läsion weiter nach apikal aus, ohne von Kollagenfasern eingekapselt zu werden wie dies bei der Parodontitis der Fall ist. Das entzündliche Infiltrat kann sich bei der Periimplantitis bis zum periimplantären Knochen ausdehnen, während es bei der Parodontitis durch einen ca. 1 mm breiten, entzündungsfreien Bindegewebssaum vom Knochen getrennt bleibt.
Parodontitis und andere Risikofaktoren für die Ausbildung einer periimplantären Infektion
Wie bei der Parodontitis handelt es sich bei der Periimplantitis ebenfalls um ein multifaktorielles Geschehen, bei dem viele verschiedene Faktoren zusammenspielen.
Stefan Renvert und Jean-Louis Giovannoli unterscheiden hier lokale von allgemeinen Faktoren6:
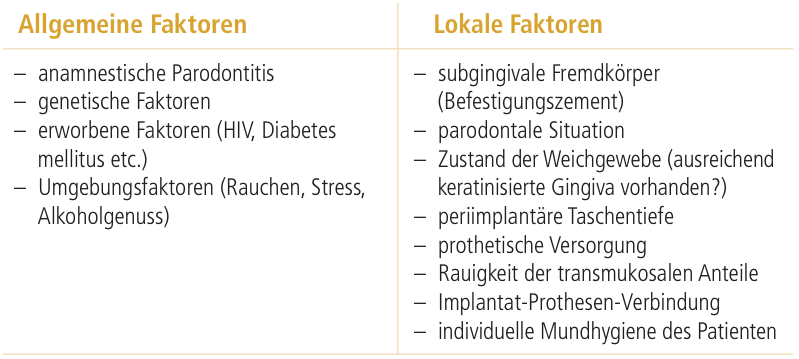
Alle diese Faktoren beeinflussen die entzündliche Reaktion auf die Mikroorganismen bzw. die Entwicklung und Pathogenität der supra- und subgingivalen Plaque. Sobald sich ein pathogener Biofilm etabliert hat und der Patient eine gesteigerte Suszeptibilität für entzündliche Veränderungen hat, steigt das Periimplantitisrisiko.6 In diesem Artikel sollen nur einige dieser Faktoren beschrieben werden.
Da es sich bei der Periimplantitis um eine bakterielle Infektion handelt, kommt der individuellen Mundhygiene des Patienten eine entscheidende Rolle zu. Eine Übersichtsarbeit von Mombelli und Décaillet aus dem Jahr 2011 fasste die Merkmale periimplantärer Biofilme zusammen13: Danach handelt es sich bei der Periimplantitis um anaerobe Mischinfektionen, bei der die Zusammensetzung des subgingivalen Biofilms der einer chronischen Parodontitis gleicht. Es dominieren gramnegative Bakterienspezies. Darüber hinaus können verschiedene andere Mikroorganismen wie Peptostreptokokken und Staphylokokken vorkommen. Mechanische und chemische Interventionen können bei derartigem Geschehen zu einem Rückgang der Symptomatik führen. Einige Langzeitstudien deuten darauf hin, dass Patienten mit einer Parodon- titisvorgeschichte im Vergleich zu parodontal gesunden Patienten langfristig ein höheres Risiko für das Auftreten einer Periimplantitis und auch für Implantatverluste aufweisen.14 Dies gilt für die chronische Parodontitis3,15–19 und auch für die aggressive Form20–22. Die Vierte Deutsche Mundgesundheitsstudie zeigte, dass in Deutschland ca. 20 Prozent der 35- bis 44-Jährigen und ca. 40 Prozent der 65- bis 74-Jährigen die Symptome einer fortgeschrittenen Parodontitis mit Sondierungstiefen von mindestens 6 mm aufweisen.23 Bei derartigen Patienten finden Implantate zum Verlust verloren gegangener Kaueinheiten ebenfalls Anwendung. Eine Übersichtsarbeit von Christgau 2013 bestätigte die Annahme, dass parodontal vorerkrankte Patienten im Vergleich zu parodontal gesunden Patienten lang- fristig ein höheres Risiko für das Auftreten einer Periimplantitis und möglicherweise für Implantatverluste aufweisen. Er betonte jedoch, dass die Ergebnisse mit Vorsicht zu interpretieren sind, da die Studien diverse methodische Probleme beinhalten.14 Ein aktuellerer Review von Sgolastra et al. fand eine hohe Evidenz dafür, dass Parodontitis ein Risikofaktor für späteren Implantatverlust darstellt, jedoch nur moderate Evidenz, dass Parodontitis ein Risikofaktor für die Ausbildung einer Periimplantitis ist.24
Auch die Auswirkung des Rauchens wurde in diversen Studien diskutiert. Hervorzuheben ist, dass sich in den verschiedenen Studien die Definition eines Rauchers unterscheidet. Dies wird in Abhängigkeit der täglich konsumierten Zigaretten festgelegt. Strietzel und Mitarbeiter stellten 2007 in einer Übersichtsarbeit den Zusammenhang zwischen einer positiven Raucheranamnese und Periimplantitis dar.25 Ein aktueller Review fand nur geringe Evidenz dafür, dass Rauchen ein Risikofaktor für Periimplantitis darstellt.26 Zukünftig werden mehr prospektive Studien gebraucht, welche nach strukturierten Protokollen und v.a. genauen allgemeingültigen Definitionen durchgeführt werden.26
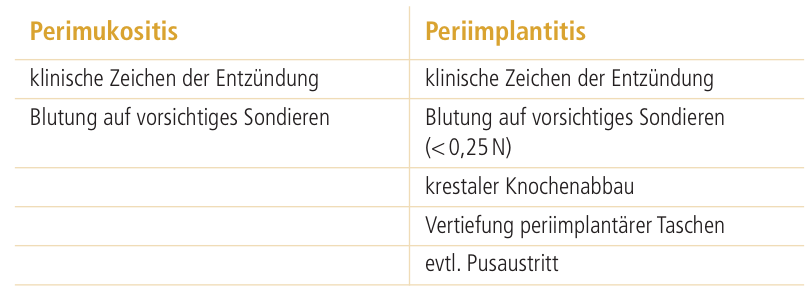
Tab. 1: Merkmale von Perimukositis und Periimplantitis.
Immer häufiger werden die Suprakonstruktionen zementiert und nicht mehr verschraubt. Wenn in solchen Fällen der Zement nicht sorgfältig aus dem Sulkus entfernt wird, löst er eine entzündliche Reaktion aus, welche zum Verlust des periimplantären Knochens führen kann.
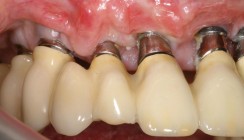
Im Consensus Report des siebten Workshop on Periodontology wurde zudem darauf verwiesen, dass auch andere iatrogene Faktoren eine Rolle spielen. Hier sind eine insuffiziente Passung zwischen Abutment und Restauration (Abb.1), eine Überkonturierung der prothetischen Restauration, eine Fehlpositionierung des Implantats sowie technische Komplikationen zu nennen.27
Auch endodontische Infektionen der Nachbarzähne spielen eine wesentliche Rolle und können die Prognose des Implantats deutlich beeinträchtigen.6 Der Abstand zwischen endodontisch behandelten Zähnen und dem Implantat sowie der zeitliche Abstand der endodontischen Behandlung und der Implantation sind hierbei von entscheidender Bedeutung.
Diagnostik periimplantärer Erkrankungen
Die Diagnostik der periimplantären Erkrankungen unterscheidet sich nicht maßgeblich von den diagnostischen Maßnahmen, welche üblicherweise in der Parodontologie Anwendung finden. Neben klinischer und radiologischer Untersuchung kommt der mikrobiologischen Diagnostik eher eine untergeordnete Rolle zu. Um den Gesundheitszustand der periimplantären Gewebe zu erfassen, sollte zunächst eine systematische Inspektion der periimplantären Mukosa erfolgen. Auf diese Weise können Ödeme, Hyperplasien, Rezessionen, Erytheme und eventuelle spontane Blutungen oder Pusaustritt erfasst werden.
Danach sollte im Zuge einer periimplantären Sondierung mittels Metallsonde, Titansonde oder Kunststoffsonde die Tiefe der periimplantären Taschen sowie die Höhe der marginalen Mukosa bestimmt werden.6 In der Praxis haben sich flexible Kunststoffsonden bewährt, da sich diese bei sehr ausladenden prothetischen Suprakonstruktionen, wie sie leider öfter vorkommen, der Geometrie entsprechend formen können. Bei der Sondierung um Implantate ist besonders auf geringen Sondierungsdruck (0,2–0,25 N) zu achten. Dies ist auf die besondere anatomische Struktur der Weichgewebe um Implantate zurückzuführen. Bei gesunden Gewebeverhältnissen erreicht die Sondenspitze den apikalen Anteil des Epithels. Bei Entzündung der periimplantären Gewebe durchbricht die Sonde leichter das periimplantäre Bindegewebe und kommt auf dem Niveau des krestalen Knochens zu liegen. Dies konnte Schou 2002 in einer tierexperimentellen Studie zeigen. Ein weiterer wichtiger Faktor bei der Sondierung ergibt sich aus dessen Zeitpunkt, da die Zunahme von Sondierungstiefe und Veränderungen des periimplantären Knochenniveaus dynamische Prozesse darstellen.31 Daher sollten Befunde von mindestens zwei Untersuchungszeitpunkten vorliegen, um diese Parameter richtig beurteilen zu können.31 So ist ein krestaler Knochenverlust von bis zu 1,5 mm im ersten Jahr nach der Implantation eher auf das Remodeling des Alveolarknochens während der initialen Heilungsphase als auf entzündliche Veränderungen zurückzuführen. Man nimmt an, dass das Remodeling ca. zwölf Monate nach der prothetischen Versorgung abgeschlossen ist. Aus diesem Grund sollten die Sondierungstiefen zu diesem Zeitpunkt als Baseline erhoben werden. In der Nachsorge sollte ein Sondierungsstatus abhängig von der sonstigen parodontalen Situation und den weiteren individuellen Risikofaktoren mindestens einmal pro Jahr angefertigt werden. Sollten im Verlauf der Nachsorge eine Suppuration oder Blutung auf Sondierung auftreten, werden die Befunde mit der Baseline-Messung verglichen und erlangen dadurch eine größere Aussagekraft. Eine Blutung auf Sondierung oder eine Suppuration sind Anzeichen für das Bestehen einer Entzündung periimplantärer Gewebe, welche in aller Regel auf eine bakterielle Besiedelung der submukösen Abutment- oder Implantatoberflächen zurückzuführen ist. Eine fortbestehende Blutung auf Sondierung um Implantate ist mit einem fortschreitenden Knochenverlust verbunden.32
Bereits bei Eingliederung der prothetischen Versorgung sollte ein Röntgenbild im Sinne eines Referenzbildes angefertigt werden. Nach dem ersten Jahr in Funktion sollte ein weiteres Bild angefertigt werden, da zu diesem Zeitpunkt die Remodeling-Prozesse abgeschlossen sind. Bestehen im weiteren Verlauf der Implantatnachsorge nach Erhebung der klinischen Parameter in definierten Abständen der begründete Verdacht auf eine Periimplantitis, so sollten auch zu diesem Zeitpunkt intraorale Röntgenaufnahmen angefertigt werden. Wünschenswert bei diesen Aufnahmen wäre die Verwendung eines standardisierten Filmhalters. Intraorale Röntgenaufnahmen ohne klinische Befunde reichen für die Diagnose periimplantärer Knochendefekte nicht aus, da vestibuläre oder orale Knochendefekte durch die metalldichte Verschattung eines Implantatkörpers überlagert werden können.
Die Kombination von klinischen Befunden und röntgenologischer Diagnostik ist hilfreich, um die Morphologie periimplantärer Knochendefekte besser einschätzen zu können. Diese Befunde können durch mikrobiologische Untersuchungen ergänzt werden. Zum Nachweis der subgingivalen Mikroflora um Implantate kommen bakterielle Kulturen und DNA-Sondentests zur Anwendung.
Bei den sekundären Implantatkomplikationen müssen biomechanische Zwischenfälle von den infektiösen Komplikationen abgegrenzt werden. Dies führt zu den Differenzialdiagnosen einer Periimplantitis, welche auch bedacht werden müssen. So können auch Frakturen am Implantat, welche durch Überbelastung hervorgerufen werden können, zum Verlust der Osseointegration führen. Weiterhin kommt eine Osseodesintegration auch durch okklusales Trauma vor.
Eine Einteilung der Periimplantitis-Stadien (Tab. 2) wurde bereits 1993 durch Spiekermann vorgeschlagen.33

Tab. 2: Stadieneinteilung der Periimplantitis nach Spiekerkamm
Therapie periimplantärer Infektionen
In Analogie zu den Therapiestrategien der parodontalen Erkrankungen unterscheidet man bei der Therapie periimplantärer Infektionen zwischen der Hygienephase und chirurgischen Phase gefolgt von der Erhaltungsphase. Im Rahmen dieser Implantatnachsorge hat sich dann das Berner Konzept der auffangenden kumulativen unterstützenden Therapie (AKUT) bewährt.34 Das übergeordnete Ziel der Periimplantitistherapie ist der Implantaterhalt mit Vermeidung eines weiteren Verlustes periimplantären Knochens.35
Während der sogenannten Hygienephase (initiale Phase) werden die Infektionsursachen beseitigt und mögliche modulierende (Risiko-)Faktoren ermittelt und ausgeschlossen. Dies umfasst eine professionelle Zahnreinigung mit Mundhygieneanweisung. Die subgingivalen Zahn- und Implantatoberflächen werden, falls erforderlich, durch nichtchirurgische Maßnahmen wie mechanisches Debridement gereinigt. Hierzu stehen verschiedene Instrumente zur
Verfügung: Handinstrumente aus Karbon oder Titan, Schall- oder Ultraschallinstrumente mit Kunststoffansatz, Pulverstrahlgeräte, Laser und die Anwendung der Photodynamischen Therapie. Darüber hinaus finden adjuvant zur Instrumentierung der Implantatoberflächen lokal antiseptische (z.B. Chlorhexidindigluconat) und/oder antibiotische Substanzen (z. B. Minocyclin) Anwendung. In wenigen Fällen kann die adjuvante systemische Antibiotikagabe eine sinnvolle Therapieergänzung sein. Die mechanische Instrumentierung der Implantatoberfläche alleine hat jedoch einen geringeren Einfluss auf die klinischen Zeichen der Periimplantitis als die Kombination von submukosalem Debridement und adjuvanter Gabe von lokalen oder systemischen Antibiotika. Dieser Zusammenhang wurde durch Übersichtsarbeiten von Renvert und Mitarbeitern bestätigt.36,37
In einer Übersichtsarbeit kamen Muthukuru und seine Mitarbeiter zu dem Schluss, dass lokal applizierte Antibiotika wie Minocycline oder Doxycycline in Kombination mit submukosalem Debridement ebenfalls wirkungsvoller sind als mechanisches Debridement und anschließende Taschenirrigation mittels Chlorhexidindigluconat.38 Des Weiteren konnte gezeigt werden, dass die Behandlung der Implantatoberfläche mit einem Er:YAG-Laser im Vergleich zur Kombination von submukosalem Debridement mit adjuvanter, submukosaler Chlorhexidindigluconat-Irrigation einen größeren Einfluss auf die klinischen Zeichen der Periimplantitis haben könnte.38
Das submukosal angewendete Pulverstrahlgerät mit Glycinpulver scheint ebenfalls klinisch besser abzuschneiden als die Kombination aus submukosalem Debridement und Chlorhexidindigluconat-Irrigation. Keine klinisch signifikanten Unterschiede zeigten sich hingegen aus dem Vergleich von Er:YAG-Laser und Pulverstrahlgerät mit Glycinpulver zur Dekontamination der Implantatoberfläche.38
Derzeit liegen für nichtchirurgische und chirurgische Periimplantitistherapie nur sehr wenige qualitativ hochwertige Studien vor.39 Daher ist es auch schwierig, eindeutige Therapieempfehlungen auszusprechen.39,40
Nach geschlossenem Vorgehen während der Hygienephase werden die klinischen Parameter erneut evaluiert. In vielen Fällen reicht die geschlossene Vorgehensweise nicht aus. Aus diesem Grund schließt sich eine chirurgische Phase an. Das wichtigste Ziel der chirurgischen Periimplantitistherapie ist die Schaffung eines Zugangs für das Debridement und die Dekontamination der infizierten Implantatoberfläche.6 Die Schnittführung sollte möglichst so gewählt werden, dass viel Weichgewebe erhalten werden kann. Die Reinigung der Implantatoberfläche sollte dann mit den oben genannten Hilfsmitteln erfolgen. Es bietet sich an, Instrumente aus Reintitan (z.B. eine Rundbürste) zu verwenden.6
Bei regenerativen oder resektiven Zielsetzungen kann mittels Laser gut eine Dekontamination erfolgen. Vielfach wurde auch die Möglichkeit von Implantoplastiken der exponierten Implantatanteile diskutiert. Unterstützend zur mechanischen Oberflächenbearbeitung kommen lokal antimikrobiell wirksame Substanzen zum Einsatz (Chlorhexidindigluconat, EDTA, Zitronensäure).35 Mombelli und Lang schlugen bereits 1998 ein Stufenkonzept vor34: Das AKUT-Konzept (auffangende kumulative unterstützende Therapie). Anhand der klinischen Parameter Plaque, Blutung, Suppuration, Sondierungstiefe und radiologisch nachweisbarem Knochenverlust wird eine befundadäquate Therapie durchgeführt (Tab. 3 und 4). Als Standard wird ein vierteljährliches Intervall für die Implantatnachsorge empfohlen.
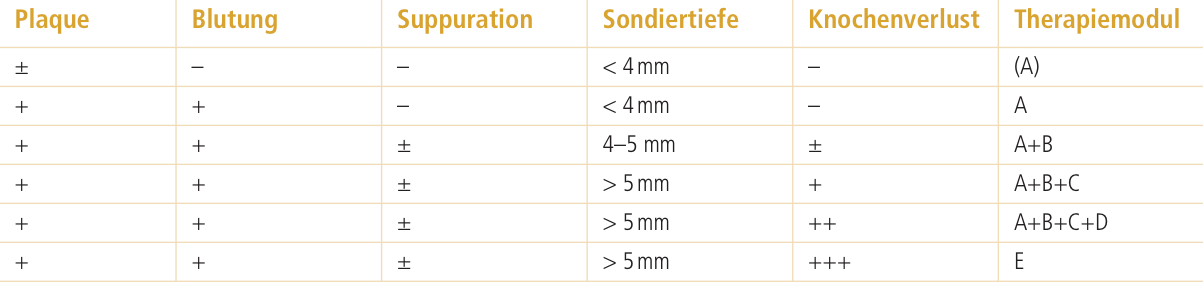
Tab. 3: AKUT-Konzept – klinische Parameter mit therapeutischer Konsequenz.34
Auszüge eines hoffnungslosen
klinischen Falls in Bildern: Wenn auch alles Wissen zur
Periimplantitis nichts mehr nützt ...
Abbildung 4 zeigt den radiologischen Ausgangsbefund einer 58-jährigen Patientin. Es imponiert ein generalisierter Knochenabbau um Zähne und Implantate. Anamnestisch konnte evaluiert werden, dass die bestehenden Implantate ohne vorherige Parodontitistherapie direkt einphasisch nach Extraktion inseriert und direkt prothetisch versorgt worden sind. Es fand keine strukturierte Implantatnachsorge statt.
Abbildung 5 zeigt den klinischen Ausgangsbefund: Zu sehen sind generalisiert erhöhte Sondierungstiefen mit erhöhter Lockerung der gesamten prothetischen Versorgungen im OK und UK und einer generalisierten Blutung mit lokalem Pusaustritt an Implantaten und Zähnen.
Aufgrund des generalisierten, fortgeschrittenen Knochenverlustes war im Rahmen einer Totalsanierung die Extraktion sämtlicher Zähne und Explantation aller Implantate unumgänglich (Abb. 6).
Die Zähne 32 und 33 wurden zunächst belassen, um eine verkürzte Unterkieferprothese bei extrem ausgeprägtem Würgereiz zu verankern. Im Vorfeld wurde eine mikrobiologische Diagnostik (Abb. 7) durch ein Fachlabor (PCR und Lebendanzucht) mit Antibiogramm erstellt, um bei bestehendem klinischen Istzustand eine mögliche Besiedelung mit dem Aggregatibacter actinomycetemcomitans auszuschließen. Die Extraktion/Explantation und auch die spätere Implantation fanden unter dem Schutz von Amoxicillin mit Clavulansäure statt (Abb. 7). Nach Rücksprache mit dem Mikrobiologen und dem implantierenden Kieferchirurgen wurden alle Zähne und Implantate im Oberkiefer entfernt. Zur Überbrückung der insgesamt beinahe einjährigen Abheilphase (sechsmonatige Abheilphase nach Extraktion; sechsmonatige Einheilphase der Implantate) wurde im Oberkiefer eine Totalprothese und im Unterkiefer eine Teilprothese mit Verankerung an 32 und 33 eingegliedert.
Der radiologische Befund nach Ausheilung aller Gewebe vor prothetischer Versorgung zeigt stabile periimplantäre Knochenverhältnisse (Abb. 8). Wie die Abbildungen 9 und 10 zeigen, wurde die Situation mit herausnehmbaren teleskopierenden Brücken versorgt. Die neue klinische Situation der Patientin zeigt entzündungsfreie periimplantäre Verhältnisse (Abb. 11). Durch ein strukturiertes Implantatnachsorgeprogramm alle drei Monate mit professioneller Implantatreinigung und Evaluierung der klinischen Parameter kann dieser Zustand im besten Fall ein Leben lang erhalten werden.

Tab. 4: AKUT-Konzept – Therapiemodule.34
Schlussfolgerungen für die Praxis
Die Periimplantitis ist eine ernst zu nehmende, sekundäre Komplikation bei Implantaten mit einer Prävalenz von zehn Prozent der Implantate und 20 Prozent der Patienten. Die Reaktionen der periimplantären Gewebe bei bakterieller Infektion führen zu rascheren Destruktionen des Weichgewebes und zu schnellerem Tiefenwachstum der Läsionen als am Zahn. Eine schlechte Mundhygiene, eine anamnestische oder bestehende Parodontalerkrankung und Rauchen sind wichtige Risikofaktoren für die Ausbildung einer Periimplantitis. Diese und andere Risikofaktoren gilt es im Vorfeld der Implantation und auch bei bestehender Periimplantitis auszuschließen. Ein strukturiertes Implantatvor- und -nachsorgeprogramm mit Erhebung aller auch in der Parodontologie wichtigen diagnostischen Parameter ist integraler Bestandteil der täglichen zahnärztlichen Praxis.
Derzeit liegen für nichtchirurgische und chirurgische Periimplantitistherapien nur sehr wenige, qualitativ hochwertige Studien vor. Daher ist es auch schwierig, eindeutige Therapieempfehlungen auszusprechen. Des Weiteren zeigt der in Auszügen präsentierte klinische Fall, dass auch bei Patienten mit parodontalen Erkrankungen eine Implantation möglich ist, wenn eine optimale Diagnostik, Vorbehandlung und Nachsorge durchgeführt wird.
Autoren: Dr. Tim Backhaus, Dr. med. Dr. med. dent. Torsten Erdsach, Priv.-Doz. Dr. Dr. Matthias Kreppel
Hier gibt es die vollständige Literaturliste