Oralchirurgie 09.09.2024
Der Speichel als Spiegelbild oraler und systemischer Erkrankungen
share
Speichel wird von den drei paarigen großen und den zahlreichen in der Mukosa lokalisierten kleinen Glandulae salivariae in Abhängigkeit vom jeweiligen Drüsentyp in unterschiedlicher Zusammensetzung sezerniert. Bei gesunden Personen werden pro Tag durchschnittlich 0,6 bis 1,5 l Speichel in die Mundhöhle freigesetzt.12 Für die orale Gesundheit sind sowohl die Menge als auch die qualitative Komposition und die Inhaltsstoffe der Saliva von Bedeutung.
Bei einer Reduktion der Sekretionsrate unter 0,1 ml/min Ruhespeichel und unter 0,5 ml/min bei Stimulation spricht man von Hyposalivation, welche meist mit dem subjektiven Empfinden einer Mundtrockenheit (Xerostomie) einhergeht. Speichelmangel führt zu Kau- und Schluckbeschwerden und häufig auch zu einem „Burning-Mouth-Syndrom“. Der fehlende protektive Pellikel auf den oralen Hart- und Weichgeweben exponiert die Schleimhaut und die Zahnoberflächen zu exogenen Noxen.6 Die Prävalenz der Hyposalivation liegt in der Bevölkerung bei immerhin 20 Prozent, in der Altersgruppe der über 65-Jährigen sogar bei 30 bis 50 Prozent. Die Ursachen sind heterogen und reichen von primären und sekundären Erkrankungen der Speicheldrüsen wie Sialadenose, dem Sjögren-Syndrom, chronischen dyschylischen Sialadenitiden und den Nebenwirkungen einer tumorbedingten Radiatio im Kopf-Hals-Bereich bis zu Auswirkungen systemischer Krankheiten. Zu letzteren zählen metabolische Störungen wie Diabetes, Autoimmunerkrankungen und psychische Probleme. Dazu kommen die sehr häufigen speichelflusshemmenden Nebenwirkungen diverser Dauermedikationen.13, 19, 22 Besonders ZNS-wirksame Medikamente, wie Antihistaminika, Neuroleptika, Sedativa und Antidepressiva, Antihypertensiva (vor allem β-Blocker), α-Rezeptorblocker, sowie Parasympathiolytika wie Atropin und Scopalamin29, hemmen die Speichelbildung. Auch Nikotin als Ganglienblocker wirkt über die Verlängerung der Depolarisationszeit an den postsynaptischen Membranen reduzierend auf den Speichelfluss. Eine sorgfältige Evaluation der Grunderkrankungen und regelmäßige Aktualisierung der Medikamentenanamnese sind daher Voraussetzung für die Ursachenfindung.
Komponentenverarmung bei Speichelmangel
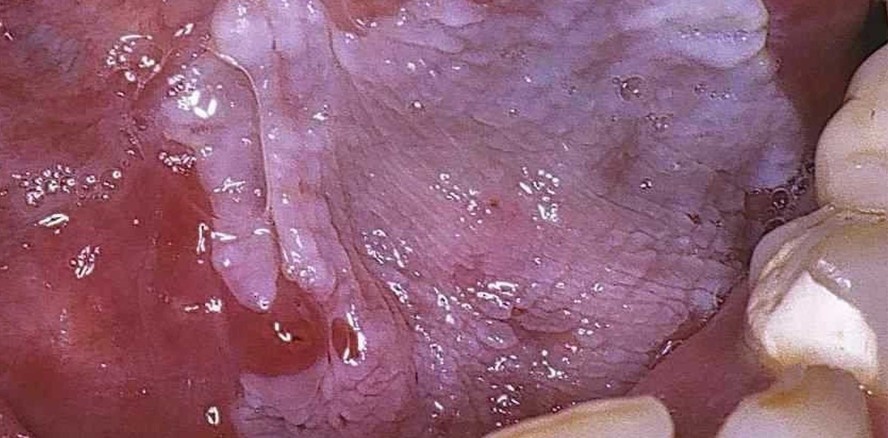
Speichel enthält zahlreiche antimikrobielle Faktoren wie Laktoperoxidase, Lysozym, Histatin, Laktoferrin und den spezifischen Antikörper IgA. Eine Verringerung der Saliva führt zu einer Reduktion dieser Komponenten und hat eine pathologische Veränderung des oralen Mikrobioms zur Folge.8, 9, 30 Erregerassoziierte Läsionen und Entzündungen wie Karies, Gingivitis, Parodontitis und Stomatitis korrelieren in vielerlei Hinsicht mit der Menge und der Zusammensetzung des Speichels. Die bei Hyposalivation verminderte Pufferkapazität bedingt eine überproportionale Vermehrung säuretoleranter Bakterien.1 Dazu gehören vor allem die Erreger und Betreiber der dentalen Karies. Die Interaktion von Streptococcus mutans mit einem ausreichenden Angebot an fermentierbaren Kohlenhydraten führt zur Entstehung primärer Läsionen.10 Zudem begünstigt der niedrige pH-Wert die Bildung von Zahnstein (Abb. 1). Eine Veränderung der wirtseigenen Modulations- und Abwehrmechanismen destabilisiert die orale Biozönose und führt über eine Artenverarmung dieses Kleinökosystems zu einem Überhandnehmen des Anteils kariogener Bakterien zu Ungunsten der normalen Residentflora.5 Neben S. mutans haben auch weitere Keime wie Lactobacillus, S. sanguis, S. mitis, Bifidobakterien und bestimmte Actinomyces-Arten kariogenes Potenzial. Saurer pH-Wert und die eingeschränkte lokale Immunabwehr begünstigen das Wachstum des Sprosspilzes Candida albicans. Candida bildet durch die Produktion spezifischer Vitamine eine kariesfördernde Symbiose mit S. mutans, beteiligt sich an der Progression parodontaler Läsionen und verursacht den häufig mit der Xerostomie einhergehenden Soor27 (Abb. 2). Speichel ist mit einem Gehalt von 108 bis 109 CFU (colony forming units/ml) ein Reservoir für orale Mikroorganismen und bietet sich daher für bakterielle Speicheltests an. Während für den Nachweis parodontalpathogener Keime und deren Biofilmaktivität der Sulkusfluid das geeignetere Medium darstellt, kommen Speicheltests auf S. mutans, Lactobacillus und Candida in der Kariesdiagnostik zum Einsatz. Hohe Konzentrationen dieser Mikroorganismen stehen in Zusammenhang mit dem Vorhandensein und der Progression kariöser Läsionen und haben hinsichtlich ihrer Vorhersagekraft für eine Erkrankung hohe Spezifität aber unzureichende Sensitivität. Ein negativer S. mutans-Test korreliert zwar mit Zahngesundheit, ein positiver Nachweis ist aber nicht zwingend mit der Genese von Karies korreliert. Die Tests sind aber dennoch ein probates Hilfsmittel bei der Evaluierung eines möglichen Risikos.32
Antikörper und Enzyme als Zeichen der Dysbiose
Speichel ist ein Reservoir biologischer Markersubstanzen, welche den aktuellen Zustand der oralen Strukturen abbilden.24 Er steht mit sämtlichen Geweben im Mund in unmittelbarem Kontakt und nimmt dabei Antigene, Stoffwechselprodukte des Mikrobioms und reaktiv gebildete Komponenten und Mediatoren des Wirtsorganismus auf. Durch den Reiz bakterieller Komponenten steigt die Menge an IgA und es werden Metalloproteinasen wie Kollagenase-2 und Gelatinase-B freigesetzt, welche sich nicht nur gegen die Bakterien, sondern auch gegen das Bindegewebe und die extrazellulären Matrixproteine des Parodonts richten.16 Der Level dieser Proteinasen korreliert signifikant mit dem Gingiva-Blutungsindex und der Tiefe der Zahnfleischtaschen. Die Konzentration bestimmter Interleukine, vor allem IL-1β und IL-1α steht in Zusammenhang mit der Aktivität der knochenabbauenden Osteoklasten.18 Des Weiteren sind im Speichel antimikrobielle Peptide wie Defensine und Histatine vermehrt nachweisbar.7, 23 Bei nekrotischen destruierenden Prozessen sind Enzyme wie alkalische Phosphatase und Aspartat-Aminotransferase erhöht. Auch Biomarker wie Kalzium, Peroxidase und die Menge an Speichel-IgA korrelieren mit dem Ausmaß der Entzündung.
Krankheitsbedingte Variabilität des Speichelproteoms
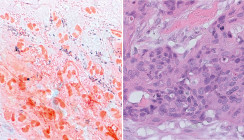
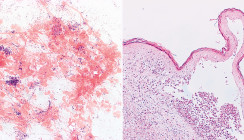
Moderne genomische Technologien ermöglichen eine Untersuchung des Proteoms der Saliva.11 Unter diesem versteht man die Gesamtheit der Speicheleiweiße, welche ständigen Veränderungen und Variationen durch Stoffwechsel, Synthese und Zelltod (Apoptose) unterworfen ist. Bisher konnten über 3.000 unterschiedliche Proteine und Peptide analysiert werden. Da zahlreiche Grunderkrankungen unseres Organismus auch Manifestationen in der Mundhöhle haben, ist es nicht verwunderlich, dass diese sich im Proteom des Speichels darstellen. Bestimmte Krankheiten beeinflussen nicht nur das orale Mikrobiom, sie destabilisieren auch das ökologische Gleichgewicht des Proteoms in typischer Art und Weise. Vergleiche ergaben charakteristische Zunahme oder Abnahme bestimmter Komponenten in Zusammenhang mit oralen und systemischen Krankheitsbildern.17, 20 Es zeigen sich deutliche Unterschiede zwischen gesunden physiologischen und pathologischen Konditionen. Interessante Forschungsergebnisse gibt es für präkanzeröse orale Vorläuferläsionen, wie die orale Leukoplakie und für das orale Plattenepithelkarzinom (OSCC; Abb. 3 und 4). Letzteres hat wegen seiner oft späten Erstdiagnose eine entsprechend schlechte Prognose. Auf das Vorhandensein eines OSCC können über 22 hochregulierte Proteinbiomarker hinweisen.2, 21, 25 Diese sind nicht ausschließlich für kanzerogene Prozesse charakteristisch, aber in Zusammenhang mit Tumorgenese und Progression vermehrt nachweisbar. Unter anderem sind dies IL-6, IL-8 und Cyklin D1, welches als Onkogen beschleunigte Zellproliferation induziert.26 Resistin alteriert inflammatorische Pathways und korreliert mit fortgeschrittenen invasiven Karzinomen und der Metastasierung in die regionären Lymphknoten.Bei Autoimmunerkrankungen wie dem primären Sjögren- Syndrom (pSS), der systemischen Sklerose, dem systemischen Lupus erythematodes (Abb. 5) und Formen der rheumatoiden Arthritis findet man im Speichel erhöhte Werte für Thymosin β, wobei beim Sicca Syndrom speziell Tβ4 und Tβ10 exprimiert werden. Bei pSS konnten Aberrationen von insgesamt 88 Metaboliten im Speichel festgestellt werden, davon 41 in deutlich reduzierter Konzentration. Besonders die verringerten Anteile von Glycin, Tyrosin, Harnsäure und Fucose, eines essenziellen Zuckers für die Zellkommunikation, weisen auf die krankheitsbedingte Destruktion des Drüsenepithels und die chronische Sialadenitis hin.4, 28, 31
Psychische Erkrankungen verändern Inhaltsstoffe des Speichels
Stress und Depression können neben zahlreichen körperlichen Symptomen wie Atem- und Kreislaufstörungen, kardialen Problemen und gastroenteralen Beschwerden auch die orale Gesundheit beeinträchtigen.3 Die übermäßige Produktion von Kortisol und/oder CRH über die Achse Hypothalamus – Hypophyse – Nebennierenrinde, sowie eine Überaktivierung des Neurotransmitters Acetylcholin führen zu verringerter Speichelbildung und Mundtrockenheit mit den bekannten Folgen für die oralen Gewebe. Im mengenmäßig oft drastisch reduzierten Speichel kann man bei diesen Patienten parallel zu den Blutwerten erhöhtes salivarisches Cortisol nachweisen. Psychische Erkrankungen wie Schizophrenie und bipolare Störungen können sich im Speichel durch eine Erhöhung von α-Defensin 1–4, Cystatin A und S und des granulozytären Proteins S100A12 abbilden.14, 15 Proteomverschiebungen durch Dysregulation immunologischer Pathways von weißen Blutkörperchen stehen auch in Zusammenhang mit frühmanifesten Alzheimererkrankungen, dem Down-Syndrom und der genetisch bedingten Kupferspeicherkrankheit Morbus Wilson.Die Erforschung des Speichelproteoms ist derzeit in erster Linie noch Gegenstand wissenschaftlicher Untersuchungen. Der routinemäßige Einsatz für zahn- und allgemeinmedizinische Fragestellungen bedarf weiterer Ergebnisse. Dennoch bietet die Analyse des Speichelproteoms eine nicht zu unterschätzende Zukunftsperspektive für die nichtinvasive Diagnostik oraler und systemischer Krankheiten.
Eine Literaturliste steht Ihnen hier zum Download zur Verfügung.
Dieser Beitrag ist im OJ Oralchirurgie Journal erschienen.