Parodontologie 21.11.2017
Das orale Mikrobiom
share
Parodontitis gezielt diagnostizieren und behandeln
Die Symbiose mit unserem individuellen Mikrobiom ist neuesten Erkenntnissen zufolge von fundamentaler Wichtigkeit für unsere Gesundheit. Ist das Gleichgewicht zwischen dem Wirt und seinen körpereigenen Bakterien gestört, können Krankheiten entstehen. Auch die Parodontitis stellt letztlich eine Entgleisung des oralen Mikrobioms dar, bei der parodontopathogene Bakterien die natürliche Standortflora überwuchern. Ein Hauptziel der Parodontitistherapie muss deshalb die Reetablierung einer ausbalancierten oralen Mikroflora sein.
Neue molekularbiologische Technologien erlauben heute eine differenziertere Sicht auf die den menschlichen Körper besiedelnden Mikroorganismen.25, 27 Dabei zeichnet sich ab, dass wir enge Wechselwirkungen mit den Bakterien eingehen, die unseren Darm, unsere Haut oder unsere Mundhöhle bevölkern.
Der menschliche Körper – ein Holobiont
Untersuchungen der israelischen Wissenschaftler Sender et al.21 zufolge besteht der menschliche Körper im Durchschnitt aus rund 30 Billionen Zellen, ist aber von etwa 39 Billionen Mikroorganismen besiedelt. Zusammen mit diesem aus verschiedensten Bakterien bestehendem, hochorganisierten Mikrobiom bildet unser Körper ein symbiontische Gemeinschaft, einen sogenannten Holobionten.14
Das menschliche Mikrobiom wird vom Körper nicht nur geduldet, sondern ist wichtig für unsere Gesundheit. Es hat Anteil an einer Reihe essenzieller Stoffwechselvorgänge wie Ernährung und Verdauung, Energiegewinnung und Fettspeicherung. Auch an Abbau und Entgiftung von Umweltstoffen, der Entwicklung und Regulation von Immunreaktionen sowie dem Schutz vor Invasion und Wachstum pathogener Mikroorganismen ist unser Mikrobiom beteiligt.11, 16
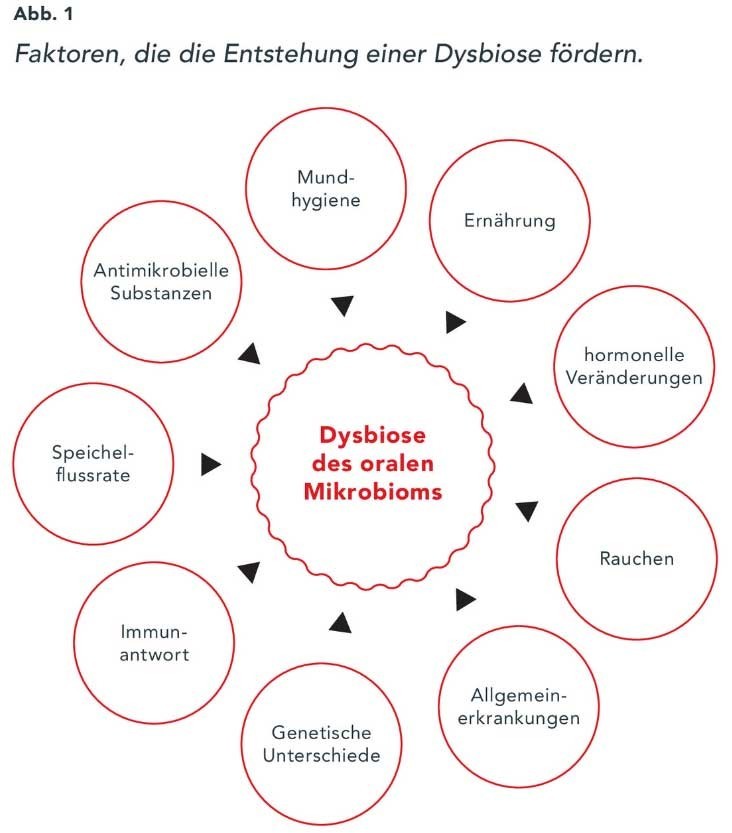
Die Zusammensetzung der Bakteriengemeinschaften ist sowohl von Mensch zu Mensch als auch an den einzelnen Besiedlungsorten unterschiedlich. Erworben wird das individuelle Mikrobiom vor allem durch das familiäre Umfeld. Eine erste Kolonisierung findet bereits im Geburtskanal statt und wird durch das Stillen modifiziert.14 Das Verhältnis zwischen Mikrobiom und Wirt ist dabei dynamisch und wird vor allem durch äußere Bedingungen und somit auch durch viele Aspekte des modernen Lifestyles beeinflusst (Abb. 1). Ernährung, Stress, Tabakkonsum, hormonelle Veränderungen, schlechte Mundhygiene oder Allgemeinerkrankungen können unser Mikrobiom verändern. Dies kann zu einem Zustand führen, in dem das sensible Ökosystem außer Balance gerät und eine Dysbiose entsteht – mit signifikanten Folgen für die Gesundheit.10, 11, 14, 27
Parodontitis: Entgleisung der oralen Symbiose
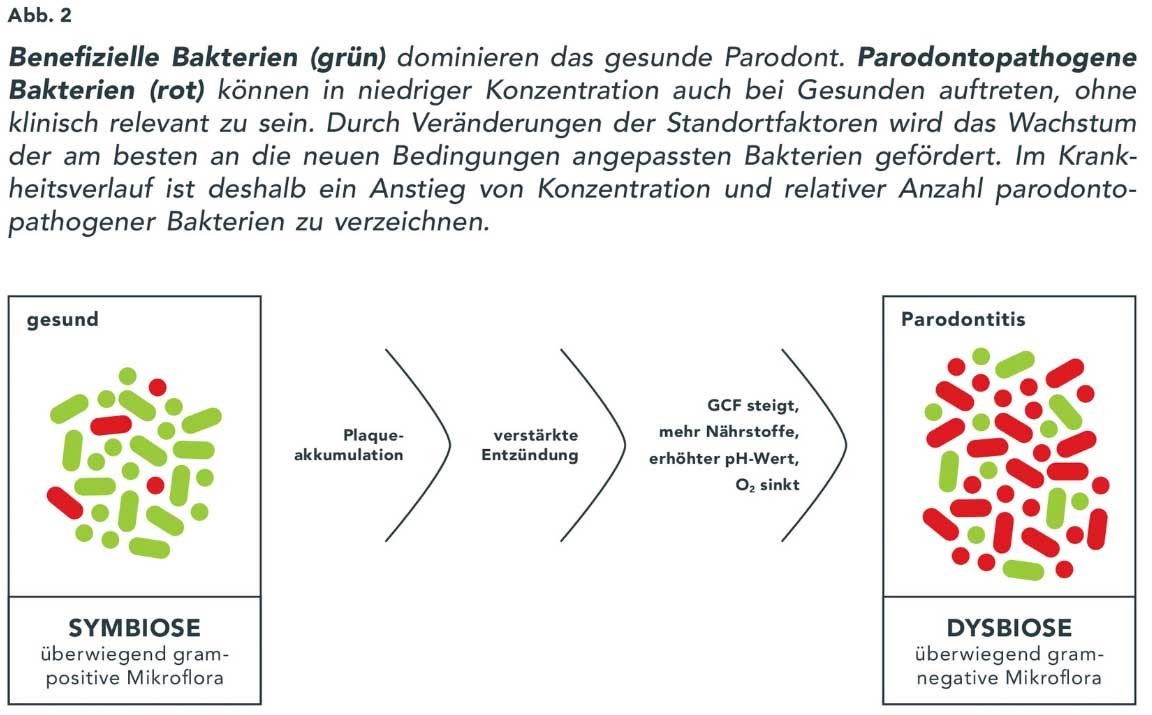
Im Rahmen des „Human Microbiome Project“ wurde festgestellt, dass die bakterielle Besiedlungsdichte im Darm und an den Zähnen am größten ist.25, 27 Das „Biotop Mundhöhle“ weist dabei einige Besonderheiten auf. Aufgrund von hoher Feuchtigkeit und optimaler Temperatur herrschen ideale Bedingungen für bakterielles Wachstum. Mit Zähnen, Zunge, Gingiva, Wangenschleimhaut und Zahnfleischtaschen stellt es eine Reihe unterschiedlichster Habitate mit verschiedenen Standortbedingungen zur Verfügung.14 Das gesunde Parodont wird dominiert von grampositiven, aeroben Bakterienspezies, die für die Aufrechterhaltung der oralen Symbiose eine wichtige Rolle spielen.4 Aber auch im Sulkus parodontal Gesunder sind parodontopathogene Keime vorhanden.Sie machen allerdings nur einen geringen Anteil der subgingivalen Mikroflora aus und können vom Immunsystem des Wirtes und der benefiziellen Flora unter Kontrolle gehalten werden.2, 15, 17, 18
Bei der Akkumulation von Plaque an der marginalen Gingiva kommt es zu einer lokalen Entzündung. Dies bedingt eine gesteigerte Fließrate der Sulkusflüssigkeit sowie einen Rückgang des sulkulären Sauerstoffgehalts. Dadurch wird vor allem das Wachstum anaerober bzw. fakultativ anaerober, parodontopathogener Bakterien gefördert (Abb. 2). Die Sulkusflüssigkeit enthält viele Proteine, die insbesondere den vorwiegend proteolytischen PA-Keimen als Nährstoffe dienen. Dadurch bietet die Zahnfleischtasche den Parodontitisbakterien optimale Lebensbedingungen und einen Standortvorteil gegenüber den benefiziellen Bakterien. Diaz et al.5 konnten zeigen, dass die Gesamtbakterienzahl bei der Entwicklung einer Parodontitis um das 1.000-Fache ansteigt, der prozentuale Anteil der benefiziellen Keimen jedoch zurückgeht. Da gleichzeitig der Anteil parodontopathogener Spezies und damit auch deren Konzentration signifikant ansteigt, entgleist das mikrobiologische Gleichgewicht. Die Symbiose wird zur Dysbiose.1, 2, 5, 10, 11, 14, 15, 16
Das subgingivale Keimspektrum – eine komplexe Gemeinschaft
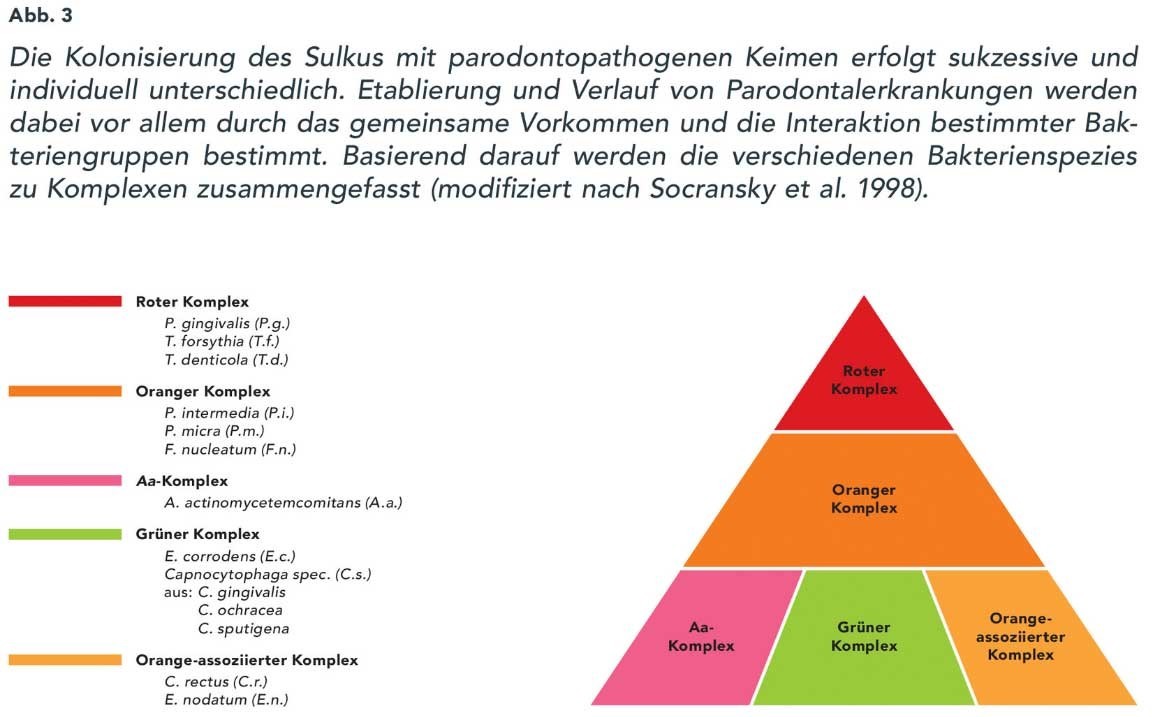
Socransky und Haffajee23 haben in ihrer bahnbrechenden Arbeit zur Komplextheorie die Veränderungen der metabolisch und physikalisch interagierenden Bakteriengemeinschaften der Zahnfleischtasche im Verlauf einer parodontalen Erkrankung untersucht. Sie konnten zeigen, dass sich Zusammensetzung und Konzentration der verschiedenen Bakteriengruppen als Reaktion auf die modifizierten Standortfaktoren ändern. Die Arbeitsgruppe ordnet die einzelnen Bakterienspezies gemäß ihrer Pathogenität und ihrer Rolle im Rahmen der Parodontitispathogenese verschiedenen Komplexen zu (Abb. 3).
Insbesondere die Vertreter des Roten Komplexes sind durch die Bildung verschiedener Enzyme und Virulenzfaktoren maßgeblich an der Zerstörung des Weich- und Knochengewebes beteiligt. Ähnlich dem hochpathogenen Aggregatibacter actinomycetemcomitans besitzen sie zudem die Fähigkeit, Epithelzellen zu invadieren und können deshalb durch eine rein instrumentelle Reinigung oft nur ungenügend entfernt werden. Daher ist vor allem bei Vorliegen von Aggregatibacter actinomycetemcomitans oder Rot-Komplex- Bakterien häufig eine antibiotische Begleittherapie nötig.8, 13, 19, 23, 24, 26
Antibiotika: Gezielte Therapie statt Schrotschuss
Eine Parodontitistherapie muss darauf abzielen, bestehende Entzündungen zu beseitigen, den Anteil parodontopathogener Bakterien zu reduzieren und wieder symbiontische, mikrobiologische Verhältnisse herzustellen.20, 22 Insbesondere bei Vorliegen gewebeinvasiver PA-Keime kann der unterstützende Einsatz eines systemischen Antibiotikums notwendig sein, um die verantwortlichen Bakterien nachhaltig zur reduzieren und die parodontale Situation langfristig zu stabilisieren.7, 9, 12, 19
Welcher antibiotische Wirkstoff optimalerweise dazu eingesetzt werden sollte, richtet sich maßgeblich nach Konzentration und Zusammensetzung der Subgingivalflora. Die antibiotische Therapie sollte dabei möglichst spezifisch auf die Parodontitisbakterien abzielen. Vor allem Kombinationstherapien mit mehreren Wirkstoffen haben häufig zur Folge, dass auch benefizielle Bakterienspezies abgetötet werden. Dies sollte – wann immer möglich – vermieden werden, denn die benefizielle Flora ist zur Reetablierung gesunder parodontaler Verhältnisse und zur Wiederherstellung der Symbiose essenziell.4, 6, 12
Da das subgingivale Keimspektrum von Patient zu Patient unterschiedlich ist, kann die Auswahl eines optimal wirksamen Antibiotikums nur auf Basis einer mikrobiologischen Analyse erfolgen.3, 26 Deshalb empfiehlt auch die DG PARO/DGZMK in ihrer Stellungnahme zum Einsatz systemischer Antibiotika im Rahmen der Parodontaltherapie, dass „[…] zur Auswahl eines geeigneten Antibiotikums die vorliegende parodontale Infektion durch eine mikrobiologische Analyse der subgingivalen Plaque bestimmt werden [soll].“ Die Fachgesellschaften betonen darüber hinaus, dass „[…] die intra- und extraorale physiologische Keimflora jedoch möglichst wenig verändert werden [soll].“3
Mikrobiologische Tests (zum Beispiel micro-IDent® und micro-IDent®plus, Hain Lifescience GmbH) sind demnach ein wichtiges Hilfsmittel im Rahmen der antibiotikaunterstützten Parodontaltherapie, da sie sowohl dieZusammensetzung des subgingivalen Keimspektrums als auch die Konzentrationen der untersuchten Bakterienspezies bestimmen können. Das Testergebnis erlaubt eine spezifische, auf den Patienten abgestimmte antibiotische Unterstützung der mechanischen Parodontaltherapie nach dem Prinzip „so viel wie nötig und so wenig wie möglich“. Nur so ist eine gezielte Reduktion der parodontopathogenen Erreger bei maximaler Schonung der benefiziellen Flora und somit die Reetablierung einer gesunden subgingivalen Mikrobiota möglich.
Fazit
Die parodontale Gesundheit wird maßgeblich vom Zustand der mikrobiologischen Symbiose bestimmt. Gerät diese aus dem Gleichgewicht, dominieren parodontopathogene Bakterien die subgingivale Flora, welche das Entzündungsgeschehen und den Abbau des parodontalen Halteapparates ständig weiter vorantreiben.
Um die symbiontischen Verhältnisse wiederherzustellen, müssen einerseits die PA-Bakterien gezielt reduziert und andererseits die benefizielle Flora möglichst geschont werden. Ist im Rahmen der Parodontitistherapie eine unterstützende Antibiotikabehandlung notwendig, ermöglichen mikrobiologische Analysen des subgingivalen Keimspektrums eine zielgerichtete Behandlung. So kann die im Verlauf der Erkrankung entstandene Dysbiose optimal bekämpft und ein mit gesunden parodontalen Verhältnissen assoziiertes, symbiontisches Gleichgewicht wiederhergestellt werden.
Die vollständige Literaturliste gibt es hier.
Der Beitrag ist in der ZWP Zahnarzt Wirtschaft Praxis 11/2017 erschienen.