Parodontologie 22.09.2015
Adjuvante Antibiotika: Ist die klinische Diagnose ausreichend
share
Die Frage, ob sich eine systemische Antibiose im Rahmen einer Parodontalbehandlung lediglich am vorliegenden klinischen Bild orientieren oder auf dem Ergebnis einer mikrobiologischen Keimanalyse basieren sollte, sorgt immer wieder für lebhafte Diskussionen.
So diskutierten auch drei hochkarätige Experten – die Professoren David Herrera, Arie van Winkelhoff und Andrea Mombelli – auf der EuroPerio8 in London über die Notwendigkeit einer diagnostisch-basierten Antibiose im Zuge der PA-Therapie. Dabei kristallisierte sich klar heraus, dass der Stellenwert der mikrobiologischen Diagnostik für die PA-Therapie unverändert hoch ist. Vor dem Hintergrund der zunehmenden, vor allem allgemeinmedizinisch relevanten Resistenzproblematik bewertete die Mehrheit der Experten den unreflektierten Einsatz von Antibiotika als unverantwortlich.
Die offiziellen Empfehlungen der DGParo/DGZMK zum Einsatz systemischer Antibiotika in der Parodontitistherapie sind in der diesbezüglichen Stellungnahme klar umrissen. So wird eine unterstützende Antibiose in der Regel nur bei schweren, therapieresistenten oder aggressiven Verlaufsformen sowie bei moderaten Parodontitiden in Verbindung mit systemischen Erkrankungen bzw. vorliegender Beeinträchtigung des Immunsystems empfohlen.1 Grundsätzlich wird eine flankierende Antibiotikatherapie dann als sinnvoll erachtet, wenn initial durchgeführte Mundhygiene- oder mechanische Reinigungsmaßnahmen nicht den gewünschten Erfolg erzielen konnten. Zeigt das klinische Bild trotz sorgfältigem SRP (Scaling and Root Planing) und entsprechender Compliance des Patienten keine deutliche Besserung, so halten für gewöhnlich gewebsinvasive Keime oder Bakterien in für die mechanische Therapie schwer zugänglichen Bereichen die Infektion aufrecht. In diesen Fällen kann eine unmittelbar nach Desintegration des Biofilms einsetzende Antibiose die parodontopathogenen Markerkeime nachhaltig reduzieren und den Therapieerfolg langfristig sichern.1, 5, 9
Gezielte Parodontitistherapie
Die Parodontitis ist eine polybakterielle Infektion. Das heißt, die Erkrankung wird durch eine Gruppe verschiedener Bakterien ausgelöst, die in ihrer Zusammensetzung und Konzentration von Patient zu Patient deutlich variiert.6,10 Die Entscheidung, ob der Einsatz eines Antibiotikums überhaupt notwendig ist und welcher Wirkstoff die jeweils vorliegenden Mikroorganismen möglichst gezielt angreift, kann somit nur auf Basis einer mikrobiologischen Diagnostik getroffen werden.7,12 Die generelle Applikation des Winkelhoff-Cocktails (d.h. der Kombination aus Amoxicillin und Metronidazol) bei Parodontitiden mit schweren Verlaufsformen ohne diagnostische Absicherung, wie von einigen Parodontologen empfohlen, nimmt daher die unnötige oder zu breit wirkende Antibiose von etwa 75 Prozent der Patienten billigend in Kauf2 (Abb. 1).
Metaanalyse von 169.512 Sulkusproben parodontal erkrankter Patienten mittels molekulargenetischer Analyse auf fünf Markerkeime (micro-IDent®, Hain Lifescience GmbH, Nehren). Aufgrund des gefundenen Bakterienprofils wurde jeweils der optimal wirksame antibiotische Wirkstoff bestimmt. Nur 23,67 Prozent der Untersuchten hätten eine Therapie mit dem Winkelhoff-Cocktail (Amoxicillin und Metronidazol) benötigt. Mehr als 75 Prozent der untersuchten Patienten wären ohne vorherige mikrobiologische Analyse übertherapiert worden.2
Verschärfte Resistenzsituation
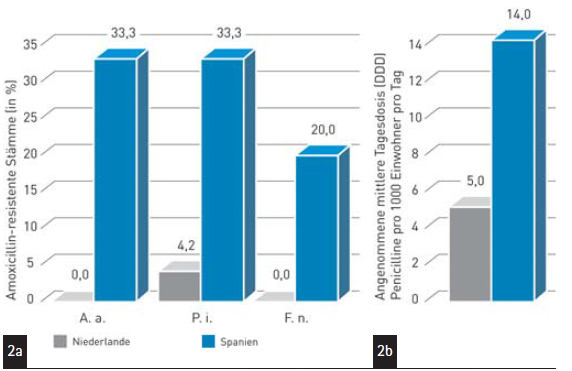
Vor dem Hintergrund weltweit deutlich ansteigender Antibiotikaresistenzen, die insbesondere in der Zunahme multiresistenter Bakterienspezies wie zum Beispiel dem Krankenhauskeim MRSA deutlich wird, warnten daher auch die Experten auf der EuroPerio8 vor dem unreflektierten Einsatz von Antibiotika im Zuge der Parodontaltherapie. „Dies mache insbesondere ein Vergleich der Resistenzen gegen die in der PA-Therapie häufig eingesetzten Wirkstoffe bei Parodontalpathogenen von niederländischen und spanischen Patienten deutlich“, so die Professoren van Winkelhoff und Herrera (Abb. 2a).
Abb. 2: a) Anteil Amoxicillin-resistenter Stämme von Aggregatibacter actinomycetemcomitans (A.a.), Prevotella intermedia (P.i.) und Fusobacterium nucleatum (F.n.) in den Niederlanden und Spanien. Im Vergleich ist dieser Anteil in den Niederlanden deutlich niedriger als in Spanien (adaptiert nach Literaturverweis 11). b) Der Pro-Kopf-Verbrauch von Penicillinen (inkl. Amoxicillin) ist in Spanien deutlich höher als in den Niederlanden (adaptiert nach Literaturverweis 13).
Der in Spanien signifikant höhere Pro-Kopf-Verbrauch von Antibiotika (Abb. 2b) wirkte sich direkt negativ auf die Resistenzentwicklung der Infektionserreger aus, während sich die niederländische Zurückhaltung im Einsatz antibiotischer Wirkstoffe auch in der deutlich geringeren Resistenzrate bei den parodontalpathogenen Keimen reflektierte.11 Die weltweit erhobenen Daten der World Health Organization (WHO) und des European Centre for Disease Prevention and Control (ECDC) sprechen gemäß den in London präsentierten Daten eine noch deutlichere Sprache: als Konsequenz zunehmender Resistenz bakterieller Krankheitserreger gegen Antibiotika nimmt sowohl die Anzahl der Todesfälle durch multiresistente MRSA, Mykobakterien etc. als auch das Ausmaß der verursachten Kosten in den letzten Jahren merklich zu.3,13 Das Votum der Spezialisten für eine mikrobiologische Diagnostik vor dem Einsatz von Antibiotika war daher eindeutig und durch eine Reihe von Argumenten untermauert. So erachten sie aufgrund der der Parodontitis zugrunde liegenden polymikrobiellen und individuell unterschiedlichen Keimflora die personalisierte Medizin als unbedingt empfehlenswert: nur auf Basis einer mikrobiologischen Analyse ist ein wirksames, möglichst gezielt auf die jeweils vorliegenden Erreger ausgerichtetes Antibiotikum zu ermitteln.
Ferner machten sie klar, dass die Parodontitis keine Akutsituation darstelle und eine fundierte Diagnostik somit keinem zeitlichen Druck unterliege. Den Empfehlungen von WHO und ECDC folgend, forderten die Vortragenden daher eindringlich dazu auf, den unnötigen Einsatz von Antibiotika zu vermeiden und die Anwendung möglichst gezielt wirkender Präparate zu favorisieren.3,13 Unter diesem Aspekt erteilten sie einem Einsatz des Winkelhoff-Cocktails, der sich ohne mikrobiologische Grundlage nur am klinischen Bild orientiert, eine eindeutige Absage.
Fazit
Als Fazit erging der Appell an die Zuhörer, die mikrobiologische Diagnostik als wichtiges Hilfsmittel im verantwortungsvollen Umgang mit Antibiotika und zur Therapie parodontaler Erkrankungen zu nutzen, um diese wertvolle Waffe im Kampf gegen Infektionserkrankungen nicht wirkungslos werden zu lassen.
Die Literaturliste steht hier zum Download bereit.